Křemík
Křemík (chemická značka Si, latinsky Silicium) je polokovový prvek, hojně se vyskytující v zemské kůře. Slouží jako základní materiál pro výrobu polovodičových součástek, ale i jako základní surovina pro výrobu skla a významná součást keramických a stavebních materiálů.
| Křemík | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ Periodická tabulka ↓ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obecné | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Název, značka, číslo | Křemík, Si, 14 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cizojazyčné názvy | lat. Silicium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina, perioda, blok | 14. skupina, 3. perioda, blok p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemická skupina | Polokovy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Koncentrace v zemské kůře | 257 000 až 282 000 ppm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Koncentrace v mořské vodě | 3
mg/l | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | Stříbřitě modrošedá látka | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Registrační číslo CAS | 7440-21-3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relativní atomová hmotnost | 28,0855 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | 111 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 111 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 210 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronová konfigurace | [Ne] 3s2 3p2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační čísla | −IV, −III, −II, −I, I, II, III, IV | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita (Paulingova stupnice) | 1,9 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| První | 786,5 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Druhá | 1577,1 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Třetí | 3231,6 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Látkové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografická soustava | Krychlová | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární objem | 12,06×10−6 m3/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota | 2,3290 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenství | Pevné | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tvrdost | 6,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak syté páry | 100 Pa při 2339K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 8433 m/s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 149 W⋅m−1⋅K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termodynamické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota tání | 1413,85 °C (1 687 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota varu | 3264,85 °C (3 538 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo tání | 50,21 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo varu | 359 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární tepelná kapacita | 19,789 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektromagnetické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrická vodivost | 4,35×10−4 S/m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Měrný elektrický odpor | 2300 Ω·m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standardní elektrodový potenciál | 1,12 V | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetické chování | Diamagnetický | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bezpečnost | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| R-věty | R36/38, R11, R36/37/38 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S-věty | S26, S36/37/39, S22 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Historie objevu
Křemík poprvé identifikoval roku 1787 Antoine Lavoisier jakožto složku pazourku a jiných křemíkatých hornin. Později, v roce 1800, jej Humphry Davy mylně považoval za sloučeninu. Roku 1811 Gay-Lussac a Thénard pravděpodobně vyrobili amorfní křemík zahříváním draslíku s tetrafluorosilanem. Křemík jakožto prvek byl poprvé izolován švédským chemikem J. J. Berzeliem roku 1823. Roku 1824 Berzelius získal amorfní křemík přibližně stejným postupem jako předtím Gay-Lussac. Berzelius také produkt přečistil opakovaným promýváním.
Názvy
Latinský název silicium je odvozen od slova silex (2. pád silicis), které označovalo formu křemene česky nazývanou pazourek.[1]
Český název křemík je jedním z neologismů, které zavedl v rámci nového českého chemického názvosloví Jan Svatopluk Presl ve svých knihách Lučba čili chemie zkusná (1828–35) a Nerostopis (1837). Český název prvku je odvozen od názvu křemen, jehož praslovanský kořen má souvislost buď s hořením (a slovy křesat či kremace) nebo s řezáním a sekáním (a např. slovem sekera).[2]
Základní fyzikálně-chemické vlastnosti
Jedná se o poměrně tvrdý polokov s vysokou afinitou ke kyslíku. Elementární křemík je na vzduchu neomezeně stálý, v okolní přírodě se s ním však setkáváme prakticky pouze ve formě sloučenin, v nichž se vyskytuje pouze v mocenství Si4+.
Je odolný vůči většině minerálních kyselin s výjimkou směsi kyseliny fluorovodíkové (HF) a kyseliny dusičné (HNO3), velmi snadno se však rozpouští v zásaditých roztocích (např. v hydroxidu draselném) za vzniku křemičitanového aniontu [SiO3]−2.
Výskyt v přírodě


V čisté podobě se křemík v přírodě nevyskytuje, setkáváme se pouze s jeho sloučeninami. Je po kyslíku druhým nejvíce zastoupeným prvkem v zemské kůře. Podle posledních dostupných údajů tvoří 26 – 28 % zemské kůry. V mořské vodě je jeho koncentrace poměrně nízká, pouze 3 mg Si/l, ve vesmíru připadá na jeden atom křemíku pouze přibližně 30 000 atomů vodíku.
Křemík je základní složkou velké většiny hornin tvořících zemskou kůru – příkladem mohou být pískovcové horniny, jíly, žuly a především aluminosilikátové horniny na bázi ortoklasu (aluminosilikáty obsahující draslík) nebo plagioklasu (aluminosilikáty obsahující sodík). Křemík se tedy vyskytuje prakticky ve všech vyvřelých horninách.
Mineralogicky je bezesporu nejvýznamnějším zástupcem křemen, chemicky oxid křemičitý SiO2. Minerály s tímto složením se liší barevně podle přítomnosti malých množství cizorodých prvků, které způsobují charakteristické zbarvení krystalického oxidu křemičitého. Téměř čistý oxid křemičitý je mineralogicky označován jako křišťál, fialově je zbarven ametyst (příměs Fe4+), žlutý je citrín (příměs Fe3+), růžový růženín (Mn2+), hnědý záhněda (příměs Al, Na, Li). Další, např. jaspis, se mohou vyskytovat v několika barevných variantách.
Zvláštní případ minerálu na bázi oxidu křemičitého je amorfní forma této sloučeniny – opál. Tento módní polodrahokam se vyskytuje v řadě barevných variant. V současné době se největší množství opálů dobývá v Austrálii a střední Americe včetně Mexika.
Z biologického hlediska patří křemík mezi biogenní prvky, i když jeho obsah v tkáních živých organismů není příliš vysoký. Uvádí se, že v těle dospělého člověka je přítomen přibližně 1 g křemíku a to především v kostech, chrupavkách a zubní sklovině, pro jejichž zdravý růst a vývoj je nezbytný. Zvýšený obsah křemíku v rostlinných buňkách můžeme nalézt např. v přesličkách nebo žahavých chloupcích kopřiv.
Mimořádně důležitý je křemík pro rozsivky, neboť jeho sloučeniny tvoří hlavní složku schránky těchto jednobuněčných řas, frustuly. Jde zejména o vodnatý polymer oxidu křemičitého, blízký opálu. Rozsivky jsou jedinou skupinou organismů, jejíž rozvoj je naprosto závislý na přítomnosti rozpustných forem oxidu křemičitého v prostředí. Po vyčerpání zdrojů křemíku se zastaví replikace DNA. Rozsivky jsou významnými primárními producenty biomasy, jejich biomasa tvoří 25% z celkového množství produkovaného rostlinami.
Výroba a využití

Křemík má také využití při výrobě skla, porcelánu, nebo cementu. Výroba křemíku v průmyslovém měřítku spočívá v redukci taveniny vysoce čistého oxidu křemičitého v obloukové elektrické peci na grafitové elektrodě, jejíž materiál je přitom spalován na plynný oxid uhelnatý podle reakce:
- SiO2 + 2C → Si + 2CO
za vzniku křemíku o čistotě 97 – 99 %. Pro účely elektronického průmyslu je ovšem tato čistota naprosto nedostatečná, neboť výroba elektronických součástek vyžaduje většinou křemík o čistotě minimálně 99,9999 %, protože i nepatrné znečištění výrazně ovlivňuje kvalitu vyrobených tranzistorů a dalších elektronických součástek.
Výroba vysoce čistého křemíku
Jednou z nejstarších metod pro přípravu vysoce čistého křemíku je zonální tavení. Čištěný materiál se nejprve upraví do tvaru dlouhé tenké tyče. Ta se potom ve speciální pícce postupně přetavuje tak, aby se tavená zóna posunovala od jednoho konce ke druhému. Přitom se nečistoty přítomné v materiálu koncentrují v roztavené zóně a postupně se dostávají ke konci tyče, který se nakonec odstraní odříznutím. Několikanásobným opakováním tohoto postupu vznikne poměrně vysoce čistý materiál.
V současné době se pro přípravu extrémně čistého křemíku používají chemické metody. V tzv. Siemensově postupu je z křemíku nejprve vyrobena nějaká těkavá sloučenina, obvykle trichlorsilan HSiCl3 nebo chlorid křemičitý SiCl4. Tyto plynné sloučeniny se potom vedou přes vrstvu vysoce čistého křemíku o teplotě přes 1 100 °C. Přitom dochází k jejich rozkladu a vzniklý vysoce čistý křemík se ukládá v krystalické podobě na původní křemíkovou podložku. Reakci trichlorsilanu vystihuje rovnice:
- 2 HSiCl3 → Si + 2 HCl + SiCl4
Uvedeným postupem vzniká tzv. polykrystalický křemík, který typicky obsahuje nečistoty v řádu jednotek ppb (1 : 1 000 000 000) a plně vyhovuje požadavkům pro výrobu elektronických polovodičových součástek.
Po určitou dobu byl alternativou k Siemensově metodě postup DuPontův, který vycházel z chloridu křemičitého a jeho rozkladu při teplotě 950 °C na vysoce čistém zinku podle rovnice:
- SiCl4 + 2 Zn → Si + 2 ZnCl2
Technické problémy s těkavostí vznikajícího chloridu zinečnatého, který následně znečišťoval vyrobený čistý křemík, vedly nakonec k tomu, že byl tento proces prakticky opuštěn.
Výroba monokrystalického křemíku

Jelikož pro výrobu některých polovodičových součástek je polykrystalický křemík nepoužitelný, používá se křemík monokrystalický. Obvyklou metodou pro jeho výrobu je řízená krystalizace z taveniny, nazývaná Czochralského proces. Při tomto postupu je do křemíkové taveniny vložen zárodečný krystal vysoce čistého křemíku.
Tento krystal se přitom otáčí a pulzuje podle předem přesně definovaného programu, přičemž teplota taveniny je také velmi pečlivě sledována a řízena. Celý proces probíhá v nádobách z velmi čistého křemene v inertní atmosféře argonu. Na zárodečném krystalu se pak vylučují další vrstvy mimořádně čistého křemíku, výsledný produkt (křemíkový ingot) pak může mít až 400 mm v průměru a délku do 2 m, tvořen je přitom jediným krystalem. Vyrobený ingot se po ochlazení řeže na tenké vrstvy (typicky 0,5 mm), leští a je použit jako výchozí surovina pro výrobu polovodičových součástek.
Slitiny
Metalurgický význam křemíku spočívá pouze ve výrobě některých speciálních slitin, v nichž jeho podíl představuje pouze jednotky procent. Nejznámější je ferrosilicium, slitina křemíku a železa, která se vyznačuje vysokou tvrdostí a chemickou odolností. Pro zvýšení tvrdosti se křemík v malém množství přidává i do speciálních ocelí a hliníkových slitin.
Rafinace křemíku
Chemická rafinace se provádí převedení na sloučeninu trichlorsilanu SiHCl3, a následná destilace, při níž se odstraní většina nečistot.
Fyzické rafinace:
- Pásmové tavení: Ingot se postupně natavuje po celé svojí délce, poté je postaven kolmo k zemi. Nečistoty mají jinou hustotu, a tak po skončení tavení zatuhnou na jednom konci křemíkové šišky. Poté jsou odříznuty. Několikanásobným opakováním tohoto postupu vznikne poměrně vysoce čistý materiál. Protože se potřebuje určitý typ polovodiče, P nebo N, dotuje se tedy před tažením určitým vodičem. Tato tyč je umístěna vertikálně donorem, nebo akceptorem, a tím se docílí vodivosti P nebo N.
- Řezání na „Salámky“: Po vytažení z kelímku už je hotový polovodič určeného typu, který se dále rozřezává na určené plátky, takzvané salámky. Salámky se řežou diamantovým řezačem, podobným strojem, který se používá na salám nebo chléb.
- Broušení – Lapování: Lapování je druh strojního obrábění. Technicky patří do broušení a leštění, neupravuje se jím geometrie ale drsnost materiálu. Dosahuje se jím až zrcadlový lesk materiálu. Jde o dokončovací operaci, při které dochází k úběru materiálu účinkem volných zrn brusiva, které se přivádí mezi lapovací nástroj a lapovaný povrch. Řezný pohyb volných zrn je vyvolán pohybem lapovacího nástroje, který je vůči lapované ploše nepravidelný. Proto se zrna brusiva pohybují po stále se měnících drahách, a tím zanikají stopy po předchozím obrábění.
- Odleptání: I přes dokonalé obroušení se musí salámek vyhladit leptáním slabou kyselinou, která zarovná veškeré nerovnosti. Po omytí a vyleštění po odleptání je salámek omyt v deionizované vodě, aby se odstranily zbytky kyseliny. Poté je salámek vyleštěn do vysokého lesku, a je připraven k dalšímu použití.
Polovodivé vlastnosti
Čistý křemík má z hlediska pásové struktury vlastnosti polovodiče. Z hlediska polovodivých aplikací se však častěji používá křemík s příměsí jiného prvku, což má za následek elektronovou resp. děrovou vodivost a snížení elektrického odporu. Vzniká tak polovodič typu n resp. p; takovýto materiál tvoří základ součástek jako jsou diody, tranzistory, fotovoltaické články a další.
Sloučeniny křemíku a jejich význam
Oxid křemičitý
Patrně nejvýznamnější anorganickou sloučeninou křemíku je oxid křemičitý, SiO2. Tato látka se vyskytuje v řadě modifikací se zcela odlišnými fyzikálně-chemickými vlastnostmi.
- Minerály na bázi SiO2 se ve formě polodrahokamů vyskytují v nejrůznějších barevných odstínech po celém světě.
- Zbarvení: fialová – ametyst, hnědá – záhněda, žlutá – citrin, bez barvy – křišťál
- Ve velkém množství okolních hornin je křemen přítomen ve formě žil a vrostlic. Při erozi hornin dochází k narušení její struktury a křemen je jako jedna z nejtvrdších a nejodolnějších součástí z horniny vyplavován ve formě křemenných písků, oblázků a valounů. Tento materiál slouží jako cenná surovina ve sklářském a stavebním průmyslu.
- V jílových horninách je křemík přítomen ve formě mikroskopických částic. Tyto horniny jsou základní surovinou v keramickém průmyslu a uplatňují se i při výrobě stavebních hmot (pálené cihly a tašky).
Sklo

V současné době se vyrábí stovky druhů skla pro nejrůznější praktické aplikace, které se liší fyzikálními vlastnostmi i vzhledem. Základní surovinou pro výrobu skloviny je směs, nazývaná sklářský kmen o přibližném složení: 50% písek (křemen nebo oxid křemičitý), 16% soda (uhličitan sodný), 12% vápenec (uhličitan vápenatý), 18% odpadní sklo (drcené střepy). Tato směs taví při teplotě kolem 1 500 °C a dále zpracovává především na výrobu lahví litím nebo foukáním.
- Přídavkem potaše, uhličitanu draselného se získává tabulové sklo pro výrobu oken, výkladních skříní apod. Sklovina přitom tuhne na vrstvě roztaveného cínu a vzniklé tabule mají zvlášť hladký povrch – plavené sklo.
- Sklo s vyšším obsahem olova se vyznačuje vysokým indexem lomu a je zvláště těžké. Olovnaté sklo se používá pro výrobu lustrů, bižuterie, ozdobných karaf a sklenic.
- Sklo pro výrobu optických přístrojů (čočky, hranoly, optické filtry) obsahuje kromě olova i baryum, zinek a titan.
- Skla borosilikátová mají část sklotvorného SiO2 nahrazenu oxidem boritým. Přísada oxidu hlinitého zvyšuje jejich pevnost a zlepšuje zpracovatelnost skloviny. Borosilikátová skla jsou žáruvzdorná a chemicky odolná. Slouží jako sklo laboratorní a varné využívané v domácnostech.
- Chemicky nejjednodušší je křemenné sklo, tavený čistý oxid křemičitý SiO2. Propouští ultrafialové záření, má výbornou chemickou tepelnou odolnost a snese prudké ochlazení, aniž popraská. Vysoká tavicí teplota kolem 1 800 °C a s tím spojená cena křemenného skla omezuje jeho praktické využití na výrobu laboratorních potřeb a speciálních žárovek.
- Na optické kabely se používá obzvlášť čisté a průhledné sklo.
Křemičitany

Křemík tvoří celou řadu kyslíkatých kyselin, z nichž nejjednodušší a nejznámější je kyselina křemičitá H2SiO3. V dalších kyselinách jsou za sebou řetězeny skupiny [SiO3]. Všechny uvedené kyseliny jsou poměrně slabé a nestálé. Běžně se však setkáváme s jejich solemi křemičitany, které jsou velmi stabilní.
Křemičitany alkalických kovů a kovů alkalických zemin jsou podstatnou součástí vyvřelých hornin, jílů, cihlářských hlín a dalších.
Velmi běžné jsou horniny na bázi hlinitokřemičitanů (aluminosilikátů), tzv. živce. Aluminosilátové minerály tvoří např. orthoklas KAlSi3O8 a plagioklas NaAlSi3O8 .
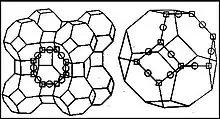
Velmi cenné jsou aluminosilikáty zvané zeolity, které vytvářejí komplikované prostorové sítě, složené z tetraedrů SiO4 a AlO4, vázaných navzájem sdílením svých vrcholových kyslíků. Tvoří vzájemně propojené kanály a dutiny, které obsahují slabě vázané, tedy v podstatě pohyblivé molekuly vody a kationy alkalických kovů (Na, K, Li, Cs) a alkalických zemin (Ca, Mg, Ba, Sr), které vyrovnávají nenasycenou negativní valenci AlO4. Zeolity se chovají jako přírodní iontoměniče nebo molekulová síta.
Keramika a stavební hmoty
Keramika je obecný název pro výrobky zhotovené vypalováním keramických směsí, jejichž hlavními složkami jsou kaolíny, jíly a hlíny. Keramické směsi získají po prohnětení s vodou plastické vlastnosti, v tom stavu je lze tvarovat a naopak po vypálení při teplotě 800 až 1500 °C plastické vlastnosti ztrácejí a mění se v trvale tvrdou látku zvanou střep.
Nejvíce ceněnou keramickou hmotou je porcelán, jehož vstupní suroviny tvoří směs, která obsahuje průměrně 50 % nejčistšího kaolínu, 25 % křemenného písku a 25 % živce. Velmi známý a ceněný je například míšeňský porcelán, v Česku se výroba porcelánu koncentruje v západních Čechách, světově proslulý je karlovarský porcelán.
Cihlářské hlíny jako méně hodnotné keramické suroviny slouží pro výrobu cihel, střešních tašek a jiných stavebních materiálů. Z jílů nebo méně hodnotného kaolinu, živce a křemene se vypalováním při teplotě okolo 1300 °C vyrábí buď obyčejná kamenina (potrubí, dlaždice) nebo jemná bílá kamenina (talíře, umyvadla, kachlíky, sošky).
Další uplatnění ve stavebnictví nachází křemenný písek jako složka malty a pojivých materiálů a především při výrobě betonu.
Halogenidy křemíku
Křemík tvoří sloučeniny s fluorem SiF4, chlorem SiCl4 a bromem SiBr4, které se mohou dále řetězit za vzniku vyšších halogenidů. Všechny uvedené sloučeniny jsou značně nestálé a při styku s vodou okamžitě hydrolyzují za vzniku gelovité kyseliny křemičité.
Chlorid křemičitý je značně důležitou sloučeninou při přípravě čistého křemíku pro polovodičové účely (viz výše).
Těkavosti fluoridu křemičitého se v analytické chemii používá k odstranění fluoru z jeho stabilních fluoridů AlF3 a fluoridů lantanoidů. Vzorek se přitom vaří při asi 150 °C v 50 % kyselině sírové ve skleněné aparatuře a vzniklý těkavý SiF4 je okamžitě odváděn proudem horké vodní páry do roztoku alkalického hydroxidu, kde je pak možno snáze určit jeho obsah.
Karbid křemíku
Krystaly karbidu křemíku SiC mají analogickou krystalickou strukturu jako diamant a patří mezi jedny z nejtvrdších známých látek. V Mohsově stupnici tvrdosti dosahuje karbid stupně 9 – 10 a nalézá uplatnění jako brusný materiál pod názvem karborundum.
Křemíkaté analogie uhlovodíků
Protože křemík a uhlík se v periodické soustavě prvků nalézají v jedné skupině pod sebou, dalo by se usuzovat, že křemík bude stejně jako uhlík vytvářet nesmírně pestrou škálu sloučenin analogických organickým látkám. Ve starší vědeckofantastické literatuře jsme se mohli poměrně často setkat s živými bytostmi, které na rozdíl od nás mají tělo složené ze silikonových molekul, koupou se v kapalném čpavku, dýchají sirné páry apod. Skutečnost je však daleko prozaičtější.
Přestože křemík vytváří řadu analogických sloučenin k uhlovodíkům, nemůže jejich množství nikdy dosáhnout pestrosti organických látek. Důvodem je především fakt, že atomy křemíku nejsou schopny vytvářet dvojnou vazbu Si=Si a pochopitelně ani vazbu trojnou. Další významný důvod je síla vazby mezi dvěma atomy křemíku, která je přibližně poloviční, než u vazby C-C. V důsledku toho jsou molekuly o vysokém počtu vazeb Si-Si nestálé a velmi snadno se rozkládají. Přesto však existují skupiny látek, které jsou analogy mezi organickými sloučeninami a podobnými sloučeninami křemíku.
Silany
Silany jsou bezbarvé látky o složení SinH2n+2. První dva silany jsou plynné, od trisilanu Si3H8 kapalné. Všechny jsou mimořádně reaktivní a na vzduchu samozápalné, reakcí s kyslíkem vzniká oxid křemičitý a voda. Ve vodě také rychle hydrolyzují za uvolnění plynného vodíku a gelu kyseliny křemičité.
Silany jsou velmi silná redukční činidla. S halogeny reagují explozivně, za jistých podmínek (přítomnost AlCl3 a vhodné teploty) lze připravit molekuly s jedním atomem halogenu SiH3Cl až SiHCl3 apod.
Silany se uplatňují především jako výchozí sloučeniny pro výrobu složitějších křemíkatých látek např. pro výrobu čistého polovodičového křemíku.
Siloxany (silikony)
Siloxany jsou sloučeniny, které obsahují v molekule vazbu Si-O-Si. Tato chemická skupina je velmi stabilní a může proto být připraven teoreticky neomezený řetězec o složení –(O-Si-O-Si-O)-, zbylé dvě volné vazby křemíkového atomu mohou být obsazeny např. skupinami –HO nebo nejčastěji organickými ligandy jako -CH3 a dalšími. Nejběžněji užívané sloučeniny tohoto typu jsou polydimethylsiloxany a mají vzorec: (CH3)3SiO[SiO(CH3)2]nSi(CH3)3.
Uvedené látky jsou přitom za běžných podmínek zcela stabilní a nepodléhají rozkladu ani v přítomnosti kyslíku nebo vody. Podle počtu siloxanových skupin i jejich ligandů mohou být výslednými produkty jak kapalné, tak pevné látky. Jejich další vlastností je hydrofobie (odpuzují vodu) a prakticky naprostá neškodnost pro živé organizmy.
Praktické využití siloxanů je velmi široké:
- Ve stavebnictví jsou využívány především hydrofobní vlastnosti. Jsou složkou speciálních omítek a nátěrů, které zabraňují pronikání vlhkosti do staveb.
- Pevné polymerní sloučeniny na bázi siloxanů jsou většinou označovány jako silikonový kaučuk. Tato látka má elastické vlastnosti podobné klasickému kaučuku, navíc však snáší mnohem vyšší teploty a je téměř nehořlavá. Vzhledem k těmto vlastnostem se ze silikonového kaučuku vyrábějí různá těsnění nebo vystýlky nádob pro chemický průmysl a podobné aplikace.
- Hydrofobní vlastnosti siloxanů lze potlačit tím, že na určité procento křemíkových atomů jsou navázány skupiny –OH. Takové polymery se pak uplatňují v medicíně pro výrobu chirurgických implantátů (nejznámější je pravděpodobně umělé zvětšování velikosti ženských prsů).
- Kapalné nebo polotuhé siloxany jsou známy jako silikonové oleje, popř. silikonové tuky. Jejich předností oproti klasickým mazadlům je odolnost proti vysokým teplotám a jsou proto nasazovány do prostředí se zvýšeným teplotním namáháním nejen jako mazadla, ale i jako média pro přenos tepla (olejové lázně).
Zdravotní rizika
Křemík ani jeho běžné anorganické sloučeniny nejsou toxické, jsou natolik inertní, že projdou trávicím traktem zcela neporušeny. Problémy nastávají spíše při dlouhodobém vdechování mikroskopických částeček, vznikajících při broušení za použití silikátových materiálů nebo při mechanickém opracovávání silikátových výrobků. Vzniká tak choroba silikóza, která se projevuje snížením plicní kapacity a dušností.
Přísná bezpečnostní opatření ovšem musí být dodržována při průmyslové výrobě a zpracování silanů a jejich chlorovaných derivátů. Jejich reakce s kyslíkem nebo vlhkostí může způsobit explozi, únik toxického a žíravého chlorovodíku a jiných nebezpečných sloučenin.
Odkazy
Reference
- Emilie Musilová, Hana Cídlová: Chemické názvosloví anorganických sloučenin, 1.2.1 Vznik názvů prvků, Pedagogická fakulta Masarykovy univerzity, 2009
- Jiří Rejzek: Český etymologický slovník, hesla křemen, křemík
Literatura
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood – A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu křemík na Wikimedia Commons
Obrázky, zvuky či videa k tématu křemík na Wikimedia Commons  Galerie křemík na Wikimedia Commons
Galerie křemík na Wikimedia Commons Slovníkové heslo křemík ve Wikislovníku
Slovníkové heslo křemík ve Wikislovníku- (česky) Chemický vzdělávací portál
- (anglicky) Mineral.Galleries.com – Silicon