Alkalické kovy
Alkalické kovy jsou členy 1. skupiny periodické tabulky. Mezi alkalické kovy patří lithium, sodík, draslík, rubidium, cesium a francium. Tyto prvky jsou velmi reaktivní a v přírodě se nacházejí pouze ve sloučeninách. Musí být skladovány pod vrstvou nereaktivní, bezvodé kapaliny (např. petroleje).
| Alkalické kovy ≻ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC skupina | 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS skupina | I. A | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Typická elektronová konfigurace | ns1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Počet valenčních elektronů | 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vlastnosti

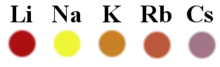
Alkalické kovy jsou měkké, lehké a stříbrolesklé kovy (cesium je nazlátlé), které lze krájet nožem. V Mohsově stupnici tvrdosti mají hodnoty menší než 1 (jsou tedy měkčí než mastek). Nejtvrdší ze všech alkalických kovů je lithium. Všechny dobře vedou elektrický proud i teplo, lithium, sodík a draslík jsou lehčí než voda a plovou na ní, ale rubidium, cesium a francium jsou těžší a klesají tedy ke dnu. V parách alkalických kovů se kromě jednoatomových částic můžeme setkat i s dvouatomovými molekulami, které mají barvu. V kapalném amoniaku se rozpouští za vzniku temně modrého roztoku. Kationty alkalických kovů barví plamen různými barvami (Li – karmínová/červená; Na – světlá oranžová/žlutá; K – fialová). Elementární kovy lze dlouhodobě uchovávat pod vrstvou alifatických uhlovodíků jako petrolej nebo nafta, s nimiž nereaguje.
Alkalické kovy mají také velmi nízkou teplotu tání, u lithia je asi 180 °C, u ostatních dokonce pod 100 °C:
| Kov | Teplota tání [°C] |
|---|---|
| Lithium | 180,54 |
| Sodík | 97,72 |
| Draslík | 63,38 |
| Rubidium | 39,31 |
| Cesium | 28,44 |
| Francium | 27 |
Reaktivita
Alkalické kovy jsou velmi reaktivní. Mají nejnižší ionizační potenciál v příslušné periodě, ale hodnota jejich druhého ionizačního potenciálu je velmi vysoká. Ve valenční slupce elektronového obalu mají jeden elektron, takže snadno tvoří kationty s jedním kladným nábojem. Reaktivita alkalických kovů stoupá s protonovým číslem prvku – lithium je nejméně reaktivní a francium je nejreaktivnější. Reagují přímo s halogeny za vzniku iontových solí a s vodou za vzniku silných hydroxidů.
Alkalické kovy jsou známé bouřlivou reakcí s vodou, tato reaktivita se zvyšuje se stoupajícím protonovým číslem prvku. Při reakci vzniká hydroxid, uvolňuje se plynný vodík a velké množství tepla.
- 2 K + 2 H2O → 2 KOH + H2
V kapalném amoniaku se alkalické kovy rozpouštějí za vzniku tmavě modrých, paramagnetických roztoků.
- K + NH3 → K+ + e−
Vzniklé solvatované elektrony jsou velmi dobrým redukčním činidlem.
Kromě těchto dvou základních reakcí reagují alkalické kovy také s kyslíkem za vzniku oxidů, peroxidů nebo hyperoxidů, za mírného zahřátí s vodíkem a dusíkem. I když je lithium nejméně reaktivní, tak jako jediné reaguje s dusíkem za normální teploty a při zahřátí také dokonce s uhlíkem a křemíkem.
Výskyt v přírodě
Díky vysoké reaktivitě se alkalické kovy volně v přírodě nevyskytují. Velmi hojně se však vyskytují ve formě svých sloučenin. Sodík a draslík dokonce patří mezi deset nejhojněji se vyskytujících prvků na zemi. Velké množství alkalických kovů se nachází v mořské vodě, v podobě svých iontových sloučenin – solí (nejvíce je zastoupena sůl NaCl neboli chlorid sodný a sylvín KCl neboli chlorid draselný). Odtud se také získávají. Tyto rozpuštěné minerály se také nacházejí v oblastech, kde dříve bylo moře, ale při vrásnění se postupně moře vysušilo a minerály zkrystalizovaly. Proto se zejména ve střední Evropě (v okolí Salcburku) vyskytují velká podzemní naleziště kamenné soli. V poměrně velkém množství se také vyskytují ledky, zejména na chilském pobřeží, které vznikly mineralizací rostlinných zbytků.
Získávání a výroba
Všechny alkalické kovy se získávají především z mořské vody. Pouze lithium se ve větším množství získává ze svých minerálů. U ostatních alkalických kovů se nejdříve odpaří mořská voda a nechají se zkrystalizovat minerály rozpuštěné ve vodě. Jednotlivé sloučeniny alkalických kovů se od sebe odseparují a poté se získávají elektrolýzou jejich taveniny nebo se rovnou elektrolyzují a jednotlivé kovy se odseparují na základě různých teplot tání a varu.
Využití
Alkalické kovy se dají použít především jako dobrá redukovadla v organické chemii nebo analytické chemii, ale vzhledem k jejich vysoké reaktivitě se na tyto reakce ve velkém nepoužívají. Z čistých kovů má největší využití lithium, které je nejstálejší na vzduchu a nejméně reaktivní. U ostatních alkalických kovů jsou významné především jejich sloučeniny.
Odkazy
Literatura
- Jursík F.: Anorganická chemie kovů. 1. vyd. 2002. ISBN 80-7080-504-8 (elektronická verze)
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood – A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9