Chlorid draselný
Chlorid draselný (KCl) je v čistém stavu bílá krystalická látka slané chuti, při vyšších koncentracích nahořklá, dobře rozpustná ve vodě. V přírodě se vyskytuje jako minerál sylvín a v carnallitu jako součást podvojné soli. Je nehořlavý a bez zápachu.
.jpg.webp)
| Chlorid draselný | |
|---|---|

Krystalický chlorid draselný | |
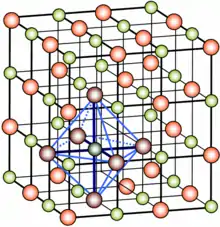
Struktura chloridu draselného | |

Krystalická forma | |
| Obecné | |
| Systematický název | Chlorid draselný |
| Triviální název | Sylvín |
| Ostatní názvy | Drasloš, Draselná sůl |
| Anglický název | Potassium chloride |
| Německý název | Kaliumchlorid |
| Sumární vzorec | KCl |
| Vzhled | bílé krystalky nebo prášek |
| Identifikace | |
| Registrační číslo CAS | 7447-40-7 |
| Vlastnosti | |
| Molární hmotnost | 74,551 g/mol |
| Teplota tání | 770,3 °C |
| Teplota varu | 1 411 °C |
| Hustota | 1,989 1 g/cm3 (20 °C) 1,984 g/cm3 (30 °C) |
| Dynamický viskozitní koeficient | 1,15 cP (787 °C) 0,92 cP (857 °C) 0,81 cP (927 °C) |
| Rozpustnost ve vodě | 28,14 g/100 g (0 °C) 31,2 g/100 g (10 °C) 34,19 g/100 g (20 °C) 36 g/100 g (25 °C) 37,4 g/100 g (30 °C) 40,3 g/100 g (40 °C) 43,05 g/100 g (50 °C) 45,88 g/100 g (60 °C) 51,25 g/100 g (80 °C) 56,2 g/100 g (100 °C) |
| Rozpustnost v polárních rozpouštědlech |
Methanol 0,54 g/100 g Ethanol 0,03 g/100 g Glycerol 6,7 g/100 g Aceton 0,000 091 g/100 g |
| Relativní permitivita εr | 5,03 (20 °C) |
| Měrná magnetická susceptibilita | −6,04×10−6 cm3g−1 |
| Povrchové napětí | 100,3 mN/m (780 °C) 95 mN/m (850 °C) 85,7 mN/m (970 °C) |
| Struktura | |
| Krystalová struktura | krychlová |
| Hrana krystalové mřížky | a=627,7 pm |
| Dipólový moment | 34,25×10−30 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −435,9 kJ/mol |
| Entalpie tání ΔHt | 345,6 J/g |
| Entalpie varu ΔHv | 9 250 J/g |
| Entalpie rozpouštění ΔHrozp | 246,8 J/g (18 °C) 230,9 J/g (25 °C) |
| Standardní molární entropie S° | 82,56 J K−1 mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −408 kJ/mol |
| Izobarické měrné teplo cp | 0,668 JK−1g−1 |
| Bezpečnost | |
| R-věty | Žádné nebezpečí |
| S-věty | Žádné nebezpečí |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Užití
K výrobě draselných hnojiv, elektrolýzou taveniny chloridu draselného se vyrábí elementární draslík.
Monokrystal KCl se používá jako detektor radioaktivity, působením ionizujícího záření se zbarvuje fialově. Sytost zbarvení je úměrná celkové absorbované energii (dávce) záření. Použito např. v krystalovém dozimetru ČSLA DK-62.
Dále se využívá jako poslední látka zastavující srdce při popravách smrtící injekcí v USA.[1]
Potravinářské použití
Používá se jako náhražka kuchyňské soli, která nezvyšuje krevní tlak, avšak při jeho používání byly zaznamenány stížnosti na hořkost nebo kovovou chuť.[2] Jako přídatná látka v potravinářství nese označení E508. Kvůli své slabé a hořké chuti je často míchán s obyčejnou kuchyňskou solí (chloridem sodným). Tím vznikne nízkosodíková sůl s lepší chutí. Přidání 1 ppm thaumatinu značně snižuje hořkost.[3]
Výroba
Nejsnadnějším způsobem výroby je neutralizace roztoku hydroxidu draselného kyselinou chlorovodíkovou podle rovnice:
Reference
- Lethal injections lead doctors to break medical oath|Amnesty International. www.amnesty.org [online]. [cit. 2010-08-06]. Dostupné v archivu pořízeném dne 2012-10-05.
- SINOPOLI, Dominique A.; LAWLESS, Harry T. Taste Properties of Potassium Chloride Alone and in Mixtures with Sodium Chloride Using a Check-All-That-Apply Method. Journal of Food Science. 2012, s. S319–22. DOI 10.1111/j.1750-3841.2012.02862.x. PMID 22901084. (anglicky)
- Lorient, Denis; LINDEN, G. New ingredients in food processing: biochemistry and agriculture. Boca Raton: CRC Press, 1999. Dostupné online. ISBN 978-1-85573-443-2. S. 357. (anglicky)
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid draselný na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid draselný na Wikimedia Commons