Chlorid zinočnatý
Chlorid zinočnatý (ZnCl2) je anorganická zlúčenina chlóru a zinku. Existuje v deviatich známych kryštálových formách. Ide o bezfarebnú alebo bielu látku dobre rozpustnú vo vode. Chlorid zinočnatý je hygroskopický a navlhavý, preto musí byť chránený pred vlhkosťou, vrátane vodných pár vo vzduchu. Používa sa v širokej škále aplikácií pri spracovaní textilu, ako tavidlo a v chemickej syntéze.
| Chlorid zinočnatý | |||||||||||||||||||||||||||||||||||||||
 Chlorid zinočnatý | |||||||||||||||||||||||||||||||||||||||
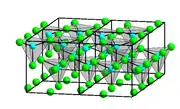 Chlorid zinočnatý | |||||||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Sumárny vzorec | ZnCl2 | ||||||||||||||||||||||||||||||||||||||
| Vzhľad | biely prášok alebo kryštáliky | ||||||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 136,3 u | ||||||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 136,32 g/mol | ||||||||||||||||||||||||||||||||||||||
| Teplota topenia | 293 °C | ||||||||||||||||||||||||||||||||||||||
| Teplota varu | 732 °C | ||||||||||||||||||||||||||||||||||||||
| Hustota | 2,907 g/cm³ (20 °C) 2,905 g/cm³ (25 °C) | ||||||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 342,0 g/100 ml (0 °C) 396,0 g/100 ml (20 °C) 408,0 g/100 ml (25 °C) 437,2 g/100 ml (30 °C) 453,0 g/100 ml (40 °C) 468,0 g/100 ml (50 °C) 488,8 g/100 ml (60 °C) 542,0 g/100 ml (80 °C) 613,5 g/100 ml (100 °C) v polárnych rozpúšťadlách: metanol etanol 100 g/100 ml (12,5 °C) acetón 43,5 g/100 ml (18 °C) roztok amoniaku v nepolárnych rozpúšťadlách: pyridín 2,6 g/100 ml (20 °C) | ||||||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Entropia topenia | 75,2 J/g | ||||||||||||||||||||||||||||||||||||||
| Entropia varu | 875 J/g | ||||||||||||||||||||||||||||||||||||||
| Entropia rozpúšťania | -514 J/g | ||||||||||||||||||||||||||||||||||||||
| Štandardná zlučovacia entalpia | −415,1 kJ/mol | ||||||||||||||||||||||||||||||||||||||
| Štandardná entropia | 111,5 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||||||
| Štandardná Gibbsová energia | −369,5 kJ/mol | ||||||||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 0,523 J K−1 g−1 | ||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||||||
| Číslo CAS | 7646-85-7 | ||||||||||||||||||||||||||||||||||||||
| Číslo UN | 2331 | ||||||||||||||||||||||||||||||||||||||
| EINECS číslo | 231-592-0 | ||||||||||||||||||||||||||||||||||||||
| Číslo RTECS | ZH1400000 | ||||||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||||||
Nie je známy žiadny minerál s týmto chemickým zložením, existuje však veľmi vzácny minerál simonkolleit so vzorcom Zn5(OH)8Cl2•H2O.
Bezpečnosť
Chlorid zinočnatý dráždi kožu a dýchaciu sústavu.[1] Bezpečnostné opatrenia, ktoré sa vzťahujú k bezvodému chloridu zinočnatého, platia aj pre iné bezvodé halogenidy kovov, t. j. ich hydrolýza môže byť exotermická a treba sa vystríhať kontaktu s týmito látkami. Koncentrované roztoky sú kyslé a žieravé, ako Lewisova kyselina poškodzujú celulózu a hodváb.
Podobné zlúčeniny
- Bromid zinočnatý
- Flurid zinočnatý
- Jodid zinočnatý
- Chlorid kademnatý
- Chlorid ortutnatý
Literatúra
- Norman Neil Greenwood, Alan Earnshaw, Chemistry of the Elements, 2nd ed., Butterworth-Heinemann, Oxford, UK, 1997. ISBN 0-7506-3365-4
- David R. Lide, Handbook of Chemistry and Physics, 71st edition, CRC Press, Ann Arbor, Michigan, 1990. ISBN 0-8493-0471-7
- The Merck Index, 7th edition, Merck & Co, Rahway, New Jersey, USA, 1960.
- D. Nicholls, Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.
- Jerry March, Advanced Organic Chemistry, 4th ed., p. 723, Wiley, New York, 1992. ISBN 0-471-60180-2
- G. J. McGarvey, in Handbook of Reagents for Organic Synthesis, Volume 1: Reagents, Auxiliaries and Catalysts for C-C Bond Formation, (R. M. Coates, S. E. Denmark, eds.), pp. 220–3, Wiley, New York, 1999.
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabuľky. 1. vyd. Praha : Grada Publishing, 1999. ISBN 80-7169-855-5.
Externé odkazy
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Chlorid zinečnatý na českej Wikipédii.






