Cyklookta-1,5-dien
Cyklookta-1,5-dien je osmiuhlíkatý cykloalkadien (cyklický uhlovodík obsahující dvě dvojné vazby).
| Cyklookta-1,5-dien | |
|---|---|
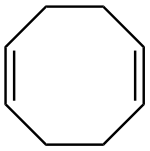
Strukturní vzorec | |
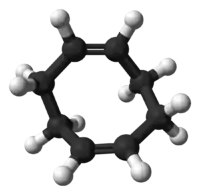
Model molekuly | |
| Obecné | |
| Systematický název | cyklookta-1,5-dien |
| Ostatní názvy | 1,5-COD, COD |
| Sumární vzorec | C8H12 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 111-78-4 |
| EC-no (EINECS/ELINCS/NLP) | 203-907-1 |
| PubChem | 82916 |
| SMILES | C1CC=CCCC=C1 |
| InChI | 1S/C8H12/c1-2-4-6-8-7-5-3-1/h1-2,7-8H,3-6H2/b2-1-,8-7- |
| Vlastnosti | |
| Molární hmotnost | 108,18 g/mol |
| Teplota tání | −56,4 °C (216,8 K)[1] |
| Teplota varu | 150,8 °C (424,0 K)[1] |
| Hustota | 0,8818 g/cm3[1] |
| Rozpustnost ve vodě | nerozpustný[1] |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v benzenu a tetrachlormethanu[1] |
| Tlak páry | 0,66 kPa[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H226 H302 H304 H332 H411 H413[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P261 P264 P270 P271 P272 P273 P280 P301+310 P301+312 P303+361+353 P304+312 P304+340 P312 P330 P331 P370+378 P391 P403+235 P405 P501[1] |
| Teplota vzplanutí | 35 °C (308 K)[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Má celkem tři stereoizomery, lišící se uspořádáním čtveřice jednoduchých vazeb C–C nacházejících se vedle dvojných vazeb. Tyto dvojice se mohou nacházet buď na stejných (cis,Z) nebo na opačných (trans, E) stranách vzhledem k rovině dvojné vazby; tři možná uspořádání se označují cis,cis, trans,trans a cis,trans, jinak také (Z,Z), (E,E) a (Z,E). (Vzhledem k souměrnosti je trans,cis stejná konfigurace jako cis,trans.)
Cis,cis izomer, obvykle uváděný pod zkratkou COD se používá na přípravu dalších organických sloučenin a je užitečným ligandem v organokovové chemii.[2][3] Lze jej připravit dimerizací buta-1,3-dienu za přítomnosti niklového katalyzátoru, vedlejším produktem je 4-vinylcyklohexen.
Organické reakce
COD reaguje s boranem za vzniku 9-borabicyklo[3.3.1]nonanu[4] (9-BBN), používaného při hydroboračně-oxidačních reakcích:
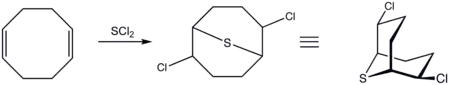
COD také reaguje s chloridem sirnatým (SCl2) (a jinými podobnými sloučeninami), produktem je 2,6-dichlor-9-thiabicyklo[3.3.1]nonan:[5][6]
Vzniklý dichlorid lze dále převést například na diazidové či dinitrilové deriváty pomocí nukleofilní substituce.
Komplexy s kovy
- Některé
2.png.webp) Bis(cyklooktadien)nikl
Bis(cyklooktadien)nikl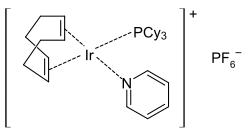
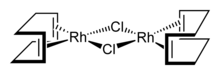 Komplex Rh2(COD)2Cl2
Komplex Rh2(COD)2Cl2(C8H13).png.webp) Co(1,5-cyklooktadien)(cyklooktenyl)
Co(1,5-cyklooktadien)(cyklooktenyl).png.webp) Dichloro(1,5‐cyklooktadien)palladium
Dichloro(1,5‐cyklooktadien)palladium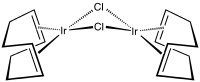
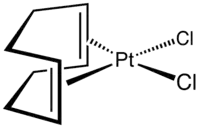 Dichloro(1,5-cyklooktadien)platina
Dichloro(1,5-cyklooktadien)platina
1,5-COD se přes alkenové skupiny váže na kovy v nižších oxidačních číslech. Vzniklé komplexy jsou zajímavé, protože jsou dostatečně stabilní, aby mohly být izolovány, často i stabilnější než odpovídající komplexy ethenu. Stabilitu COD komplexů způsobuje chelatační efekt. COD ligandy lze snadno nahradit jinými, například fosfinovými.
Ni(COD)2 se dá připravit redukcí bezvodého acetylacetonátu nikelnatého za přítomnosti ligandu, redukčním činidlem je triethylhliník[7]
- [Ni(C5H7O2)2]3 + 6 COD + 6 Al(C2H5)3 → 3 Ni(COD)2 + 6 Al(C2H5)2(C5H7O2) + 3 C2H4 + 3 C2H6
Podobný komplex Pt(COD)2 se připravuje jiným postupem, z dilithiumcyklooktatetraenu[8]
- Li2C8H8 + PtCl2(COD) + 3 C7H10 → [Pt(C7H10)3] + 2 LiCl + C8H8 + C8H12
- Pt(C7H10)3 + 2 COD → Pt(COD)2 + 3 C7H10
Byla vydána řada prací zabývajících se COD. Komplex s platinou je prekurzorem 16elektronového komplexu ethenu:
- Pt(COD)2 + 3 C2H4 → Pt(C2H4)3 + 2 COD
Komplexy cyklooktadienu jsou dobrými výchozími materiály při přípravě dalších sloučenin, příkladem může být tato reakce:
- Ni(COD)2 + 4 CO → Ni(CO)4 + 2 COD
Vzniklý Ni(CO)4 je vysoce toxický, takže je výhodné jej připravovat přímo v reakční nádobě těsně před použitím. Dalšími komplexy COD jsou například dimer cyklooktadienrhodiumchloridu, dimer cyklooktadieniridiumchloridu, Fe(COD)(CO)3 a Crabtreeův katalyzátor.
Komplexy M(COD)2, kde M = nikl, palladium nebo platina, mají tetraedrické molekulové geometrie, zatímco [M(COD)2]+ komplexy rhodia a irida jsou rovinné čtvercové.
(E,E)-COD
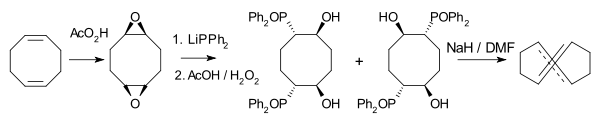
Trans,trans izomer 1,5-cyklooktadienu, (E,E)-COD, se vyznačuje velkým úhlovým napětím; poprvé jej připravili George M. Whitesides a Arthur C. Cope v roce 1969 fotoizomerizací cis,cis izomeru.[9]
Další syntézu (dvojitou eliminací z cyklooktanu) popsal Rolf Huisgen v roce 1987.[10]
Konformace (E,E)-COD není židličková, ale překřížená.[11]
Reference
V tomto článku byl použit překlad textu z článku 1,5-Cyclooctadiene na anglické Wikipedii.
- https://pubchem.ncbi.nlm.nih.gov/compound/82916
- BUEHLER, C.; PEARSON, D. Survey of Organic Syntheses. New York: Wiley-Interscience, 1970. Dostupné online. (anglicky)
- SHRIVER, D.; ATKINS, P. Inorganic Chemistry. New York: W. H. Freeman and Co., 1999. Dostupné online. (anglicky) ISBN 978-0-716-72873-3.
- SODERQUIST, John A.; NEGRON, Alvin. 9-Borabicyclo[3.3.1]nonane Dimer. Org. Synth.. 1998. Dostupné online. (anglicky); Coll. Vol.. S. 95. (anglicky)
- BISHOP, Roger. 9-Thiabicyclo[3.3.1]nonane-2,6-dione. Org. Synth.. Dostupné online. (anglicky); Coll. Vol.. S. 692. (anglicky)
- DÍAZ, David; CONVERSO, Antonella; SHARPLESS, K. Barry; FINN, M. G. 2,6-Dichloro-9-thiabicyclo[3.3.1]nonane: Multigram Display of Azide and Cyanide Components on a Versatile Scaffold. Molecules. 2006, s. 212–218. Dostupné online. DOI 10.3390/11040212. PMID 17962753. (anglicky)
- SCHUNN, R.; ITTEL, S. Bis(1,5-cyclooctadiene)nickel(0). [s.l.]: [s.n.], 1990. ISBN 978-0-470-13259-3. DOI 10.1002/9780470132593.ch25. S. 94–98. (anglicky)
- CRASCALL, L; SPENCER, J. Olefin Complexes of Platinum. [s.l.]: [s.n.], 1990. ISBN 978-0-470-13259-3. DOI 10.1002/9780470132593.ch34. S. 126–132. (anglicky)
- George M. Whitesides; Gerald L. Goe; Arthur C. Cope. Irradiation of cis,cis-1,5-cyclooctadiene in the presence of copper(I) chloride. Journal of the American Chemical Society. 1969, s. 2608–2616. DOI 10.1021/ja01038a036.
- Dieter Boeckh; Rolf Huisgen; Heinrich Noeth. Preparation and conformation of (E,E)-1,5-cyclooctadiene. Journal of the American Chemical Society. 1987, s. 1248–1249. DOI 10.1021/ja00238a046.
- Henning Stöckmann; André A. Neves; Henry A. Day; Shaun Stairs; Kevin M. Brindle; Finian J. Leeper. E,E)-1,5-Cyclooctadiene: a small and fast click-chemistry multitalent. Chemical Communications. 2011, s. 7203–7205. DOI 10.1039/C1CC12161H. PMID 21611648.