Trimethylfosfit
Trimethylfosfit je organická sloučenina se vzorcem (CH3O)3P. Používá se jako ligand v koordinační chemii a jako reaktant v organické syntéze. Molekula má pyramidální tvar s centrem tvořeným trojmocným fosforem.
| Trimethylfosfit | |
|---|---|
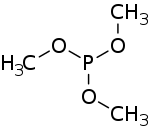
Strukturní vzorec | |
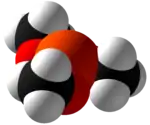
Model molekuly | |
| Obecné | |
| Systematický název | trimethyl-fosfit |
| Ostatní názvy | trimethoxyfosfan |
| Funkční vzorec | (CH3O)3P |
| Sumární vzorec | C3H9OP |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 121-45-9 |
| EC-no (EINECS/ELINCS/NLP) | 204-471-5 |
| PubChem | 8472 |
| SMILES | O(P(OC)OC)C |
| InChI | 1S/C3H9O3P/c1-4-7(5-2)6-3/h1-3H3 |
| Číslo RTECS | TH1400000 |
| Vlastnosti | |
| Molární hmotnost | 92,077 g/mol |
| Teplota tání | −78 °C (195 K)[1] |
| Teplota varu | 111,5 °C (384,6 K)[1] |
| Hustota | 1,0518 g/cm3 (20 °C)[1] |
| Index lomu | 1,4095 (20 °C)[1] |
| Rozpustnost ve vodě | reaguje[1] |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v ethanolu a acetonu[1] |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v diethyletheru, benzenu, hexanu a tetrachlormethanu |
| Tlak páry | 3,228 kPa[1] |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H226 H302 H312 H315 H318 H319 H332 H335 H361[1] |
| P-věty | P201 P202 P210 P233 P240 P241 P242 P243 P261 P264 P271 P280 P281 P301+312 P302+352 P303+361+353 P304+312 P304+340 P305+351+338 P308+313 P310 P312 P321 P322 P330 P332+313 P337+313 P362 P363 P370+378 P403+233 P403+235 P405 P501[1] |
| Teplota vzplanutí | 28 °C (301 K)[1] |
| Teplota vznícení | 250 °C (523 K)[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava a reakce
Trimethylfosfit se připravuje z chloridu fosforitého:
- PCl3 + 3 CH3OH → P(OCH3)3 + 3 HCl
Lze jej oxidovat na trimethylfosfát.
Reaguje s katalytickými množstvími jodmethanu v Michaelisově–Arbuzovově reakci za tvorby dimethylmethylfosfonátu:
- P(OCH3)3 → CH3P(O)(OCH3)2
Jako ligand má menší Tolmanův úhel a je lepším akceptorem než trimethylfosfin. Příkladem trimethylfosfitového komplexu je Ni(P(O[CH3])3)4 (s teplotou tání 108 °C).[2] Z trimethylfosfitu se připravuje tridentátní ligand nazývaný Kläuiův ligand. Tvorba tohoto ligandu dokládá schopnost trimethylfosfitu účastnit se Michaelisových–Arbuzovových reakcí.
Trimethylfosfit lze také použít jako desulfurizační činidlo, například na přípravu derivátů tetrathiafulvalenu.[3]
Reference
V tomto článku byl použit překlad textu z článku Trimethyl phosphite na anglické Wikipedii.
- Trimethyl phosphite. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- Steven D. Ittel; M. A. Cushing. Complexes of Nickel(0). Inorganic Syntheses. 1990, s. 98–104. ISBN 978-0-471-52619-3.
- Jan Larsen; Christine Lenoir. 2,2'-Bi-5,6-Dihydro-1,3-Dithiolo[4,5-b][1,4]dithiinylidene (BEDT-TTF). Organic Syntheses. 1995, s. 265.



