Metabolismus fenylpropanoidů
Metabolismu fenylpropanoidů se účastní mnoho enzymů.
Přeměna aminokyselin na skořicové kyseliny
V rostlinách vznikají všechny fenylpropanoidy z aminokyselin fenylalaninu a tyrosinu.
Fenylalanin-amoniaklyáza (také se používá název fenylalanin/tyrosin-amoniaklyáza) přeměňuje L-fenylalanin na kyselinu trans-skořicovou a tyrosin na kyselinu p-kumarovou
Cinamát-4-hydroxyláza mění trans-cinamát na 4-hydroxycinamát (kyselinu p-kumarovou). 4-kumarát-CoA ligáza zprostředkovává převod 4-hydroxycinamátu na 4-kumaroylkoenzym A.[1]
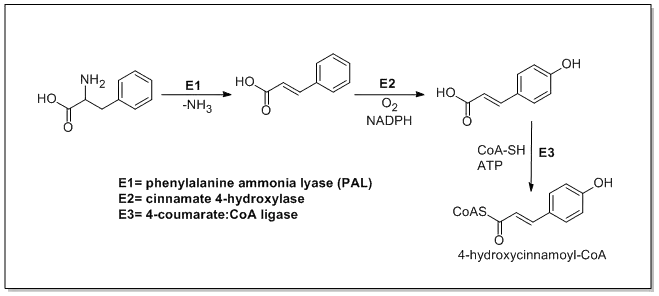
Enzymy zapojené do syntézy hydroxyskořicových kyselin
- Cinamylalkoholdehydrogenáza (CAD), enzym převádějící cinamylalkohol na cinamaldehyd
- Sinapinesteráza, přeměňuje sinapoylcholin na sinapát (kyselinu sinapovou) a cholin
- Trans-cinnamát-2-monooxygenáza, mění trans-cinnamát (kyselinu skořicovou) na 2-hydroxycinnamát
- Kafeát-O-methyltransferáza, mění kyselinu kávovou na kyselinu ferulová
- Kafeoyl-CoA-O-methyltransferáza, zprostředkovává přeměnu kafeoyl-CoA na feruloyl-CoA
- 5-O-(4-kumaroyl)-D-chinát-3'-monooxygenáza, zajištuje přeměnu trans-5-O-(4-kumaroyl)-D-chinátu na trans-5-O-kafeoyl-D-chinát
- Sinapoylglukóza—cholin-O-sinapoyltransferáza, slouží k proměně 1-O-sinapoyl-beta-D-glukózy na sinapoylcholin (sinapin)
- Sinapoylglukóza—malát-O-sinapoyltransferáza, přeměňuje 1-O-sinapoyl-beta-D-glukózu na sinapoyl-(S)-malát
- Cinnamoyl-CoA-reduktáza, vytváří cinamoyl-CoA z cinnamaldehydu
Konjugační enzymy
Konjugační enzymy zajišťují konjugace fenylpropanoidů s jinými molekulami.
- 2-kumarát-O-beta-glukosyltransferáza, enzym zprostředkovávající proměnu trans-2-hydroxycinamátu na trans-beta-D-glukosyl-2-hydroxycinamát
- Hydroxycinamát-4-beta-glukosyltransferáza, provádí přeměnu kyseliny p-kumarové na 4-O-beta-D-glukosyl-4-hydroxycinamát
- Šikimát-O-hydroxycinamoyltransferáza, mění 4-kumaroyl-CoA na 4-kumaroylšikimát
- Chinát-O-hydroxycinnamoyltransferase, enzym, který zajišťuje přeměnu feruloyl-CoA v O-feruloylchinát
- Sinapát-1-glukosyltransferáza, enzym, který mění sinapát na 1-sinapoyl-D-glukózu
- Koniferylalkoholglukosyltransferáza, zajišťuje přeměnu koniferylalkoholu na koniferin
Glukosidázy
- Koniferin-betaglukosidáza, přeměňuje koniferin na koniferylalkohol
Biosyntéza stilbenoidů
- Pinosylvin syntáza, katalyzuje přeměnu pinosylvinu v cinamoyl-CoA
- Trihydroxystilbensyntáza, zajišťuje přeměnu 4-kumaroyl-CoA na resveratrol; U bakterií Photorhabdus se vyskytuje alternativní bakteriální syntéza stilbenoidů řízená ketosyntázou, přičemž vzniká 3,5-dihydroxy-4-isopropyl-trans-stilben; lze ji využít k získání antibiotik.[2]
Biosyntéza kumarinů
Biosyntéza chalkonů
4-kumaroyl-CoA se může spojit s malonyl-CoA za vzniku základní struktury flavonoidů, skupiny sloučenin nazývaných chalkonoidy, které obsahují dvě fenylová jádra. Naringenin-chalkonsyntáza katalyzuje následující přeměnu:
- 3-malonyl-CoA + 4-coumaroyl-CoA → 4 CoA + naringeninchalkon + 3 CO2
Biosyntéza flavonoidů
Konjugačním uzavíráním kruhů chalkonů se tvoří flavonoidy, sloučeniny obsahující flavonovou strukturu složenou ze tří cyklických jader.
Biodegradace
Biodegradace hydroxyskořicových kyselin
- Enzym kafeát 3,4-dioxygenáza přeměňuje 3,4-dihydroxy-trans-cinamát (kyselinu kávovou) působením kyslíku na 3-(2-karboxyethenyl)-cis,cis-mukonát.
Reference
- Filippos Ververidis; Emmanouil Trantas; Carl Douglas; Guenter Vollmer; Georg Kretzschmar; Nickolas Panopoulos. Biotechnology of flavonoids and other phenylpropanoid-derived natural products. Part I: Chemical diversity, impacts on plant biology and human health. Biotechnology Journal. 2007, s. 1214–1234. DOI 10.1002/biot.200700084. PMID 17935117.
- S. A. Joyce; A. O. Brachmann; I. Glazer; L. Lango; G. Schwär; D. J. Clarke; D. B. Bode. Bacterial biosynthesis of a multipotent stilbene. Angewandte Chemie International Edition in English. 2008, s. 1942–1945. DOI 10.1002/anie.200705148. PMID 18236486.