Organické sloučeniny rtuti
Organické sloučeniny rtuti jsou organokovové sloučeniny obsahující rtuť, obvykle vázanou přímo na atom či atomy uhlíku. Vazby Hg–C bond jsou zpravidla stálé na vzduchu i za přítomnosti vody, ale citlivé na světlo. K významným sloučeninám z této skupiny patří methylrtuťnatý (CH3Hg+) a ethylrtuťnatý kation (C2H5Hg+), dimethylrtuť, (CH3)2Hg, diethylrtuť a merbromin. Thiomersal se používá jako konzervant vakcín a nitrožilních léčiv.
Toxicita organických sloučenin rtuti[1][2] vytváří nebezpečí i výhody. Dimethylrtuť je silně toxická, ale používá se jako antimykotikum a insekticid. Merbromin a boritan fenylrtuťnatý se používají jako povrchová antiseptika, zatímco nitromersol má využití jako konzervační látka ve vakcínách a protijedech.
Příprava
Organortuťové sloučeniny se připravují několika způsoby, například přímými reakcemi uhlovodíků se rtuťnatými solemi; v tomto ohledu připomínají organické sloučeniny palladia a liší se od sloučenin kadmia.
Merkurace aromatických sloučenin
Areny bohaté na elektrony mohou být merkurovány přímo reakcemi s octanem rtuťnatým (Hg(O2CCH3)2). Jedna octanová skupina, která zůstane navázána na atomu rtuti, může být lehce odstraněna chloridem:[3]
- C6H5OH + Hg(O2CCH3)2 → C6H4(OH)–2-HgO2CCH3 + CH3CO2H
- C6H4(OH)–2–HgO2CCH3 + NaCl → C6H4(OH)–2-HgCl + NaO2CCH3
První takové reakce, mimo jiné merkuraci benzenu, provedl mezi roky 1898 a 1902 Otto Dimroth.[4][5][6]
Adice na alkeny
Rtuťnaté ionty se vážou na alkeny, například reakcí methylakrylátu s octanem rtuťnatým v methanolu vzniká α--mercuriester:[7]
- Hg(O2CCH3)2 + CH2=CHCO2CH3 → CH3OCH2CH(HgO2CCH3)CO2CH3
Vzniklé vazby Hg-C lze štěpit bromem za vzniku alkylbromidů:[8]
- CH3OCH2CH(HgO2CCH3)CO2CH3 + Br2 → CH3OCH2CHBrCO2CH3 + BrHgO2CCH3
Tento postup se označuje jako Hofmannova-Sandova reakce.
Reakce rtuťnatých sloučenin s karbanionty a jejich ekvivalenty
Nejčastějším způsobem přípravy organortuťových sloučenin je alkylace pomocí organolithných sloučenin nebo Grignardových činidel; například diethylrtuť se vytváří reakcí chloridu rtuťnatého se dvěma ekvivalenty ethylmagnesiumbromidu, rozpouštědlem bývá diethylether.[9]
Vzniklá sloučenina, se vzorcem (CH3CH2)2Hg, je kapalná a má hustotu 2,466 g/cm3. Rozpouští se v ethanolu a diethyletheru.
Difenylrtuť (vroucí při 121–123 °C) se obdobně připravuje z chloridu rtuťnatého a fenylmagnesiumbromidu. Podobný postup představuje příprava fenylsodíku za přítomnosti rtuťnatých solí.[10]
Ostatní způsoby
Rtuťnaté sloučeniny mohou být alkylovány diazoniovými solemi za přítomnosti kovové mědi. Takto byl získán například 2-chlormerkurinaftalen.[11]
Fenyl(trichlormethyl)rtuť lze získat tvorbou dichlorkarbenu a jeho reakcí s fenylchloridem rtuťnatým. Vhodným zdrojem karbenu je zde trichloroctan sodný,[12] ze kterého se dichlorkarben uvolňuje zahřátím:
- C6H5HgCCl3 → C6H5HgCl + CCl2
Reakce
Organické sloučeniny rtuti jsou častými syntetickými meziprodukty, protože lze snadno řídit podmínky, za kterých se štěpí jejich vazby Hg-C. Difenylrtuť se používá jako zdroj fenylových radikálů v několika syntézách. Její reakcí s hliníkem vzniká trifenylhliník:
- 3 Ph2Hg + 2 Al → (AlPh3)2 + 3 Hg
Organortuťové sloučeniny reagují s halogeny za tvorby odpovídajících organohalogenidů. Jsou běžnými součástmi transmetalačních reakcí lanthanoidů a kovů alkalických zemin.
Křížovými párováními organortuťových sloučenin s organohalogenidy, katalyzovanými palladiem, se vytvářejí nové vazby C-C. Tyto reakce mají obvykle nízkou selektivitu, kterou však lze zlepšit přidáním halogenidů. Karbonylace laktonů lze provést pomocí rtuťnatých sloučenin a katalyzátorů založených na palladiu.[13]
Použití
Vzhledem ke své toxicitě a nízké nukleofilitě nejsou organické sloučeniny rtuti používány často. Oxymerkuračně–demerkurační přeměny alkenů na alkoholy s pomocí octanu rtuťnatého probíhají přes organortuťové meziprodukty; obdobně je možné získat fenoly Wolffensteinovou–Bötersovou reakcí. Toxicita má využití u antiseptik, jako jsou thiomersal a merbromin, a fungicidů, například chloridu ethylrtuťnatého a octanu fenylrtuťnatého.
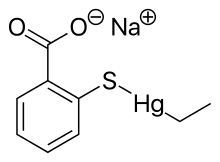
Sloučeniny jako je kyselina mersalylová, se používaly jako diuretika, ale byly nahrazeny thiazidy, které jsou bezpečnější a mají delší účinek.
Thiolová afinitní chromatografie
Thioláty (R-S−) a thioketony (R2C=S) jsou měkkými nukleofily, které vytváří silné komplexy se rtuťnatými ionty, jež jsou měkkými elektrofily.[14] Díky těmto vlastnostem mají organické sloučeniny rtuti využití v afinitní chromatografii, kde pomáhají oddlovat ze směsí sloučeniny obsahující thiolové skupiny, například organortuťový agarozový gel může sloužit k izolaci thiolovaných sloučenin, jako je thiouridin, z biologických vzorků.[15]
Odkazy
Související články
- Otrava těžkými kovy
- Otrava rtutí
- Choroba Minamata
Externí odkazy
- 1967 Evaluations of some Pesticide Residues in Food: Organomercury compounds [online]. International Programme on Chemical Safety. Dostupné online. (anglicky)
- Organomercury Compounds [online]. Mount Desert Island Biological Laboratory. Dostupné online. (anglicky)
Reference
V tomto článku byl použit překlad textu z článku Organomercury na anglické Wikipedii.
- H. Hintermann. Organomercurials. Their Formation and Pathways in the Environment. Metal Ions in Life Sciences. Cambridge: RSC publishing, 2010, s. 365–401. ISBN 978-1-84755-177-1.
- M. Aschner; N. Onishchenko; S. Ceccatelli. Toxicology of Alkylmercury Compounds. Metal Ions in Life Sciences. Cambridge: RSC publishing, 2010, s. 403–434. ISBN 978-1-84755-177-1.
- o-Chloromercuriphenol. Org. Synth.. 1941. Dostupné online. (anglicky); Coll. Vol.. S. 161. (anglicky)
- Otto Dimroth. Directe Einführung von Quecksilber in aromatische Verbindungen. Berichte der deutschen chemischen Gesellschaft. 1898, s. 2154–2156. Dostupné online. DOI 10.1002/cber.189803102162.
- Otto Dimroth. Ueber die Einwirkung von Quecksilberoxydsalzen auf aromatische Verbindungen. Berichte der deutschen chemischen Gesellschaft. 1899, s. 758–765. Dostupné online. DOI 10.1002/cber.189903201116.
- Otto Dimroth. Ueber die Mercurirung aromatischer Verbindungen. Berichte der deutschen chemischen Gesellschaft. 1902, s. 2032–2045. Dostupné online. DOI 10.1002/cber.190203502154.
- dl-Serine. Org. Synth.. 1955. Dostupné online. (anglicky); Coll. Vol.. S. 774. (anglicky)
- K. A. Hofmann; J. Sand. Ueber das Verhalten von Mercurisalzen gegen Olefine. Berichte der deutschen chemischen Gesellschaft. 1900, s. 1340–1353. Dostupné online. DOI 10.1002/cber.190003301231.
- W. A. Herrmann. Synthetic Methods of Organometallic and Inorganic Chemistry Volume 5, Copper, Silver, Gold, Zinc, Cadmium, and Mercury. [s.l.]: [s.n.], 1996. ISBN 3-13-103061-5.
- CALVERY, H. O. Diphenylmercury. Org. Synth.. 1941. Dostupné online. (anglicky); Coll. Vol.. S. 228. (anglicky)
- NESMAJANOW, A. N. β-Naphthylmercuric Chloride. Org. Synth.. 1943. Dostupné online. (anglicky); Coll. Vol.. S. 432. (anglicky)
- LOGAN, T. J. Phenyl(trichloromethyl)mercury. Org. Synth.. 1973. Dostupné online. (anglicky); Coll. Vol.. S. 969. (anglicky)
- "Reactivity control in palladium-catalyzed reactions: a personal account" Pavel Kocovsky J. Organometallic Chemistry 687 (2003) 256-268 DOI:10.1016/j.jorganchem.2003.07.008
- Jonathan Clayden; Nick Greeves; Stuart Warren. Organic Chemistry. [s.l.]: OUP Oxford, 2012-03-15. ISBN 978-0-19-927029-3. S. 658.
- =Masao Ono; Masaya Kawakami. Separation of Newly-Synthesized RNA by Organomercurial Agarose Affinity Chromatography. Journal of Biochemistry. 1977, s. 1247–1252. PMID 19428.