Oprava DNA
Oprava DNA je označení pro jakýkoliv mechanismus, který je schopen v poškozeném řetězci DNA obnovit původní pořadí nukleotidů („písmen genetického kódu“ – jednotlivých bází). Takové poškození, které může být způsobené například jednou nebo několika mutacemi. Nebo také modifikací bází, by jinak mohlo mít za následek poškození genetické informace buňky.[1] Poruchy obecně se projevujíví opravy DNA může mít někdy za následek např. rakovinné bujení. Opravy na DNA uchovávají v pořádku celý genom a nedegradovaný stav jednotlivých genů. U lidských buněk může být poškození způsobeno například vlivem radiace, či i normálními metabolickými procesy. Přes průběh jediného dne je předpokládané množství jednotlivých molekulárních lézí až 1 milión. Mnoho těchto rozkladů může mít za následek i narušení struktury molekul DNA. Porušením může nastat částečné, nebo úplné zamezení schopnosti transkripce segmentů genů ve výsledku degradující celý proces kódování sahající svým rozsahem až i po mechanismy genové exprese. Dalším vyskytujícím se nebezpečím jsou nechtěné mutace v genomu buněk (dědičné informaci), následně přenesené ne dceřiné buňky po procesu mitózy. Mechanismy opravující DNA jsou v organismu neustále aktivní, jak reagují na poškození ve struktuře DNA a náhodně se opakujícím chybám. Při selhání mechanismů opravy a nenastaní apoptózy, se mohou vyskytnout nenávratné škody. Například zlomení struktury dvoušroubovice a také vznik komplikovaných křížových vazeb mezi jednotlivými vlákny (crosslinks, ICLs), to může vést až k vytvoření rakovinných těles. Tyto šířící se chyby, následně děděné po buněčných generacích jako jeden ze základů rakovinného bujení je podstatou Knudsonovy hypotézy (two-hit hypothesis).
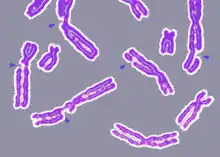
Míra proběhlých oprav DNA je závislá na mnoha faktorech, typu buňky, stáří samotné buňky, okolního prostředí obklopujícího buňku. Buňka s příliš mnoho opakujícími se narušeními DNA, nebo buňka, která v rámci vnitřních procesů není schopna efektivně aplikovat opravy vyskytnutých chyb, vstoupí do aktivního průběhu jednoho z těchto tří stavů:
- Buňka nenávratně dobrovolně vstoupí do pasivního stavu zpomalujícího vnitřní procesy, který může vést k dormanci a neomezená míra zpomalování reakcí vede k senescenci.
- Buňka aktivně vstoupí do procesu apoptózy a Programované buněčné smrti (PCD).
- Buňka zahájí integrovaný nenávratný neregulovaný proces buněčného dělení, který může vést k růstu tumoru, který je okolními buňkami považován za nebezpečí, okolní buňky neobsahující toto rozsáhlé poškození DNA nedokáží v metabolických procesech s narůstajícím tělesem komunikovat a začlenit jej. Rakovinné bujení následně u nedostatečného zásahu leukocytů gradovaně narůstá.
Průběh buněčné opravy DNA je esenciální při integrujících procesech genomu, tedy zaručuje správné fungování organismu a opakujících se metabolických reakcí. Mnoho genů, s prokázaným vlivem na délku života, ve spolupráci s některými bílkovinami, je zapojených v mechanismech opravy DNA a také její ochrany. Narušená trojrozměrná prostorová konfigurace DNA může být také faktorem tvořícím chybové úkony v průběhu translace při syntéze bílkovin.
V roce 2015 byla Tomasu Lindahlovi, Paulu Modrichovi a Azizu Sancarovi udělena Nobelova cena za chemii za poodkrytí molekulárních procesů spojených s opravou DNA: nejméně dvou konkrétních typů, a to oprava za dočasného vyjmutí na nukleotidu a oprava za dočasného vyjmutí na nukleové bázi.
Poškození DNA
K poškozením patří různé genové mutace, chromozomové aberace či dokonce genomové mutace. Výše zmíněná buněčná obměna vede k molekulárním lézím uvnitř buněk v rozsahu 10,000 až jeden milión za den. Nespravované léze u důležitých genů jako jsou tumor supresorové geny, vede k navýšenému riziku výskytu rakoviny. Většina narušení DNA ovlivňuje primární strukturu dvoušroubovice, to znamená upravení samotných bází chemickými procesy. Tyto modifikace mohou narušit obecnou šroubovitou strukturu, začleňováním cizích chemických vazeb, které nepasují do standardního modelu dvojité šroubovice. DNA obvykle na rozdíl od proteinů a RNA postrádá terciární biomolekulární strukturu a s tím spojené vlastnosti, takže se u DNA nevyskytují poškození na této úrovni. DNA má (u eukaryot) specifickou vlastnost se vinout (nadšroubovicové vinutí) a obmotávat kolem nashromážděných skupin bílkovin, nazývaných histony. U eukarytických buněk jsou tyto struktury nazývány nukleozomy, ty samotné jsou také citlivé na poruchy v DNA. Harper dělí poškození DNA následovně:[2]
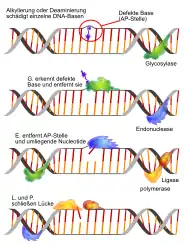
- změna jediné báze
- depurinace (purinová báze se uvolní z fosfáto-cukerné kostry)
- deaminace (adenin na hypoxantin či cytosin na uracil)
- alkylace báze
- inzerce či delece nukleotidu
- vložení analogu báze, tzn. molekuly strukturně podobné nukleové bázi schopné ji nahradit při replikaci
- změna dvou bází
- vznik thyminového dimeru vlivem absorpce UV záření
- dimerizace sousedních bází vlivem alkylačních činidel
- poruchy na úrovni celých řetězců
- poruchy vlivem ionizujícího záření
- poruchy fosfáto-cukerné složky vlivem radioaktivity
- vznik volných radikálů vlivem oxidace
- chybný vznik vazeb
- mezi dvěma bázemi na stejném řetězci nebo napříč řetězcem
- mezi DNA a okolními proteiny (histony atp.)
Zdroje poškození
Poškození na DNA lze rozdělit na 2 hlavní typy:
- Endogenní poškození jako je útok (ROS) reaktivními molekulami s kyslíkem pocházejících z obecných produktů metabolismu (spontánní mutace), především proces oxidativní deaminace (včetně chyb při replikaci).
- Exogenní poškození způsobené útoky z vnějšího okolí.

- Ultrafialové záření (UV 200 – 400 nm) radiace z Slunce.
- Ostatní typy radiace (frekvencí), včetně rentgenového záření, gama záření.
- Hydrolýza, tepelná nerovnováha
- Některé rostlinné toxiny
- Chemické látky způsobující mutace, obzvláště aromatické sloučeniny, které se dokáží vměstnat do struktury DNA a tím ji lehce poškozují.
- Účinky virusu.
Konkrétní typy narušení
Je několik typů poškození DNA vzhledem k endogenním procesům týkajících se buňky:
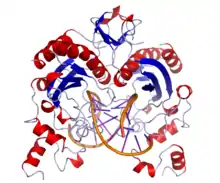
- Oxidace bází (8-oxo-7,8-dihydroguanin (8-oxoG)) a narušení generace vláken DNA přerušením reaktivními molekulami s kyslíkem.
- Alkylace bází (obvykle metylace) jako je formace 7-metylguanosine, 1-metyladenin, 6-O-Metylguanin.
- Hydrolýza bází - depyrimidinace, depurinace, deaminace.
- Tzv. "bulky adduct formation"
- Překřížení bází, vzhledem k chybám při DNA replikaci. (špatná báze DNA je sešita do nepatřičného místa v nově se formujícím vlákně DNA, nebo je přeskočena báze, chybně vložena do struktury vlákna.
- Monoaditivní poškození způsobené změnou jedné dusíkaté báze DNA.
- Diaditivní poškození.
Typy poškození exogenními vlivy:
- UV - B záření způsobuje křížové spoje mezi přilehlou bází C a T, vytváří pyrimidinový dimer, který patří do přímého poškození DNA.
- UV - A záření způsobuje zejména volné radikály, tento způsob je nazýván nepřímé poškození DNA.
- Ionizujícího záření (například i z kosmického záření) láme trojrozměrnou prostorovou konfiguraci DNA. Může ve velké míře způsobit i nenávratné škody, které již nelze opravit.
- Tepelné narušení, vlivem navýšené teploty zvyšuje míru depurinace. To může vést k přetržení vláken dvoušroubovice. U termofilních bakterií je možno sledovat hydrolitickou depurinaci. Jsou to bakterie, které rostou v horkých pramenech v teplotách 40 – 80 °C. Míra depurinace (300 purinových zbytků v genomu jedné generace) je příliš vysoká, takže nemůže být napravována běžnými mechanismy. Na to se u těchto bakterií vyvíjí adaptace odpovídající okolnímu prostředí.
- Průmyslové chemikálie s negativním vlivem na dvoušroubovici deoxyribonukleové kyseliny je vinylchlorid, nebo také peroxid vodíku ve velkém množství, způsobující alkylaci bází a neblahé křížové propojování v DNA.
Poškození UV zářením, alkylace/metylace, narušení rentgenovým zářením a oxidativní poškození jsou příklady indukované, kumulativní škody. Spontánní poškození zahrnuje ztrátu báze, deaminaci, svraštěné prstencové formace sacharidů, tautomerní posun.
Oprava DNA během replikace
Replikace DNA, tedy kopírování DNA, které musí předcházet buněčnému dělení, je choulostivý proces, při němž je vysoký potenciál vzniku chyb v genetické informaci vycházejícího vlákna (repliky). To, že je nakonec tato chybovost pouze jedna chyba na miliardu bází (1/109),[3] je zásluhou kontrolních mechanismů během replikace i po ní.
Proofreading
Přímo při replikaci by mohlo docházet k tomu, že se k sobě navážou dvě báze, které nejsou komplementární, tedy adenin k cytosinu a guanin k thyminu. Díky speciálním vlastnostem DNA polymerázy je taková chybovost pouze jedna chyba na deset milionů bází (1/107).[3]
Schopnost samotné DNA polymerázy opravovat špatně přiřazené báze se označuje jako proofreading (doslova „kontrolní čtení“). Jak tento enzym postupuje po řetězci a přidává na základě komplementarity jednotlivé nukleotidy, vždy předtím, než tento nukleotid přiřadí, zkontroluje, že navázání předchozího nukleotidu odpovídá plně zákonům komplementarity (tedy že k A je přiřazeno T, k G je přiřazeno C). Pokud je tam chyba, polymeráza je schopná opět narušit fosfodiesterovou vazbu a vložit na tomto místě nukleotid správný. Můžeme říci, že je DNA polymeráza schopná nejen 5'-3' polymerační aktivity, ale navíc praktikuje i 3'-5' exonukleotické procesy. Proofreading je zřejmě důvod, proč DNA polymeráza kopíruje DNA jen ve směru 5'-3' – jinak by nemohla provádět proofreading.[3]
U bakterií se na opravě DNA různým způsobem podílí hlavně DNA polymeráza I a DNA polymeráza II.[1]
Korekce párování bází
Po ukončení replikace dané části řetězce následuje ještě jedna korekce správného párování bází (tzv. mismatch repair), která dokáže odhalit mnoho chyb zanedbaných komplexem DNA polymerázy. Právě díky ní je výsledná chybovost pouze 1/109.[3] Příkladem chyby je například stav, kdy se naproti guaninu připojí báze adeninová, ačkoliv by tam měl být podle všech pravidel komplementarity cytosin. V tom případě je specializovaná skupina enzymů schopná rozeznat řetězec původní (templátový, ve zmíněném případě ten řetězec s guaninem) od řetězce právě dosyntetizovaného. To je zásadní, jinak by totiž nebylo jasné, jaká z bází (zda guanin nebo adenin) je bodová mutace, a jaký je výchozí stav.[3]
Oprava DNA mimo období replikace
Jednotlivé buňky nemohou správně fungovat při narušené DNA a tím pádem kompromitované integrity a dostupnosti informací genomu (i když buňky mohou být funkční i při poškození, nebo přímo postrádání genů, které nejsou esenciálně důležité). Podle typu poškození ohrožujícího dvoušrobovici DNA, se evolučně vyvinuly opravné mechanismy na rekonstrukci a obnovení ztracených informací. Pokud je to možné, buňky použijí nemodifikované komplementární vlákna DNA, nebo sousední chromatidu jako vzor k napravení škod originální informace. Bez přístupu k předloze, buňky využijí metody náchylné k chybám a to, translační syntézy jako poslední zásobu snahy o nápravu. Jakékoliv poškození DNA, narušuje originální prostorovou konfiguraci vlákna šroubovice, což buňka dokáže detekovat. Jakmile je lokalizováno poškození, konkrétní molekuly na opravu DNA se přichytí v blízkosti místa poškození. Tím napomáhají lokalizovat a přichytit se k místu dalším molekulám. Za probíhajících molekulových interakcí, dohromady vytvoří komplex, který teprve aktivně opravuje poškozené místo v určité prostorové konfiguraci.
Každá učebnice pojímá klasifikaci opravných mechanismů jinak, tento je založen na knize Biochemistry od Donalda a Judith Voetových.[4]
Přímý zvrat poškození
Do této skupiny opravných mechanismů patří například fotolyáza, enzym, jenž je schopen opravit chyby způsobené paprsky ultrafialového (UV) záření (vlnové délky 300 - 500 nm). UV záření je schopné spojit vazbou dvou sousedních thyminových bází, čímž vzniká tzv. thyminový dimer (někdy však podobná situace může vzniknout i s cytosinem). Fotolyáza se naváže ve tmě na thyminový dimer a poté ve dne absorbují její kofaktory FADH2 a pterin světlo, čímž dojde k aktivaci enzymu a k rozkladu thyminového dimeru.[4] V podstatě se tímto buňka snaží o opačný průběh události poškození, tím že jeden ze tří typů průběhu tohoto narušení chemicky obrátí. Tyto mechanismy nevyžadují předlohu, protože nastalé poškození, které se snaží zvrátit se nachází jen v jedné z bází. Takovéto opravy jsou velmi konkrétní a není u nich tedy, potřeba rozložení fosfodiesterové vazby. U lidí probíhají opravy (NER) v reakci po vystavení vlivu UV záření.
- První poškození je způsobené UV zářením (NER).
- Druhým typem je zvrat poškození způsobené metylací báze guaninu, proteinem MGMT.
- Třetím typem zvratu v buňce určitého poškození DNA, které je způsobené konkrétní metylací báze cytosinu a adeninu
Opravy jiných typů poškození DNA je schopná také 06-methyl-guanin-DNA-methyltransferáza. Tento protein je schopen opravit báze 06-methylguanin a 06-ethylguanin, které vznikají alkylací guaninu např. po jeho vystavení alkylačním činidlům, jako je MNNG.[4]
Vyštěpovací oprava
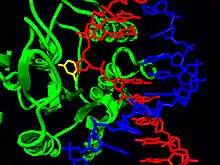
Vyštěpovací či také ekcizní typ oprav (z angl. excision repair) představuje další možnost, jak opravit poškození ultrafialovým světlem. V tomto případě je pomocí speciálních enzymů (jistých endonukleáz; konkrétně UvrABC–endonukleázou) vyštěpen z molekuly DNA oligonukleotid (jednovláknový řetězec dlouhý několik nukleotidů) obsahující pyrimidinové dimery (cytosinové či thyminové). Následně jsou (u bakterií zřejmě DNA polymerázou I) syntetizovány předtím odstraněné nukleotidy. Poruchy v těchto ekcizních mechanismech mohou vést k onemocnění xeroderma pigmentosum.[4]
Jindy se díky vyštěpování mohou v DNA opravovat chyby vzniklé např. samovolnou deaminací (adeninu na hypoxantin či cytosinu na uracil), methylací či samovolné otevření cyklických molekul nukleových bází. Tzv. DNA glykosylázy jsou ve spolupráci s AP endonukleázou a DNA polymerázami schopné tento typ chyb opravit. Příkladem je uracil-N-glykosyláza, která z DNA odstraňuje uracilové báze, které do DNA vůbec nepatří, a nahrazuje je cytosinem.[4]
Rekombinační oprava
Rekombinační (protože připomíná rekombinaci) nebo také postreplikační typ oprav spočívá v tom, že pyrimidinové dimery vzniklé účinkem UV záření, jako je dimer thyminový, působí vážné potíže při replikaci DNA. Pokud DNA polymeráza replikující genom dojde na místo, kde je např. thyminový dimer, přeruší zde polymeraci a toto místo přeskočí. Taková mezera však musí být zacelena, a to nejlépe podle vzoru v podobě druhého rodičovského vlákna, které již mezi tím bylo replikováno. U E. coli toto zajišťuje nukleáza RecA, která vystřihne odpovídající část DNA z rodičovského vlákna a přesune ho na druhou část replikační vidlice, kde se řetězec zabuduje do dceřiného vlákna.[4]
Velmi nebezpečným případem, je když dojde k poškození oddělení obou vláken DNA. Takový případ může vést k reorganizaci genomu. V nejhorších případech se jedná o nevratné poškození z toho důvodu, že ani jedno vlákno nemůže sloužit jako předloha. Buňka následně zemře při příští mitóze, nebo v ojedinělých případech dojde k mutaci. Existují tři mechanismy na opravu oddělení obou vláken (DSBs), ty mají zkratky: (NHEJ), (MMEJ) a homologní rekombinace. V prostředí in vitro, se u buněk savců objevil MMEJ na úrovních 10 - 20 % oproti HR, když byly oba mechanismy HR a NHEJ také dostupné.
Při mechanismu s NHEJ se vytvoří komplex z specializované DNA ligázy (DNA ligáza IV) s kofaktorem XRCC4, který se připojí na oba konce. Aby bylo docíleno přesné opravy NHEJ spoléhá na krátké homologního sekvence, mikrohomologního charakteru. Ty jsou přítomné na konečných částech jednoho vlákna DNA, k následnému spojení. Když jsou tyto dva převisy kompatibilní dojde k přesné opravě. Během opravy s NHEJ se může během vyskytnout i mutace. Ztráta poškozených nukleotidů u narušené prostorové konfigurace může vést k odstranění, nebo spojení nekompatibilních konců a vložení nesprávných sekvencí, či translokaci. NHEJ je obzvláště důležitý před tím, než buňka replikuje svou DNA, protože není žádná dostupná předloha pro opravu způsobem HR. U vyšších eukaryot existují i "záložní" pochody NHEJ, kromě role pečovatele o genom je NHEJ potřeba pro spojování háčkovitých útvarů během opravy indukované V(D)J rekombinací. Tento proces generuje velmi užitečnou rozmanitost na B-buněčném receptoru a T-buněčném receptoru v imunitním systému obratlovců.
Homologní rekombinace vyžaduje přítomnost identické, nebo použití téměř identické sekvence jako předlohu pro opravu poškozené části. Enzymatické procesy zodpovědné za průběh opravy jsou téměř stejné jako procesy probíhající při chromozomální cross-over během meiózy. Základem procesu je spravení poškozeného chromozomu za použití sousední chromatidy (přístupné v G2 po replikaci DNA), nebo využití homologní chromozomu jako vzoru. DSBs způsobí kolaps replikační vidlice a jsou následně opraveny rekombinací. Tyto DSBs jsou způsobené během procesu replikace, snahou o syntetizování s narušením na jednom vlákně, nebo nespravené léze.
MMEJ počíná odstraněním konce o krátkém rozsahu a to MRE11 nukleázou na obou koncích narušení lokalizovaných na obou vláknech, při tom se odhalí mikrohomologní oblasti. V dalších krocích je vyžadována Poly (ADP-ribóza), polymeráza 1 (PARP1) na počáteční krok MMEJ. Dále je párování mikrohomologních oblastí následováno dodáním 1 (FEN1) na odstranění převislých částí. Navazuje dodání XRCC1-LIG3 na místo pro spojení konců DNA, vedoucí k získání neporušené DNA. MMEJ funguje vždy s odstraňováním, což z MMEJ dělá mutagenní způsob pro opravu DNA.
Extrémofilní organismus Deinococcus radiodurans oplývá obdivuhodnou schopností přežít ionizující radiaci poškozující DNA a další ničivé zdroje. Alespoň dvě kopie genomu s náhodnými poškozeními na DNA se dokáží zformovat do fragmentů DNA, kde je vnitřní stavba DNA držená pohromadě tvorbou vodíkových můstků. Částečně převislé fragmenty jsou následovně použity pro syntézu homologních oblastí přes D-loop, nadále může pokračovat prodlužování, dokud nenalezne komplementární část vlákna. Ke konci průběhu se využije cross-over od homologní rekombinace závislé na RecA.
Topoizomeráza je aktivní v narušení týkajících se jednoho i dvou vláken za účelu změny stavu DNA nad-šroubovicovým vinutím, které je obzvláště běžné v oblastech v blízkosti otevřené replikační vidlice. Takové narušení není považováno za lézi na DNA, protože se jedná o přirozený mezikrok v biochemickém mechanismu topoizomerázy a jsou okamžitě napraveny enzymy, které je původně způsobily.
SOS odpověď
U bakteriálních buněk, silně poškozených různými způsoby, dojde k utlumení dělení a místo toho se posílí opravné mechanismy. Nukleáza RecA v tom případě aktivuje celou řadu proteinů podílejících se na SOS odpovědi. Jedná se však o značně nedokonalý proces, který slouží jako „poslední záchrana“, neboť při tomto procesu dochází k četným chybám.[4]
Konkrétně způsobem SOS odpovědi reaguje Escherichia coli a další bakterie, změnou v expresi genů, na výrazné poškození DNA. Zapojené jsou dva klíčové proteiny a to LexA a RecA. LexA je bílkovinný dimer, transkripční represor , který se váže na operační sekvence obecně nazývané SOS boxes. Je známo kolem 48 genů, včetně samotného LexA a RecA u E. coli, u kterých jsou transkripce regulovány genem LexA. SOS odpověď je u bakterií široce rozšířená , ale u některých konkrétních kmenů chybí jako jsou například spirochéty. Obecnými spouštěči SOS odpovědi jsou v buňce oblasti DNA o jednom vláknu vycházející z replikační vidlice, při oddělení obou vláken od sebe. Oddělení obou vláken DNA je zaručené mechanismem za přítomnosti DNA helikázy. V počátečním kroku se bílkovina RecA naváže na ssDNA v reakci ATP hydrolýzy vedoucí k vytvoření RecA - ssDNA vláken. RecA - ssDNA vlákna aktivují autoproteázu, která ultimátně vede k výstřihu LexA dimeru a také degradaci. Ztráta LexA represoru indukuje transkripci genů podílejících se na SOS, napomáhá další indukci signálů, inhibice a navyšuje úroveň množství proteinů v procesu řešení poškození.
V Escherichia coli, jsou SOS boxy jsou složené z sekvence o přibližné délce 20 nukletidů (blízko promotoru s strukturou palindromu). V jiných třídách a kmenech se úseky SOS boxů velmi odlišují (jiné délky i složení sekvencí). Přesto se jedná o jedny z nejsilnějších signálů v genomu. Vysoký obsah informací v SOS boxes dovoluje vázání LexA na různé promotory, umožňuje načasování SOS odpovědi. Geny na opravu DNA jsou vyvolány na počátku mechanismů SOS odpovědi. Jako poslední záchranná možnost, jsou následně vypuštěny translační polymerázy náchylné k tvoření chyb, jako například UmuCD´2 (DNA polymeráza V). K potřebnému snížení koncentrace jednovláknité DNA v buňce, dochází po opravení poškození na DNA, nebo obejití mezery za použití polymerázy a rekombinace. Tím se sníží i množství RecA vláken, vedoucí k snížení aktivity LexA dimeru, který způsoboval vystřihávání. LexA se ke konci naváže k SOS boxům v blízkosti promotorů a obnoví běžnou expresi genů.
Oprava DNA a stárnutí
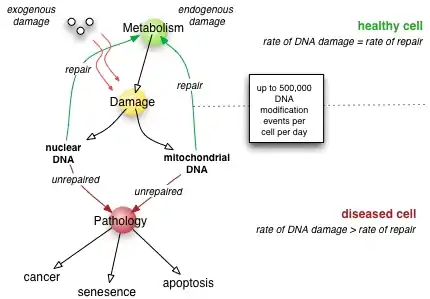
Patologické účinky nedostatečné opravy DNA
U experimentálních zvířat s nedostatečnou opravou DNA způsobenou nedostatečným procesem spojeným s geny bylo zaznamenané snížení délky života a zvýšené riziko vzniku rakoviny. U laboratorních myší s deficitem v dominantním způsobu opravy NHEJ a také v údržbě mechanismů spojených s telomerami, bylo častěji zaznamenáno onemocnění Lymfomem a infekcí, což jim zkracovalo délku života. Podobné změny byly u myší, které měly menší míru transkripčního proteinu, který uvolňuje DNA helikázu. Vyskytl se u nich předčasný nástup onemocnění souvisejících se stárnutím a s tím spojená kratší délka života. Deficit přítomný u NER, způsoboval u myší kratší délku života, bez navýšení míry mutací.
Pokud typ poškození DNA překročí míru, jakou je buňka schopna opravovat, kumulace chyb může v buňce ve výsledku způsobit stárnutí, rakovinu, nebo apoptózu. Zděděné nemoci spojené s poškozeným mechanismem opravy DNA, vedou k předčasnému stárnutí, zvýšené citlivosti na účinky karcinogenů a zvýšenému riziku vzniku rakoviny. Na druhou stranu u organismů s zvýšenou mírou opravy DNA a s tím spojených mechanismů, jako například u Deinococcus radiodurans se projevuje rostoucí rezistence na narušení obou vláken DNA. Kdy toto narušení může být způsobené radioaktivitou. Zvýšená rezistence je zapříčiněna navýšenou efektivitou procesů opravy DNA a především NHEJ.
Dlouhodobá a kalorická omezení
Bylo identifikováno několik konkrétních genů ovlivňujících různost v délce života v populaci organismů. Působení těchto genů je velmi závislé na okolním prostředí, konkrétně na složení stravy u jednotlivých organismů. Restrikce v příjmu kalorií, reprodukovatelně vede k prodloužené životnosti u různých druhů organismů. To například snížením bazálního metabolického výdeje. Nejsou plně známé pochody molekulárních mechanismů, které jsou způsobené restrikcí v příjmu kalorií. Nicméně pochody zapojených genů do opravy DNA se mění za podmínky omezení příjmu kalorií. U několika zapojených látek byly zaznamenány a prokázány účinky odvrácení stárnutí. Například tlumí konstitutivní hladinu mTOR, který signalizuje redukci metabolických reakcí. Souběžně snižuje konstitutivní úroveň poškození DNA indukované reaktivními sloučeninami s kyslíkem, které jsou generované z vnějšího prostředí.
Například navýšení výskytu jednoho konkrétní genu v genomu (SIR-2), který reguluje obalování DNA v háďátku obecném. Obecně háďátku navýší délku života. Analogový gen (genu Sir-2) u savců indukuje faktory opravy DNA typu NHEJ. Restrikce kalorií byla spojena s mírou excitace opravy bází v nukleární DNA hlodavců, nicméně podobné procesy nebyly pozorovány u mitochondriální DNA.
Gen AGE-1 u háďátka obecného, dramaticky prodlužuje délku života pod podmínkami dodávaní různého typu stravy. Nicméně vede pod kalorickou restrikcí k snížení reprodukčního stavu zdraví. Tyto pozorování potvrzují teorii pleiotropie o biologickém původu procesu stárnutí. V podstatě odkazuje na to, že geny užitečné k přežití, budou v raném vývoji vybrány k aktivování u živého organismu i přesto, že v sobě souběžně nesou i znevýhodnění rozvíjející se až později během života.
Oprava DNA a rakovina
| HR | NHEJ | SSA | FA | BER | NER | MMR | |
|---|---|---|---|---|---|---|---|
| ATM | x | x | x | ||||
| ATR | x | x | x | ||||
| PAXIP | x | x | |||||
| RPA | x | x | x | ||||
| BRCA1 | x | x | |||||
| BRCA2 | x | x | |||||
| RAD51 | x | x | |||||
| RFC | x | x | x | ||||
| XRCC1 | x | x | |||||
| PCNA | x | x | x | ||||
| PARP1 | x | x | |||||
| ERCC1 | x | x | x | x | |||
| MSH3 | x | x | x |
Tabulka: Při vývoji rakoviny jsou často mutované geny, které jsou zapojené do cest a způsobů opravy DNA (HR = homologní rekombinace, NHEJ = nehomologní spojování konečných částí, SSA = Napojování jednoho vlákna tvorbou vodíkových vazeb, FA = genetická porucha (fanconi anemia), BER = oprava excitací báze, NER = oprava excitací nukleotidu, MMR = oprava na přeskáčku.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku DNA repair na anglické Wikipedii.
- ROBERT C. KING; WILLIAM D. STANSFIELD; PAMELA K. MULLIGAN. A Dictionary of Genetics, Seventh Edition. [s.l.]: Oxford University Press, 2006.
- Robert K. Murray; Daryl K. Granner; Joe C. Davis; Peter A. Mayes; Victor W. Rodwell. Harper’s Illustrated Biochemistry; twenty-sixth edition. [s.l.]: [s.n.], 2003. ISBN 0-07-138901-6.
- ALBERTS, Bruce, et al. Essential Cell Biology. 2. vyd. New York: Garland Science, 2004. Dostupné online.
- VOET, Donald; VOET, Judith. Biochemie. 1.. vyd. Praha: Victoria Publishing, 1995. ISBN 80-85605-44-9.