Pyrimidin
Pyrimidin je šestičlenná heterocyklická aromatická organická sloučenina podobná benzenu a pyridinu. Obsahuje dva atomy dusíku na pozicích 1 a 3 v šestičlenném kruhu. Název je odvozen od řeckého pyr (teplo, oheň) a sloučenin skupiny amidů. Podle systematického názvosloví je také nazýván 1,3-diazin.
| Pyrimidin | |
|---|---|
 | |
 | |
| Obecné | |
| Systematický název | 1,3-diazin |
| Sumární vzorec | C4H4N2 |
| Identifikace | |
| Registrační číslo CAS | 289-95-2 |
| Vlastnosti | |
| Molární hmotnost | 80,08 g/mol |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Pyrimidin je izomerický se dvěma formami diazinu. Jsou to pyrazin (atomy dusíku na 1 a 4 pozici) a pyridazin (atomy dusíku na 1 a 2 pozici).
Deriváty pyrimidinu jsou tři nukleové báze, které se nacházející v nukleotidech nukleových kyselin. Jsou to cytosin (C), thymin (T) a uracil (U). Jsou to životně důležité látky, které se nalézají ve všech živých organismech a jsou nositeli jejich dědičných vlastností.
Vzorec pyrimidinu

Deriváty pyrimidinu
| Vzorec | Jméno | C2 | C4 | C5 | C6 |
|---|---|---|---|---|---|
| C4H5N3O | cytosin | =O | –NH2 | –H | –H |
| C4H4N2O2 | uracil | =O | =O | –H | –H |
| C4H3FN2O2 | fluorouracil | =O | =O | –F | –H |
| C5H6N2O2 | thymin | =O | =O | –CH3 | –H |
| C4H4N2O3 | kyselina barbiturová | =O | =O | –H | =O |
| C5H4N2O4 | kyselina orotická | =O | =O | –H | -COOH |
Nukleové báze
Nejdůležitějšími deriváty pyrimidinu jsou nukleové báze - cytosin, uracil, thymin. Dalšími nukleovými bázemi jsou deriváty odvozené z purinu - adenin, guanin.
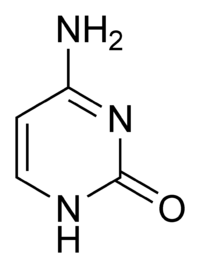 Cytosin (C)
Cytosin (C)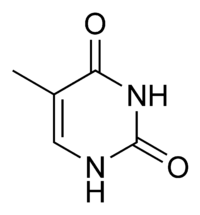 Thymin (T)
Thymin (T) Uracil (U)
Uracil (U)
Nukleové báze odvozené z pyrimidinu a purinu se v nukleových kyselinách obvykle vážou na ribózu (ribonukleová kyselina RNA) nebo na deoxyribózu (deoxyribonukleová kyselina DNA):
- v RNA se vyskytují čtyři báze: adenin (A), guanin (G), cytosin (C) a uracil (U)
- v DNA se vyskytují čtyři báze: adenin (A), guanin (G), cytosin (C) a thymin (T)
V nukleových kyselinách vytvářejí nukleové báze doplňkové dvojice (komplementární páry), v nichž se vždy jedna purinová a jedna pyrimidinová báze vzájemně vážou vodíkovými vazbami. Guanin se váže s cytosinem a adenin s thyminem nebo s uracilem. Tyto vazby tvoří kód k zápisu genetické informace v živých organismech. Komplementární párování pak umožňuje tuto informaci realizovat při procesech replikace, transkripce a translace.
Chemické vlastnosti
Chemické vlastnosti pyrimidinu se v mnohém shodují s pyridinem a benzenem. Jeho aromatický charakter způsobuje, že se snadno zúčastňuje elektrofilních a nukleofilních aromatických substitucí. Tedy reakcí, kdy elektrofil nebo nukleofil nahrazuje jinou skupinu navázanou na aromatické jádro. S narůstajícím počtem atomů dusíku v cyklu klesá energie pi elektronů a elektrofilní aromatická substituce se stává mnohem obtížnější, zatímco nukleofilní aromatická substituce se stává snadnější.
Reference
V tomto článku byl použit překlad textu z článku Pyrimidin na německé Wikipedii.
V tomto článku byl použit překlad textu z článku Pyrimidine na anglické Wikipedii.
- Pyrimidine. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)

