Katecholboran
Katecholboran (zkráceně HBcat) je organoboran používaný v organické syntéze; jedná se o derivát pyrokatecholu a boranu se vzorcem C6H4O2BH.
| Katecholboran | |
|---|---|
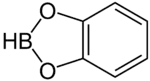
Strukturní vzorec | |
Model molekuly | |
| Obecné | |
| Systematický název | 2H-1,3,2-benzodioxaborol |
| Ostatní názvy | 7,9-dioxa-8λ2-borabicyklo[4.3.0]nona-1,3,5-trien, HBcat |
| Sumární vzorec | C6H5BO2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 274-07-7 |
| EC-no (EINECS/ELINCS/NLP) | 205-991-5 |
| PubChem | 6327445 |
| SMILES | [B]1OC2=CC=CC=C2O1 |
| InChI | 1S/C6H5BO2/c1-2-4-6-5(3-1)8-7-9-6/h1-4,7H |
| Vlastnosti | |
| Molární hmotnost | 119,91 g/mol |
| Teplota tání | 12,0 °C (285,2 K)[1] |
| Teplota varu | 50 °C (50 mmHg) |
| Hustota | 1,125 g/cm3 |
| Bezpečnost | |
| [1] | |
| H-věty | H225 H314[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P260 P264 P280 P301+330+331 P303+361+353 P304+340 P305+351+338 P310 P321 P363 P370+378 P403+235 P405 P501[1] |
| Teplota vzplanutí | 2 °C (275 K) |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava a struktura
Katecholboran se původně vyráběl reakcí katecholu s boranem (BH3) v ochlazovaném tetrahydrofuranu; při tomto postupu se ovšem ztrácí dva ekvivalenty hydridu. Nöth a Männig vyvinuli vhodnější způsob spočívající v reakci borohydridu alkalického kovu (LiBH4, NaBH4 nebo KBH4) s tris(katecholáto)bisboranem za použití etherového rozpouštědla, například diethyletheru.[2] V roce 2001 zveřejnil Herbert C. Brown dalčí postup, zahrnující reakci tri-O-fenylenbisborátu s diboranem, přičemž lze jako rozpouštědlo použít triglym nebo tetraglym. Tato metoda se vyznačuje 85% výtěžností a produkt 97% čistotou.[3]
Na rozdíl od samotného boranu nebo alkylboranů se katecholboran vyskytuje jako monomer. Tato vlastnost je důsledkem elektronových vlivů aryloxyskupin, které snižují Lewisovskou kyselost boru. Pinakolboran má strukturu podobnou.
Reakce
Katecholbotran v hydroboracích reaguje pomaleji než boran v tetrahydrofuranu (THF) nebo dimethylsulfidu (DMS).
Reakcemi katecholboranu s koncovými alkyny vznikají trans-vinylborany:
- C6H4O2BH + HC2R → C6H4O2B-CHCHR
Produkty mohou být následně zapojeny do Suzukiových reakcí.[4][5]
Katecholboran lze použít jako stereoselektivní redukční činidlo pro přeměnu β-hydroxyketonů na syn-1,3-dioly.
Katecholboran se oxidativně aduje na komplexy kovů s nízkými oxidačními čísly, přičemž se tvoří borylové komplexy.[6]
- C6H4O2BH + Pt(PR3)2 → C6H4O2BPt(PR3)2H
Reference
V tomto článku byl použit překlad textu z článku Catecholborane na anglické Wikipedii.
- https://pubchem.ncbi.nlm.nih.gov/compound/6327445
- Process for producing catecholborane - Patent 4739096
- New Economical, Convenient Procedures for the Synthesis of Catecholborane
- Janice Gorzynski Smith Organic Chemistry: Second Edition 2008 pp 1007
- MIYAURA, Norio; SUZUKI, Akira. Palladium-Catalyzed Reaction of 1-Alkenylboronates with Vinylic Halides: (1Z,3E)-1-Phenyl-1,3-octadiene. Org. Synth.. 1990, s. 130. DOI 10.15227/orgsyn.068.0130. (anglicky)
- Emily C. Neeve; Stephen J. Geier; Ibraheem A. I. Mkhalid; Stephen A. Westcott; Todd B. Marder. Diboron(4) Compounds: From Structural Curiosity to Synthetic Workhorse. Chemical Reviews. 2016, s. 9091–9161. DOI 10.1021/acs.chemrev.6b00193. PMID 27434758.

