Terc-butylalkohol
terc-Butylalkohol (systematický název 2-methylpropan-2-ol) je nejjednodušší terciární alkohol, jeden ze čtyř izomerů butanolu. Je zvláštní tím, že je za pokojové teploty pevnou látkou, neboť jeho teplota tání je mírně nad 25 °C.

| terc-Butylalkohol | |
|---|---|
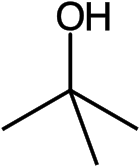
Strukturní vzorec | |
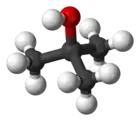
Prostorový model | |
| Obecné | |
| Systematický název | 2-methylpropan-2-ol |
| Triviální název | tercbutanol[zdroj?!] |
| Ostatní názvy | t-butanol, 2-methyl-2-propanol, terc-butylalkohol, 2-methylisopropylalkohol |
| Anglický název | 2-Methylpropan-2-ol (systematický název), 2-methyl-2-propanol, tert-butanol, tert-butylalcohol |
| Německý název | tert-Butanol |
| Funkční vzorec | C(CH3)3OH |
| Sumární vzorec | C4H10O |
| Vzhled | bezbarvá kapalina/pevná látka kafrového zápachu |
| Identifikace | |
| Registrační číslo CAS | 75-65-0 |
| EC-no (EINECS/ELINCS/NLP) | 200-889-7 |
| PubChem | 6386 |
| ChEBI | 45895 |
| UN kód | 1120 |
| SMILES | CC(C)(C)O |
| InChI | 1S/C4H10O/c1-4(2,3)5/h5H,1-3H3 |
| Vlastnosti | |
| Molární hmotnost | 74,12 g/mol |
| Teplota tání | 25–26 °C (298–299 K) |
| Teplota varu | 82–83 °C (355–356 K) |
| Hustota | 0,775 g/cm3 |
| Index lomu | 1,387 |
| Rozpustnost ve vodě | velmi dobře rozpustný |
| Rozpustnost v polárních rozpouštědlech |
mísitelný s ethanolem a diethyletherem |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −360,04 až −358,36 kJ/mol |
| Standardní molární spalná entalpie ΔH°sp | −2644,79 až −2643,21 kJ/mol |
| Standardní molární entropie S° | 189,5 JK−1mol−1 |
| Měrné teplo | 215,37 JK−1mol−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H225 H319 H332 H335 |
| P-věty | P210 P261 P305 |
| R-věty | R11, R20, R36 |
| S-věty | S2, S9, S16, S46 |
| NFPA 704 |  3
1
0
|
| Teplota vzplanutí | 15 °C |
| Teplota vznícení | 480 °C |
| Meze výbušnosti | 2,4–8,0 % |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Výskyt
terc-Butylalkohol byl nalezen v pivu a cizrně, ovšem jeho obsah nebyl zjištěn.[2] Také se nachází v manioku jedlém, který se používá jako fermentační přísada v některých alkoholických nápojích.
Výroba
terc-Butylalkohol se průmyslově vyrábí z isobutanu jako společný produkt výroby propylenoxidu.
Také jej lze vyrobit katalytickou hydratací isobutylenu nebo Grignardovou reakcí acetonu a methylmagnesiumchloridu.
Použití
terc-Butylalkohol se používá jako rozpouštědlo, jako denaturační činidlo pro výrobu denaturovaného ethanolu, jako přísada do odstraňovačů barev, ke zvyšování oktanového čísla benzinu. Je rovněž meziproduktem při výrobě dalších sloučenin, jako jsou MTBE, ETBE, TBHP a různé vůně a parfémy.
Chemické vlastnosti
Jako terciární alkohol je terc-butylalkohol nezoxidovatelný, je také stabilnější a méně reaktivní než ostatní izomery butanolu i v dalších reakcích.
Když je deprotonován silnými zásadami, vzniká z něj alkoxidový anion, který se v tomto případě nazývá terc-butoxid, například často používané organické činidlo terc-butoxid draselný se připravuje reakcí suchého terc-butylalkoholu s kovovým draslíkem:
2 K + 2 tBuOH → 2 tBuO−K+ + H2.
Samotný terc-butoxid je také užitečný jako silná nenukleofilní zásada v organické chemii.
Převod na alkylhalidy
terc-Butylalkohol reaguje s chlorovodíkem za vzniku terc-butylchloridu a vody.
Reference
V tomto článku byl použit překlad textu z článku Tert-Butyl alcohol na anglické Wikipedii.
- Tert-Butanol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- http://toxnet.nlm.nih.gov/cgi-bin/sis/search/a?dbs+hsdb:@term+@DOCNO+50
Externí odkazy
 Obrázky, zvuky či videa k tématu terc-butylalkohol na Wikimedia Commons
Obrázky, zvuky či videa k tématu terc-butylalkohol na Wikimedia Commons

