Cyklohexenon
Cyklohexenon (cyklohex-2-en-1-on) je organická sloučenina, která patří mezi ketony, konkrétně mezi enony. Jedná se o užitečný meziprodukt při syntéze různých látek jako jsou léčiva a vůně.[2] V čisté podobě to je čirá bezbarvá kapalina, ovšem komerční produkty jsou zpravidla nažloutlé.
| Cyklohexenon | |
|---|---|
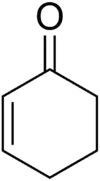
strukturní vzorec | |
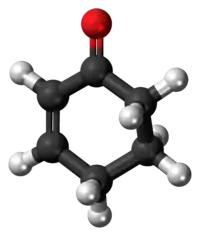
model molekuly | |
| Obecné | |
| Systematický název | Cyklohex-2-en-1-on |
| Anglický název | cyclohexenone |
| Sumární vzorec | C6H8O |
| Vzhled | bezbarvá nebo nažloutlá kapalina |
| Identifikace | |
| Registrační číslo CAS | 930-68-7 |
| PubChem | 13594 |
| ChEBI | 15977 |
| SMILES | C1CC=CC(=O)C1 |
| InChI | 1/C6H8O/c7-6-4-2-1-3-5-6/h2,4H,1,3,5H2 |
| Vlastnosti | |
| Molární hmotnost | 96,127 g/mol |
| Teplota tání | −53 °C (220 K) |
| Teplota varu | 171 až 173 °C (444 až 446 K) |
| Rozpustnost ve vodě | 4,13 g/100 ml |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v alkoholech a aprotických polárních rozpouštědlec |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v etherech, esterech a halogenalkanech |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R10 R22 R23/24 R36/37/38 |
| S-věty | S20 S27 S36/37/39 S45 S60 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
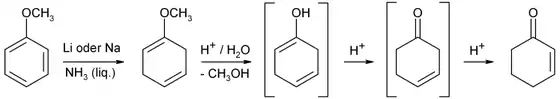
Průmyslově se vyrábí z fenolu Birchovou redukcí.[3]
Běžné reakce cyklohexenonu jsou nukleofilní konjugovaná adice s organoměďnatými činidly, Michaelovy reakce a Robinsonovy anelace.[4][5]
Vlastnosti
Cyklohexen je rozpustný v mnoha rozpouštědlech jako jsou alkoholy, ethery, halogenuhlovodících, esterech a rovněž v aprotických polárních rozpouštědlech.
Cyklohexenon reaguje s ketony i alkeny. Jako typický zástupce α,β-nenasycených karbonylových sloučenin má nízkou elektronovou hustotu na uhlíkových atomech tvořících dvojnou vazbu.
Při reakci se silnými zásadami dochází k deprotonaci na čtvrtém a šestém uhlíkovém atomu.
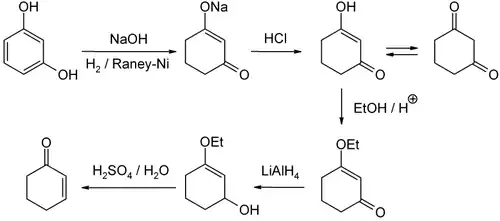
Výroba
Existuje několik různých způsobů výroby cyklohexenonu. V laboratořích se používá redukce 3-ethoxy-2-cyklohexen-1-onu a následně kyselá hydrolýza vzniklého produktu. Prekurzor lze získat z 1,3-cyklohexandionu, který se zase připraví z resorcinolu.
Jako výchozí surovinu lze rovněž použít anisol. Cyklohexenon se z něj získá Birchovou redukcí následovanou kyselou hydrolýzou.
Dalšími možnostmi jsou příprava z cyklohexanonu α-bromací a eliminací a rovněž z 3-chlorcyklohexenu hydrolýzou a oxidací.
Průmyslově se cyklohex-2-en-1-on vyrábí katalytickou oxidací cyklohexenu, například peroxidem vodíku za přítomnosti katalytzátorů s obsahem vanadu. Bylo vyvinuto několik, patentovaných, postupů s různými oxidačními činidly a katalyzátory.
Použití
Cyklohexenon je látkou často používanou v organické syntéze, jelikož umožňuje mnoho způsobů rozšiřování molekul. Snadno u něj probíhá Michaelova adice s nukleofily (například enoláty či silylenolethery); lze jej rovněž zapojit do Dielsovy–Alderovy reakce s dieny s vysokou elektronovou hustotou. Též reaguje s organoměďnatými sloučeninami 1,4 adicí (Michaelovou adicí) či s Grignardovými činidly 1,2 adicí. Využívá se také při syntéze polycyklických přírodních látek.
Roku 1986 bylo náhodou zjištěno, že cyklohexenon působí jako in-vitro katalyzátor dekarboxylace alfa-aminokyselin.[6] Japonští výzkumníci zkoumali využití ditercbutylperoxidu jako katalyzátoru dekarboxylace za použití cyklohexanolu jako rozpouštědla, ovšem zjistili, že když použili méně čistý (tedy technický, 98%) cyklohexanol, reakce probíhala asi čtyřikrát rychleji než při použití čistšího cyklohexanolu (>99,3%). Následně zjistili, že cyklohexanol obsahoval cyklohexenon jako nečistotu, která byla v technické látce přítomna ve třikrát větší koncentraci (přibližně 0,3 % oproti 0,1 %). Dalším výzkumem bylo zjištěno, že 1% roztok cyklohexenonu v cyklohexanolu dekarboxyluje většinu aminokyselin, včetně neobvyklých, s výtěžností 80-95 % během několika hodin. Výjimkami jsou například histidin, kde reakce trvala přes 26 hodin, a polyaminokyseliny, u nichž k dekarboxylaci při použití cyklohex-2-en-1-onu vůbec nedošlo a je třeba hledat jiné způsoby.[7]
Reference
V tomto článku byl použit překlad textu z článku Cyclohexenone na anglické Wikipedii.
- 2-Cyclohexen-1-one. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- Podraze, K.F. Org. Prep. Proced. Int., 1991, 23, p. 217.
- Organic Building Blocks of the Chemical Industry, Harry H. Szmant, ISBN 978-0-471-85545-3
- Michael G. Organ and Paul Anderson. Carbonyl and Conjugate Additions to Cyclohexenone: Experiments Illustrating Reagent Selectivity. Journal of Chemical Education. 1996, s. 1193. DOI 10.1021/ed073p1193. (anglicky)
- Tetrahedron Lett. 34, 3881, (1993)
- HASHIMOTO, M; EDA, Y; YASUTOMO, O; TOSHIAKI, I; AOKI, S. A novel decarboxylation of .ALPHA.-amino acids. A facile method of decarboxylation by the use of 2-cyclohexen-1-one as a catalyst.. Chemistry Letters. 1986, s. 893–896. Dostupné online [cit. 4 January 2016]. DOI 10.1246/cl.1986.893. (anglicky)
- LAVAL, G; GOLDING, B. One-pot Sequence for the Decarboxylation of α-Amino Acids. Synlett. 2003, s. 542–546. Dostupné online [cit. 4 January 2016]. DOI 10.1055/s-2003-37512. (anglicky)