4-nitrochlorbenzen
4-nitrochlorbenzen (systematický název 1-chlor-4-nitrobenzen) je organická sloučenina používaná jako surovina při výrobě řady průmyslově využívaných sloučenin jako jsou antioxidanty v kaučuku. Je izomerní s 2-nitrochlorbenzenem a 3-nitrochlorbenzenem.
| 4-nitrochlorbenzen | |
|---|---|
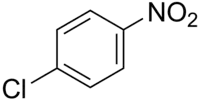
Strukturní vzorec | |
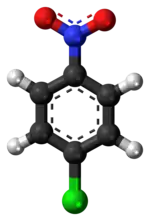
Model molekuly | |
| Obecné | |
| Systematický název | 1-chlor-4-nitrobenzen |
| Anglický název | 4-nitrochlorobenzene |
| Sumární vzorec | C6H4ClNO2 |
| Vzhled | světle žlutá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 100-00-5 |
| PubChem | 7474 |
| SMILES | C1=CC(=CC=C1[N+](=O)[O-])Cl |
| InChI | 1/C6H4ClNO2/c7-5-1-3-6(4-2-5)8(9)10/h1-4H |
| Vlastnosti | |
| Molární hmotnost | 157,55 g/mol |
| Teplota tání | 83,6 °C (356,8 K) |
| Teplota varu | 242,0 °C (515,2 K) |
| Hustota | 1,52 g/cm3 (20 °C) |
| Index lomu | 1,5857 (60 °C) |
| Rozpustnost ve vodě | nerozpustný |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v acetonu a horkém ethanolu |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v diethyletheru a toluenu |
| Tlak páry | 27 Pa (30 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Teplota vzplanutí | 12 °C (285 K) |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Výroba
4-nitrochlorbenzen se průmyslově vyrábí nitrací chlorbenzenu:[2]
Touto reakcí vznikají 2-nitroizomer a 4-nitroizomer v poměru 1:2, které se oddělí destilací. 4-nitrochlorbenzen byl původně získán nitrací 4-bromchlorobenzenu.[3]
Použití
4-nitrochlorbenzen je meziproduktem při výrobě mnoha dalších látek. Nitrací z něj vzniká 2,4-dinitrochlorbenzen a 1,2-dichlor-4-nitrobenzen. Redukcí kovovým železem vzniká 4-chloranilin. Díky přítomnosti nitroskupiny je benzenové jádro (na rozdíl od podobného chlorbenzenu) náchylné k nukleofilní aromatické substituci. Silně nukleofilní sloučeniny jako například hydroxidy, methoxidy a anorganické amidy nahrazují atom chloru jinými funkčními skupinami, přičemž se utváří 4-nitrofenol, 4-nitroanisol respektive 4-nitroanilin.[2]
Dalším významným způsobem použití 4-nitrochlorbenzenu je jeho kondenzace s anilinem za vzniku 4-nitrodifenylaminu. Redukční alkylací nitroskupin vznikají sekundární arylaminy používané jako antioxidanty v kaučuku.
.
Reference
V tomto článku byl použit překlad textu z článku 4-Nitrochlorobenzene na anglické Wikipedii.
- 1-Chloro-4-nitrobenzene. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- Gerald Booth "Nitro Compounds, Aromatic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim, 2005.
- "The nitration of mixed dihalogen benzenes" Recueil des Travaux Chimiques des Pays-Bas et de la Belgique. Amsterdam, 1915; pp. 204-235.


