Koordinační polymer
Koordinační polymer je anorganický nebo organokovový polymer, který obsahuje kationty kovů propojené ligandy. Jinak řečeno se jedná o koordinační sloučeninu s opakujícími se koordinačními jednotkami.[1]
Koordinační polymery mají mnoho potenciálních využití.[2]
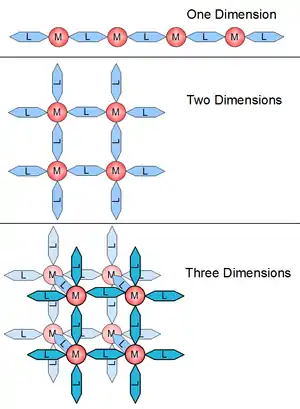
Koordinační polymery lze, na základě struktury a složení, dělit několika způsoby. Prvním z nich je dimenzionalita, kde struktury mohou být jedno-, dvoj- nebo trojrozměrné.[3]
Historie
Základ výzkumu koordinačních polymerů vytvořily práce Alfreda Wernera a jeho současníků. Mnoho významných látek je tak řazeno mezi koordinační polymery; například kyanidové komplexy berlínská modř a Hofmannovy klatráty.[4]
Příprava
Koordinační polymery se mohou připravit několika metodami, například kokrystalizací solí kovů s ligandy.[2]
Vazby a mezimolekulové síly
Mezi síly, které ovlivňují vlastnosti koordinačních komplexů, patří van der Waalsovy síly, pí-pí interakce, vodíkové vazby a stabilizace polarizovaných vazeb pí. Tyto molekulové interakce jsou slabé a oproti kovalentním vazbám mají dlouhé rovnovážné vzdálenosti; například pí-pí interakce mezi molekulami benzenu vykazují energie přibližně 5–10 kJ/mol a délky 3,4–3,8 ångstromů.
Koordinace
Krystalová struktura a dimenzionalita koordinačních polymerů jsou určovány funkčními skupinami na ligandech a koordinační geometrií kovového centra. Dimenzionalitu obvykle řídí kov, na nějž se v některých případech váže až 16 funkčních skupin; v některých případech však hlavní vliv mají navázané skupiny, kde se může jedna skupina vázat na více atomů kovu, než kolik skupin se váže na jeden kov.[5]
Nejvyšší zaznamenané koordinační číslo u koordinačního polymeru je 14,[6] nejčastěji bývá mezi 2 a 10.[7]
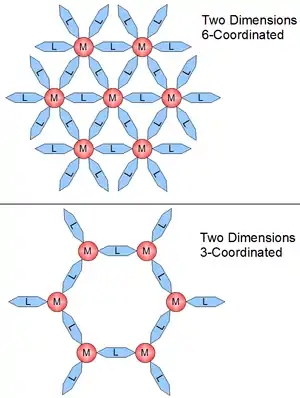
Příklady rovinných komplexů s různými koordinačními čísly jsou uvedeny na obrázku 2. Na obrázku 1 je jednorozměrná struktura 2-koordinovaná, dvourozměrná 4-koordinovaná je 6-koordinovaná.
Kovová centra
Kovové ionty se vážou na dané počty ligandů a v daných úhlech. Počet ligandů navázaných na jeden atom kovu se nazývá koordinační číslo a, společně s úhly vazeb, určuje dimenzionalitu polymeru. Koordinační číslo a koordinační geometrie kovového centra jsou určovány nerovnoměrným rozdělením elektronové hustoty a koordinační čísla bývají větší i rozměrnějších kationtů. K předpovídání a vysvětlení koordinačních geometrií se používá několik postupů, jako jsou hybridizace orbitalů a teorie molekulových orbitalů, s využitím Schrödingerovy rovnice, toto předpovídání je ovšem obtížné, protože vlivy prostředí na rozdělení elektronové hustoty mohou být složité.[9]
Přechodné kovy
Přechodné kovy jsou jako centra v koordinačních polymerech časté. Částečně zaplněné orbitaly d, ať už v atomu nebo iontu, se, v závislosti na okolí, mohou hybridizovat různě. Elektronová struktura může umožňovat několik různých koordinačních geometrií, což nastává například u iontů mědi a zlata, které mají jako neutrální atomy plné orbitaly d ve vnějších slupkách.
Lanthanoidy
Lanthanoidy mají velké atomy a koordinační čísla se pohybují od 7 do 14. Jejich koordinační prostředí se často špatně předvídají, což ztěžuje jejich využití.
Lanthanoidy často umožňují dodávat produktům luminescenční vlastnosti.
Alkalické kovy a kovy alkalických zemin
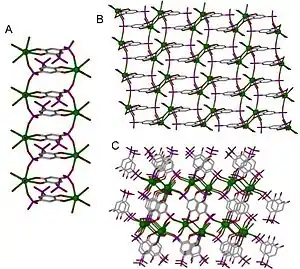
Alkalické kovy a kovy alkalických zemin tvoří stálé kationty. Kationty alkalických kovů mívají stálé valenční slupky, což jim dává vlastnosti odlišné od lanthanoidů a přechodných kovů. Jsou silně ovlivňovány protiionty solí použitých při přípravě. Koordinační polymery na obrázku 3 obsahují kovy alkalických zemin. Dimenzionalita těchto struktur se zvyšuje s nárůstem poloměrů iontů těchto kovů (v řadě vápník - stroncium - baryum).
Ligandy
Ve většině koordinačních polymerů ligandy (atomy nebo skupiny atomů) dodávají volné páry elektronů kationtům kovů a vytvářejí komplex založený na Lewisovské kyselosti a zásaditosti. Koordinační polymer vznikne, pokud může ligand vytvořit více koordinačních vazeb a fungovat jako můstek mezi různými kovovými centry. Ligandy vytvářející jednu koordinační vazbu se nazývají monodentátní, pokud nějaký může utvořit více takových vazeb, jež tak mohou vést ke koordinačnímu polymeru, jedná se o polydentátní ligand. Polydentátní ligandy mohou propojovat kovová centra a vytvářet „nekonečné“ řetězce. Jeden polydentátní ligand může být navázán i na více atomů kov; potom se jedná o chelataci. Monodentátní ligandy bývají také označovány jako koncové, protože nemají na sobě místo, kde by struktura mohla pokračovat. Koordinační polymery často obsahují kombinace poly- a monodentátních, můstkových, chelatujících a koncových ligandů.
Složení
Součástmi ligandů mohou být téměř všechny atomy obsahující volné páry elektronů. K nejčastějším ligandům v koordinačních polymerech patří polypyridiny, fenantroliny, hydroxychinoliny a polylarboxyláty. Na vazebných místech se obvykle objevují atomy kyslíku a dusíku, může však jít i o jiné prvky, například síru[10] a fosfor.[11][12]
Ligandy a kationty se obvykle chovají podle předpokladů teorie HSAB. Větší a snáze polarizovatelné „měkké“ kovy tak reagují snadněji s lépe polarizovatelnými měkkými ligandy a malé a hůře polarizovatelné „tvrdé“ kovy se lépe koordinují s tvrdými ligandy.
Strukturní orientace
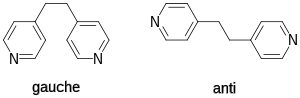
Ligandy mohou být ohebné nebo tuhé. Tuhé ligandy nemohou rotovat kolem vazeb nebo změnit své struktury. Ohebné ligandy tyto možnosti mají a rozdíly v jejich konformacích zvětšují rozmanitost struktur. Existují koordinační polymery, které mají na stejném ligandu dvě koordinace na jedné struktuře[13] nebo dvě oddělené struktury, které se od sebe liší pouze orientací ligandů.
Délka ligandu
Délka ligandu může výrazně působit na možnost tvorby polymeru oproti nepolymerním (mono- či oligomerním) uspořádáním.[14]
Ostatní vlivy
Protiionty
Kromě vlastností kovu a ligandů existuje i řada dalších faktorů ovlivňujících strukturu koordinačních polymerů. Většina kovových center je kladně nabitých a protiionty v jejich solích ovlivňují celkovou strukturu; například stříbrné soli, jako jsou dusičnan (AgNO3), tetrafluorboritan (AgBF4), chloristan (AgClO4), hexafluorfosforečnan (AgPF6), hexafluorarseničnan (AgAsF6) a hexafluorantimoničnan stříbrný (AgSbF6) při krystalizaci se stejným ligandem vytvoří rozdílné struktury, jako je koordinační prostředí kovu i dimenzionalita celého polymeru.[15]
Krystalizační prostředí
Změny v prostředí, v němž polymer krystalizuje, mohou také změnit jeho strukturu. Vliv mívají zejména pH,[16] intenzita světla a teplota.[17]
Hostující molekuly
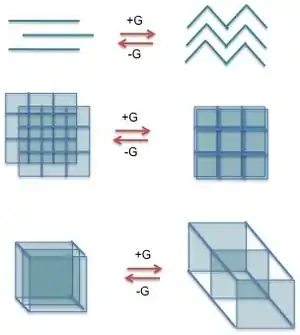
Koordinační polymery mají ve svých strukturách často prázdná místa, termodynamicky nevýhodná. Strukturu lze mnohdy stabilizovat přidáním hostujících molekul do těchto míst. Tyto molekuly nevytvářejí vazby s polymerem, ale mohou interagovat prostřednictvím mezimolekulových sil, jako jsou například vodíkové vazby. Hostující molekulou je nejčastěji rozpouštědlo, ze kterého koordinační polymer krystalizuje, může jít ovšem o jakoukoliv látku (soli, plyny jako jsou kyslík, dusík a oxid uhličitý).
Využití
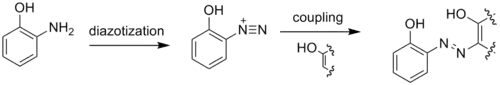
Koordinační polymer, jako jsou deriváty aminofenolů, se používají jako barviva. Komplexní barviva obsahující měď nebo chrom nacházejí využití v matných barvách. Tridentátní ligandová barviva jsou stabilnější než jejich bidentátní a monodentátní protějšky.[18][19]

K průmyslově používaným koordinačním polymerům patří Hofmannovy sloučeniny, Ni(CN)4Ni(NH3)2. Krystalizují s malými aromatickými hostujícími molekulami (benzenem, xyleny), což se využívá při oddělování těchto uhlovodíků.[20]
Výzkum
Luminescence
Luminescentní koordinační polymery zpravidla obsahují ligandy působící jako organické chromofory, které pohlcují světlo a vyzařují excitační energii. Koordinační polymery by mohly být díky svým emisním vlastnostem při zapojení hostujících molekul nejuniverzálnějšími zdroji luminescence. Luminescentní supramolekulární struktury by mohly být použity v optoelektronických zařízeních nebo jako fluorescenční senzory. Koordinační polymery často bývají, z hlediska tepla a rozpouštědel, stabilnější než čistě organické sloučeniny.
Ligandy fluoreskující bez přítomnosti kovů mohou mít fotoluminiscenci příslušných polymerů o několik řádů silnější než u volných ligandů. Lze je využít při vývoji světelných diod. Výrazný nárůst fluorescence je způsoben zvětšením asymetrie ligandu při koordinaci s kovem.[21]
Elektrická vodivost
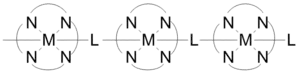
Koordinační polymery obsahují ve svých strukturách krátké anorganické a konjugované organické můstky, jež mohou vytvářet elektrickou vodivost. K vodivým koordinačním polymerům patří například vodivé organokovové sítě. Některé jednorozměrné koordinační polymery utvořené jako na obrázku výše mají měrné elektrické vodivosti mezi 1x10−6 a 2x10−1 S/cm. Jejich vodivost způsobují interakce mezi d orbitaly kovů a můstkovými ligandy. Některé tyto polymery se chovají jako polovodiče. Trojrozměrné polymery s listovitými strukturami obsahujícími stříbro jsou polovodivé při navázání kovových center do rovnoběžných poloh a při jejich přechodu do kolmého uspořádání se vodivost snižuje.[21]
Magnetismus
U koordinačních polymerů se vyskytují antiferromagnetismus, ferrimagnetismus i ferromagnetismus. K dosažení dostatečně silného magnetismu se používají malé můstkové ligandy, jako jsou oxo-, kyano- a azido-, které umožňují přiblížení atomů kovů na krátké vzdálenosti.[21]
Senzory
Koordinační komplexy často mění barvu při změně molekul rozpouštědla zabudovaných do struktury; tuto vlastnost má například komplex dvou kobaltnatých iontů navázaných na iont [Re6S8(CN)6]4−, obsahující molekuly vody koordinované na atomy kobaltu. Původně oranžový roztok se zbarví do růžova či zelena po nahrazení cody tetrahydrofuranem a do modra po přidání diethyletheru. Polymer tak může podle své barvy detekovat přítomnost různých rozpouštědel. Změny barvy po nahrazení molekul vody jinými ligandy jsou způsobeny změnou geometrie molekuly z oktaedrické na tetraedrickou.[21]
Reference
V tomto článku byl použit překlad textu z článku Coordination polymer na anglické Wikipedii.
- Stuart R. Batten, Neil R. Champness, Xiao-Ming Chen, Javier Garcia-Martinez, Susumu Kitagawa, Lars Öhrström, Michael O'Keeffe, Myunghyun P. Suh, Jan Reedijk. Terminology of metal–organic frameworks and coordination polymers (IUPAC Recommendations 2013). Pure and Applied Chemistry. 2013, s. 1715. DOI 10.1351/PAC-REC-12-11-20.
- K. Fromm. Coordination polymer networks with s-block metal ions. Coordination Chemistry Reviews. 2008, s. 856–885. Dostupné online. DOI 10.1016/j.ccr.2007.10.032.
- X. Chen; B. Ye; M. Tong. Metal-organic molecular architectures with 2,2′-bipyridyl-like and carboxylate ligands. Coordination Chemistry Reviews. 2005, s. 545–565. DOI 10.1016/j.ccr.2004.07.006.
- S. Kitagawa; R. Kitaura; S. I. Noro. Functional Porous Coordination Polymers. Angewandte Chemie International Edition. 2004, s. 2334. DOI 10.1002/anie.200300610.
- Glenn Lamming; Osama El-Zubir; James Kolokotroni; Christopher McGurk; Paul G. Waddell; Michael R. Probert; Andrew Houlton. Two-Dimensional Frameworks Based on Ag(I)–N Bond Formation: Single Crystal to Single Molecular Sheet Transformation. Inorganic Chemistry. 2016-10-03, s. 9644–9652. ISSN 0020-1669. DOI 10.1021/acs.inorgchem.6b01365.
- P. Charpin; M. Nierlich; D. Vigner; M. Lance; D. Baudry. Structure of the Second Crystalline Form of Uranium(IV) Tetrahydroborate. Acta Crystallographica Section C. 1987, s. 1465–1467. DOI 10.1107/S0108270187091431.
- A. Y. Robin; K. M. Fromm. Coordination polymer networks with O- and N-donors: What they are, why and how they are made. Coordination Chemistry Reviews. 2006, s. 2127–2157. DOI 10.1016/j.ccr.2006.02.013.
- A. Cote; G. Shimizu. Coordination Solids via Assembly of Adaptable Components: Systematic Structural Variation in Alkaline Earth Organosulfonate Networks. Chemistry—A European Journal. 2003, s. 5361–5370. DOI 10.1002/chem.200305102. PMID 14613146.
- Jeremy Bernstein; Paul M. Fishbane; Stephen G. Gasiorowicz. Modern Physics. [s.l.]: Prentice-Hall, 2000-04-03. ISBN 978-0-13-955311-0. S. 624.
- M. Wen; M. Munakata; Y. Suenaga; T. Kuroda-Sowa; M. Maekawa; S. G. Yan. Silver(I) coordination polymers of cyclic sulfur ligand, 2,2′,3,3′-tetrahydro-4,4′-dithia-1,1′-binaphthylidene. Inorganica Chimica Acta. 2001, s. 133–137. DOI 10.1016/S0020-1693(01)00556-4.
- F. Hung-Low; K. K. Klausmeyer; J. B. Gary. Effect of anion and ligand ratio in self-assembled silver(I) complexes of 4-(diphenylphosphinomethyl)pyridine and their derivatives with bipyridine ligands. Inorganica Chimica Acta. 2009, s. 426. DOI 10.1016/j.ica.2008.04.032.
- G. Ricci; A. Ricci; F. Masi; M. Ricci; A. Boglia; G. Leone. Well-defined transition metal complexes with phosphorus and nitrogen ligands for 1,3-dienes polymerization. Coordination Chemistry Reviews. 2010, s. 661. DOI 10.1016/j.ccr.2009.09.023.
- J. M. Knaust; S. W. Keller. A Mixed-Ligand Coordination Polymer from the in Situ, Cu(I)-Mediated Isomerization of Bis(4-pyridyl)ethylene. Inorganic Chemistry. 2002, s. 5650–5652. DOI 10.1021/ic025836c. PMID 12401066.
- Andrii I. Buvailo; Elzbieta Gumienna-Kontecka; Svetlana V. Pavlova; Igor O. Fritsky; Matti Haukka. Dimeric versus polymeric coordination in copper(ii) cationic complexes with bis(chelating) oxime and amide ligands. Dalton Transactions. 2010, s. 6266–6275. DOI 10.1039/C0DT00008F. PMID 20520918.
- L. Carlucci; G. Ciani; D. M. Proserpio; S. Rizzato. New polymeric networks from the self-assembly of silver(i) salts and the flexible ligand 1,3-bis(4-pyridyl)propane (bpp). A systematic investigation of the effects of the counterions and a survey of the coordination polymers based on bpp. CrystEngComm. 2002, s. 121. DOI 10.1039/b201288j.
- L. B. Ni; R. H. Zhang; Q. X. Liu; W. S. Xia; H. Wang; Z. H. Zhou. PH- and mol-ratio dependent formation of zinc(II) coordination polymers with iminodiacetic acid: Synthesis, spectroscopic, crystal structure and thermal studies. Journal of Solid State Chemistry. 2009, s. 2698–2706. DOI 10.1016/j.jssc.2009.06.042. PMID 20161370. Bibcode 2009JSSCh.182.2698N.
- M. L. Tong; S. Hu; J. Wang; S. Kitagawa; S. W. Ng. Supramolecular Isomerism in Cadmium Hydroxide Phases. Temperature-Dependent Synthesis and Structure of Photoluminescent Coordination Polymers of α- and β-Cd2(OH)2(2,4-pyda). Crystal Growth & Design. 2005, s. 837. DOI 10.1021/cg049610r.
- Grychtol, K.; Mennicke, W. (2002) "Metal-Complex Dyes." In Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH. DOI:10.1002/14356007.a16_299.
- Hunger, K.; Mischke, P.; Rieper, W.; Raue, R.; Kunde, K.; Engel, A. (2002) "Azo Dyes." In Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. DOI:10.1002/14356007.a03_245.
- Atwood, J. L. (2012) "Inclusion Compounds" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, Weinheim DOI: 10.1002/14356007.a14_119
- Stuart R. Batten. Coordination Polymers: Design, Analysis and Application. [s.l.]: RSC Publishing, 2008. ISBN 978-0-85404-837-3. DOI 10.1039/9781847558862. S. 297–307, 396–407.