Glukóza
Glukóza (v chemickém názvosloví sacharidů glukosa) (z řec. γλυκύς, tj. glykys, česky sladký nebo γλευκος, gleukos, česky mošt, sladké víno), v běžné řeči označovaná jako hroznový cukr nebo krevní cukr, je jedním z monosacharidů ze skupiny aldohexóz. V chemických vzorcích oligosacharidů a polysacharidů se značí symbolem Glc. V čistém stavu je glukosa bílá krystalická látka sladké chuti. V přírodě běžná konformace glukózy je D-glukóza, která stáčí polarizované světlo doprava, odtud pochází její staré označení dextróza, které se doposud běžně používá v lékařské literatuře.
| D-glukosa | |
|---|---|
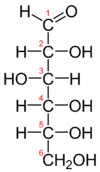
Aldehydická forma (ve Fischerově projekci) | |
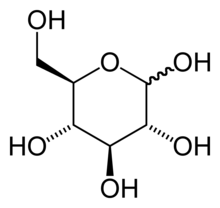
Hemiacetalová forma (standardní strukturní vzorec) | |
| Obecné | |
| Systematický název | (3R,4S,5S,6R)-6-(hydroxymethyl)oxan-2,3,4,5-tetrol (hemiacetalová forma) |
| Sumární vzorec | C6H12O6 |
| Identifikace | |
| Registrační číslo CAS | (D-glukosa) 921-60-8 (L-glukosa)&Units=SI 50-99-7 (D-glukosa) 921-60-8 (L-glukosa) |
| Vlastnosti | |
| Molární hmotnost | 180,155 g/mol |
| Teplota tání | 146 °C (bezvodá, α-D- anomer) 150 °C (bezvodá, β-D- anomer) 83 °C (monohydrát) |
| Teplota varu | rozklad |
| Hustota | 1,56 g/cm3 |
| Rozpustnost ve vodě | 1 200 g/l |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Výroba
D-Glukóza se může připravit krystalizací z rostlinných šťáv, zejména z hroznů vinné révy, ale hlavní metodou její výroby je kyselá nebo enzymatická hydrolýza rostlinného škrobu, v Česku především bramborového.
Chemické vlastnosti
Glukóza existuje ve dvou enantiomerech, a to jako D-glukóza (vyskytující se v přírodě), nazývaná též dextróza, a její zrcadlový obraz, L-glukóza. Svými chemickými a fyzikálními vlastnostmi neliší, s výjimkou toho, že jejich vodný roztok stáčí rovinu polarizovaného světla opačným směrem. V živých organismech jsou však nezaměnitelné, protože L-glukóza nemůže být fosforylována hexokinázou a nemůže tedy vstoupit do metabolismu cukrů. Některé bakterie ovšem mají enzymy schopné L-glukózu zpracovat.[1] L-Glukóza chutná stejně jako D-glukóza a byla navržena jako umělé sladidlo, kvůli vysokým nákladům na výrobu ovšem nebyla rozšířená.[2]
Vzhledem k přítomnosti aldehydické skupiny patří glukóza k redukujícím sacharidům, takže například redukuje soli dvojmocné mědi na jednomocné, což se v minulosti užívalo ke kvalitativnímu i kvantitativnímu stanovení cukru v roztoku (například v moči). Přitom se aldehydická skupina D-glukózy se mění na karboxylovou a vzniká kyselina D-glukonová. Při použití silnějších oxidačních činidel, jako například kyseliny dusičné, se oxiduje rovněž primární alkoholická skupina na opačném konci molekuly též na karboxylovou skupinu za vzniku kyseliny D-glukarové. Zoxiduje-li se pouze primární alkoholická skupina na posledním uhlíku (s lokačním číslem 6), vzniká kyselina D-glukuronová.
Redukcí glukosy, například hydrogenací vodíkem za přítomnosti katalyzátorů, se naopak redukuje aldehydická skupina na primární alkoholickou skupinu a vzniká D-glucitol, známější pod názvem sorbitol (sorbit), používaný jako umělé sladidlo pro diabetiky.
V roztoku přechází glukóza do cyklické poloacetalové formy s šestičlenným kruhem (pyranóza), která v rovnovážném stavu za laboratorní teploty 20 °C obsahuje dva anomery, lišící se orientací hemiacetalového hydroxylu: 36 % α-glukopyranózy a 64 % β-glukopyranózy.
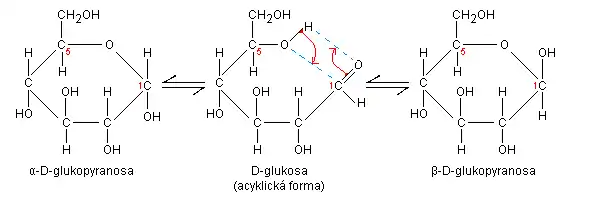
Tyto anomery jsou v dynamické rovnováze a procesem mutarotace (viz předchozí reakční schema) přecházejí s poločasem řádu hodin jeden v druhý. V obou případech prostorové uspořádání šestičlenného heterocyklu odpovídá židličkové konformaci (Z-forma). Čisté anomery v pevné fázi lze získat krystalizaci za určitých podmínek. Při krystalizaci z methanolu se vytvářejí krystaly α-D-glukopyranózy, zatímco při krystalizaci z kyseliny octové krystaly β-D-glukopyranózy. Při krystalizaci z vodného roztoku obvykle vzniká monohydrát D-glukózy. V zelených rostlinách vzniká procesem fotosyntézy z oxidu uhličitého a vody za přítomnosti chlorofylu a dodávky energie ve formě světelných kvant podle sumární rovnice
- 6 CO2 + 12 H2O + hν → C6H12O6 + 6 O2 + 6 H2O,
přičemž vzniká kyslík. Přesně opačným procesem je proces, kterým organismy rostlin a živočichů odbourávají („spalují“) D-glukózu na původní látky a získávají tak potřebnou energii.
Obecně o chemických vlastnostech a reakcích viz též heslo aldóza.
Výskyt v přírodě
Čistá D-glukóza se nachází v rostlinách jako jeden z produktů fotosyntézy a představuje pro rostliny zásobu energie. Hromadí se především v plodech. Kromě toho je podjednotkou řady přírodních oligosacharidů, např. maltózy, sacharózy, laktózy aj. a polysacharidů, např. škrobu nebo glykogenu. Obecně se tyto glukózové sacharidy nazývají glukany. Je také součástí mnoha heteroglykosidů, vyskytujících se v rostlinách.
Je také přítomna v krvi živočichů, i v některých živočišných produktech, zejména v medu. Člověk s cukrovkou má více glukózy v moči.
Fyziologický význam
D-Glukóza je nezbytná pro fungování lidského těla; je základním a nejrychlejším zdrojem energie pro všechny tělesné tkáně. Pro některé lidské buňky, zejména pro červené krvinky, je glukóza jediným zdrojem energie, bez kterého se neobejdou. Tyto tkáně spotřebují za 24 hodin přibližně 150 g glukózy. Je-li příjem v potravě nižší nebo nerovnoměrný, chybějící glukózu získává organizmus štěpením zásobního glykogenu procesem glykogenolýzy. Při poklesu hladiny glukózy se ze žláz s vnitřní sekrecí (z pankreatu a nadledvin) začnou uvolňovat kontraregulační hormony (glukagon a adrenalin), které mobilizují její tvorbu. Glykogen je uložen především v játrech a také ve svalstvu v množství od 150 do 400 g, podle situace, ve které se organizmus nalézá. V případě, že jsou zásoby glykogenu vyčerpány, vytváří si organizmus nezbytné množství glukózy přeměnou tělesného tuku pomocí glukoneogeneze. Při stresu a při delším hladovění se jako zdroj pro tvorbu glukózy využívá také bílkovin ze svalů i za cenu oslabování jejich funkce.
- Využitelná energie na 100 g glukózy je 1670 kJ.
- Koncentrace (hladina) D-glukózy v krvi se nazývá glykemie.
- Z biochemického hlediska je aktivní formou D-glukózy glukóza-6-fosfát, vznikající z ní působením adenosintrifosfátu (ATP).
Použití

Kromě již zmíněného použití v lékařství je surovinou pro fermentační výrobu ethanolu a alkoholických nápojů (pivo, víno atp.) alkoholovým kvašením působením kvasinek rodu Saccharomyces. Působením jiných mikroorganismů lze vyrábět i jiné důležité organické sloučeniny, jako butan-1-ol , glycerol, aceton, kyselinu mléčnou, kyselinu citronovou aj.
Enzymaticky se z ní vyrábí mnohem sladší monosacharid fruktóza, která se používá v potravinářském průmyslu.
Využívá se také jako umělá výživa (kapačky).
Odkazy
Reference
- SASAJIMA, Ken-Ichi, Sinskey, Anthony J. Oxidation of l-glucose by a Pseudomonad. Biochimica et Biophysica Acta (BBA) - Enzymology. 1979-11-01, roč. 571, čís. 1, s. 120–126. DOI 10.1016/0005-2744(79)90232-8.
- A Natural Way to Stay Sweet. [s.l.]: NASA Dostupné v archivu pořízeném dne 2005-01-06. (anglicky).
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu glukóza na Wikimedia Commons
Obrázky, zvuky či videa k tématu glukóza na Wikimedia Commons  Slovníkové heslo glukóza ve Wikislovníku
Slovníkové heslo glukóza ve Wikislovníku Encyklopedické heslo Glukosa v Ottově slovníku naučném ve Wikizdrojích
Encyklopedické heslo Glukosa v Ottově slovníku naučném ve Wikizdrojích