Kyselina oxaloctová
Kyselina oxaloctová (známa aj ako OAA, z anglického oxaloacetic acid) je kryštalická organická zlúčenina, ktorej vzorec je HO2CC(O)CH2CO2H. Konjugovaná báza kyseliny oxaloctovej, nazývaná oxalacetát alebo oxaloctan, je metabolickým medziproduktom v mnohých procesoch u živočíchov a rastlín. Účastní sa glukoneogenézy, močovinového cyklu, glyoxylátového cyklu, syntézy aminokyselín, syntézy mastných kyselín a citrátového cyklu.[1]
| Kyselina oxaloctová | |||
 Kyselina oxaloctová | |||
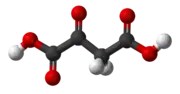 Kyselina oxaloctová | |||
| Všeobecné vlastnosti | |||
| Sumárny vzorec | C4H4O5 | ||
| Synonymá | kyselina 2-oxobutándiová, 2-oxosukcinát, 2-ketosukcinát | ||
| Fyzikálne vlastnosti | |||
| Molárna hmotnosť | 132,07 g/mol | ||
| Teplota topenia | 161 °C | ||
| Termochemické vlastnosti | |||
| Štandardná zlučovacia entalpia | -943,21 kJ/mol | ||
| Ďalšie informácie | |||
| Číslo CAS | 328-42-7 | ||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||
Vlastnosti
Kyselina oxaloctová je dikarboxylová ketokyselina. Postupne sa deprotonuje za vzniku dianiónu:
- HO2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2H + H+, pKa = 2.22
- −O2CC(O)CH2CO2H ⇌ −O2CC(O)CH2CO2− + H+, pKa = 3.89
Pri vysokom pH sa ionizuje i enolizovateľný protón:
- −O2CC(O)CH2CO2− ⇌ −O2CC(O−)CHCO2− + H+, pKa = 13.03
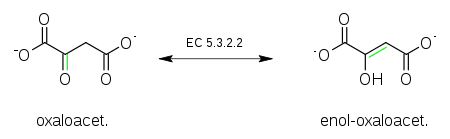
Enol formy kyseliny oxaloctovej sú veľmi stabilné, dokonca má každý z nich iný bod topenia (152 °C pre cis izoformu a 184 °C pre trans izoformu). Reakcia je katalyzovaná oxalacetáttautomerázou. trans-enol-oxalacetát vzniká i pôsobením fumarázy na kyselinu vínnu.[2]
Biosyntéza
Oxalacetát sa v prírode vytvára niekoľkými spôsobmi. Hlavným spôsobom je oxidácia L-malátu, ktorá je katalyzovaná malátdehydrogenázou v citrátovom cykle. Malát sa takisto oxiduje sukcinátdehydrogenázou za vzniku enol-oxalacetátu, reakcia je však pomalá.[3]
Takisto vzniká kondenzáciou pyruvátu s kyselinou uhličitou poháňanou hydrolýzou ATP:
- CH3C(O)CO2− + HCO3− + ATP → −O2CCH2C(O)CO2− + ADP + Pi
Táto reakcia prebieha v listovom mezofyle rastlín. Jej medziproduktom je fosfoenolpyruvát a katalyzuje ju fosfoenolpyruvátkarboxyláza.
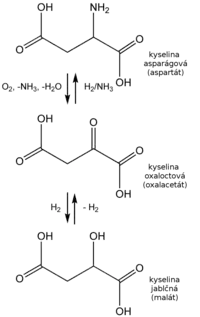
Oxalacetát môže vznikať i transamináciou či deamináciou kyseliny asparágovej.
Biochemický význam
Oxalacetát je intermediátom v citrátovom cykyle, kde reaguje s acetylkoenzýmom A za vzniku citrátu (kyseliny citrónovej). Reakciu katalyzuje citrátsyntáza. Takisto sa nachádza v glukoneogenéze, glyoxylátovom cykle, syntézy aminokyselín a syntézy mastných kyselín. Oxalacetát je silný inhibítor komplexu II (sukcinátdehydrogenázy).
Glukoneogenéza
Glukoneogenéza[1] je metabolická dráha, ktorej výsledkom je glukóza syntetizovaná z látok iných, než sacharidov. Začiatok tohto procesu prebieha v mitochondriálnej matrix, kde sa nachádzajú molekuly pyruvátu. Pyruvát je karboxylovaný pomocou pyruvátkarboxylázy aktivovanej molekulami ATP a vodou. V tejto reakci vyzniká oxalacetát. Ten je následne redukovaný pomocou NADH za vzniku malátu. Vďaka tejto zmene je možný transport molekuly mimo mitochondrie. Až je malát v cytozole, oxiduje sa naspäť na oxalacetát pomocou NAD+. Oxalacetát ostáva v cytozole, kde následne prebehne zvyšok reakcií glukoneogenézy. Oxalacetát je dekarboxylovaný a fosforylovaný pomocou fosfoenolpyruvátkarboxykinázy, pričom z neho vzniká 2-fosfoenolpyruvát. Zdrojom fosfátu je GTP (guanozíntrifosfát). Ďalším sledom reakcií, väčšinou zhodných s glykolýzou (ale v opačnom smere) sa získa glukóza.
Močovinový cyklus
Močovinový cyklus je metabolická dráha, ktorá vedie k tvorbe močoviny z dvoch molekúl amoniaku a jednej molekuly uhličitanu.[1] Tento proces bežne prebieha v hepatocytoch (bunkách pečene). Reakcie súvisiace s močovinovým cyklom produkujú NADH, ktorý je možné vyprodukovať dvomi spôsobmi. Jeden z nich využíva oxalacetát. V cytozole sú prítomné molekuly fumarátu, ktorý je možné premeniť na malát pomocou fumarázy. Malát sa následne premení na oxalacetát pomocou malátdehydrogenázy, pričom vzniká NADH. Vzniknutý oxalacetát sa recykluje a vzniká aspartát, keďže transaminázy preferujú ketokyseliny ako svoj strubstrát. Tým je zároveň zariadený prívod dusíku do bunky. Aspartát sa takisto účastní močovinového cyklu.
Glyoxylátový cyklus
Glyoxylátový cyklus je variant citrátového cyklu.[4] Je to anabolická dráha prebiehajúca v rastlinách a baktériách využívajúca enzýmy izocitrátlyáza a malátsyntáza. Niektoré medzikroky cyklu sú odlišné oproti citrátovému cyklu, oxalacetát má však v oboch cykloch rovnakú funkciu.[1] Oxalacetát teda reaguje ako prvý reaktant a vzniká ako posledný produkt i v glyoxylátovom cykle. Celkovým ziskom v glyoxylátovom cykle je vlastne jedna molekula oxalacetátu, pretože do cyklu vstupujú dve molekuly acetylkoenzýmu A.
Syntéza mastných kyselín
Počas syntézy mastnej kyseliny je acetylkoenzým A presunutý z mitochondrie do cytoplazmy, kde sa nachádza enzým syntáza mastných kyselín. Acetylkoenzým A je transportovaný z matrixu mitochondrie v podobe citrátu, ktorý vzniká reakciou acetylkoenzýmu A s oxalacetátom. Táto reakcia je zvyčajne prvou reakciou citrátového cyklu, ale ak nie je nutný zisk energie, tak sa citrát presúva do cytoplazmy, kde sa opäť rozkladá na acetylkoenzým A a oxalacetát. Vďaka tomu môže začať syntéza mastných kyselín.
Iná časť cyklu využíva NADPH na syntézu mastných kyselín.[5] Časť tohto redukčného činidla sa získava pri presune oxalacetátu z cytozolu do mitochondrie, pričom vnútorná vrstva mitochondrie nesmie byť pre oxalacetát priepustná. Oxalacetát sa najprv redukuje na malát pomocou NADH a malát sa potom dekarboxyluje na pyruvát. Pyruvát môže prejsť do mitochondrie, kde sa opäť karboxyluje (za účasti uhličitanu) na oxalacetát pomocou pyruvátkarboxylázy.
Týmto spôsobom je počas presunu acetylkoenzýmu A z mitochondrie do cytoplazmy produkovaná molekula NADH. Celkovou reakciou, ktorá je spontánna, je teda:
- HCO3– + ATP + acetyl-CoA → ADP + Pi + malonyl-CoA
Syntéza aminokyselín
Štyri esenciálne aminokyseliny a dve neesenciálne aminokyseliny sú syntetizované z oxalacetátu.[6] Z oxalacetátu sa transamináciou tvorí aspartát pomocou aspartátaminotransferázy. Z aspartátu sú následne syntetizované asparagín, metionín, lyzín a treonín. Z treonínu sa ďalej môže syntetizovať izoleucín. Bez oxalacetátu by teda syntéza týchto aminokyselín vôbec nemohla prebehnúť, keďže sa z neho syntetizuje aspartát.

Referencie
- NELSON, David L.; COX, Michael M.. Principles of Biochemistry. 4th. vyd. New York : W. H. Freeman, 2005. ISBN 0-7167-4339-6.
- VAN VUGT-LUSSENBURG, Barbara M. A.; VAN DER WEEL, Laura; HAGEN, Wilfred R.. Biochemical Similarities and Differences between the Catalytic [4Fe-4S] Cluster Containing Fumarases FumA and FumB from Escherichia coli. PLoS ONE, 2013-02-06, roč. 8, čís. 2, s. e55549. Dostupné online [cit. 2021-02-27]. ISSN 1932-6203. DOI: 10.1371/journal.pone.0055549. (po anglicky)
- Direct demonstration of enol-oxaloacetate as an immediate product of malate oxidation by the mammalian succinate dehydrogenase. FEBS Letters, 1991, s. 76–78. DOI: 10.1016/0014-5793(91)80944-X.
- Welcome to The Chemistry Place [online]. . Dostupné online.
- fatty acids synthesis [online]. http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb2/part1/fasynthesis.htm.
- http://faculty.ksu.edu.sa/69436/Documents/lecture-15-aa_from_oxaloacetate_and_pyruvate.pptx [online]. . Dostupné online.
- Gadd, Geoffrey M. "Fungal production of citric and oxalic acid: importance in metal speciation, physiology and biogeochemical processes" Advances in Microbial Physiology (1999), 41, 47-92.
- Xu, Hua-Wei. "Oxalate accumulation and regulations is independent of glycolate oxidase in rice leaves" Journal of Experimental Botany, Vol 57, No. 9 pp. 1899-1908, 2006
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Oxaloacetic acid na anglickej Wikipédii.