Kyselina m-chlorperoxybenzoová
Kyselina meta-chlorperoxybenzoová (též kyselina m-chlorperoxybenzoová) je karboxylová peroxokyselina často používaná v organické syntéze jako oxidační činidlo. Obvykle se upřednostňuje před ostatními peroxokyselinami, protože se snáze skladuje. Mezi hlavní způsoby jejího použití patří přeměna ketonů na estery (Baeyerova-Villigerova oxidace), epoxidace alkenů (Priležajevova reakce), přeměna silylenoletherů na silyl α-hydroxyketony (Rubottomova oxidace), oxidace thioetherů na sulfoxidy a sulfony a oxidace aminů na aminoxidy.[2] Je to silné oxidační činidlo, které při styku s hořlavými látkami může způsobit požár.
| Kyselina m-chlorperoxybenzoová | |
|---|---|
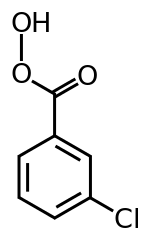
Strukturní vzorec | |
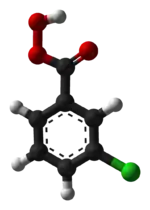
Model molekuly | |
| Obecné | |
| Systematický název | kyselina 3-chlorbenzenkarboperoxová |
| Ostatní názvy | Kyselina 3-chlorperoxybenzoová, kyselina meta-chlorperoxybenzoová |
| Anglický název | meta-Chloroperoxybenzoic acid |
| Sumární vzorec | C7H5ClO3 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 937-14-4 |
| EC-no (EINECS/ELINCS/NLP) | 213-322-3 |
| PubChem | 70297 |
| SMILES | ClC1=CC(C(OO)=O)=CC=C1 |
| InChI | 1/C7H5ClO3/c8-6-3-1-2-5(4-6)7(9)11-10/h1-4,10H |
| Vlastnosti | |
| Molární hmotnost | 172,57 g/mol |
| Teplota rozkladu | 92 až 94 °C (365 až 367 K) |
| Disociační konstanta pKa | 7,57 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H226 H314 H318 H335 |
| P-věty | P210 P220 P233 P234 P240 P241 P242 P243 P260 P261 P264 P271 P272 P280 P301+330+331 P302+352 P303 P304+340 P305+351+338 P310 P312 P321 P332+313 P333+313 P337+313 P361 P353 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava
Kyselina m-chlorperoxybenzoová se dá připravit reakcí m-chlorbenzoylchloridu s peroxidem vodíku za přítomnosti síranu hořečnatého, hydroxidu sodného a 1,4-dioxanu a následným okyselením.
Dostupnost a čistota
Jako čistá látka může kyselina m-chlorperoxybenzoová vybouchnout při nárazu nebo dotekem s jiskrami. Z tohoto důvodu se prodává jako méně než 72% směs.[2] Peroxykyselina může být přečištěna promytím komerčního materiálu mírně zásaditým pufrem a následným sušením.[3] Peroxykyseliny jsou obecně o něco slabší než odpovídající karboxylové kyseliny a tak lze zvýšit jejich čistotu opatrným pozměněním pH. Čistá kyselina je dostatečně odolná vůči rozkladu, pokud je skladována při nízkých teplotách v plastových nádobách.
V případech, kdy musí být známa přesná koncentrace kyseliny meta-chlorperoxybenzoové, může být vzorek titrován za účelem zjištění přesné koncentrace aktivního oxidačního činidla.
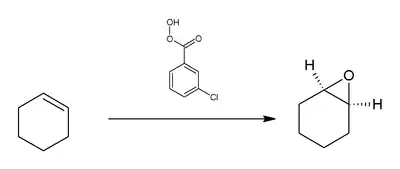
Příklad reakce
Na následujícím obrázku je znázorněna reakce kyseliny cyklohexenu s kyselinou meta-chlorperoxybenzoovou za vzniku epoxidu:
Cis nebo trans izomerie alkenového výchozího materiálu zůstává zachována.
Reference
V tomto článku byl použit překlad textu z článku meta-Chloroperoxybenzoic acid na anglické Wikipedii.
- 3-Chloroperoxybenzoic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- 3-Chloroperoxybenzoic acid [online]. Organic Chemistry Portal. Dostupné online. (anglicky)
- Armarego, W. L. F.; PERRIN, D. D. Purification of Laboratory Chemicals. 4th. vyd. Oxford: Butterworth-Heinemann, 1996. ISBN 0-7506-3761-7. S. 145. (anglicky)