Chlordifenylfosfin
Chlordifenylfosfin je organická sloučenina se vzorcem (C6H5)2PCl, zkracovaným do podoby Ph2PCl. Jedná se o bezbarvou kapalinu se zápachem podobným česneku, zachytitelným i při koncentracích v řádu 10−7 %. Používá se na zavádění skupin Ph2P do sloučenin, například při tvorbě ligandů.[2] Podobně jako ostatní halogenfosfiny reaguje Ph2PCl s mnoha nukleofily, jako je voda, a také je snadno oxidovatelný, dokonce i na vzduchu.
| Chlordifenylfosfin | |
|---|---|

Strukturní vzorec | |
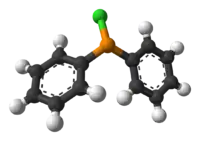
Model molekuly | |
| Obecné | |
| Systematický název | chlorid difenylfosforitý |
| Funkční vzorec | (C6H5)2PCl |
| Sumární vzorec | C12H10PCl |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 1079-66-9 |
| EC-no (EINECS/ELINCS/NLP) | 214-093-2 |
| PubChem | 66180 |
| SMILES | ClP(c1ccccc1)c2ccccc2 |
| InChI | 1S/C12H10ClP/c13-14(11-7-3-1-4-8-11)12-9-5-2-6-10-12/h1-10H |
| Vlastnosti | |
| Molární hmotnost | 256,09 g/mol |
| Teplota varu | 320 °C (593 K) |
| Hustota | 1,229 g/cm3 |
| Rozpustnost ve vodě | reaguje |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v ethanolu a tetrahydrofuranu |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v benzenu a etherech |
| Bezpečnost | |
| [1] | |
| H-věty | H290 H302 H314 H318 H412[1] |
| P-věty | P234 P260 P264 P270 P273 P280 P301+312 P301+330+331 P303+361+353 P304+340 P305+351+338 P310 P321 P330 P363 P390 P404 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Výroba a reakce
Chlordifenylfosfin se vyrábí z benzenu a chloridu fosforitého. Benzen reaguje s chloridem fosforitým za teploty kolem 600 °C, čímž se vytváří dichlorfenylfosfin (PhPCl2) a HCl. Redistribucí plynného PhPCl2 za vysoké teploty vzniká poté chlorodifenylfosfin.[2][3]
- 2 PhPCl2 → Ph2PCl + PCl3
Lze také použít redistribuční reakci, kde jsou výchozími látkami chlorid fosforitý a trifenylfosfin:
- PCl3 + 2 PPh3 → 2 Ph2PCl
Chlordifenylfosfin se hydrolyzuje na difenylfosfinoxid. Redukcí sodíkem vzniká tetrafenyldifosfin:
- 2 Ph2PCl + 2 Na → [Ph2P]2 + 2 NaCl
Použití
Chlorodifosfin se, podobně jako další chlorfosfiny, používá na přípravu různých fosfinů. Často se přitom nechává reagovat s Grignardovými činidly:[3]
- Ph2PCl + MgRX → Ph2PR + MgClX
Fosfiny vytvořené reakcemi s Ph2PCl mohou dále reagovat, výsledné produkty mohou být využity například jako pesticidy (například EPN), stabilizátory plastů (Sandostab P-EPQ), katalyzátory a zpomalovače hoření (sem patří mimo jiné cyklický anhydrid kyseliny fosfinokarboxylové), díky čemuž je Ph2PCl významným průmyslovým meziproduktem.[2][3]
Příprava difenylfosfidových sloučenin
Chlordifenylfosfin se používá k přípravě difenylfosfidu sodného reakcí se sodíkem v 1,4-dioxanu.[4]
- Ph2PCl + 2 Na → Ph2PNa + NaCl
Difenylfosfin lze získat reakcí Ph2PCl a hydridu lithno-hlinitého; ten se obvykle používá v přebytku.
- 4 Ph2PCl + LiAlH4 → 4 Ph2PH + LiCl + AlCl3
Ph2PNa i Ph2PH se také používají na přípravu fosfinových ligandů.
Charakterizace
Čistota Ph2PCl se často zkoumá pomocí 31P NMR spektroskopie.[6]
| Sloučenina | 31P chemický posuv
(ppm vs 85% H3PO4) |
|---|---|
| PPh3 | −6 |
| PPh2Cl | 81,5 |
| PPhCl2 | 165 |
| PCl3 | 218 |
Reference
V tomto článku byl použit překlad textu z článku Chlorodiphenylphosphine na anglické Wikipedii.
- https://pubchem.ncbi.nlm.nih.gov/compound/66180
- Quin, L. D. A Guide to Organophosphorus Chemistry; Wiley IEEE: New York, 2000; pp 44-69. ISBN 0-471-31824-8
- Svara, J.; Weferling, N.; Hofmann, T. "Phosphorus Compounds, Organic," In 'Ullmann's Encyclopedia of Industrial Chemistry, 7th ed.; Wiley-VCH: 2008; DOI:10.1002/14356007.a19_545.pub2; Accessed: February 18, 2008.
- Jackson W. Roy; R. J. Thomson; M. F. MacKay. The Stereochemistry of Organometallic Compounds. XXV. The Stereochemistry of Displacements of Secondary Methanesulfonate and p-Toluene-sulfonate esters by Diphenylphosphide Ions. X-ray Crystal Structure of (5α-Cholestan-3α-yl)diphenylphosphine Oxide. Australian Journal of Chemistry. 1985, s. 111–118. DOI 10.1071/CH9850111.
- Valeria A. Stepanova; Valery V. Dunina; Irina P. Smoliakova. Reactions of Cyclopalladated Complexes with Lithium Diphenylphosphide. Organometallics. 2009, s. 6546–6558. DOI 10.1021/om9005615.
- O. Kühl "Phosphorus-31 NMR Spectroscopy" Springer, Berlin, 2008. ISBN 978-3-540-79118-8

