Síran olovnatý
Síran olovnatý (PbSO4) je bílý krystalický síran dvoumocného olova. Triviálně se označuje jako olověná běloba (nezaměňovat s olovnatou bělobou). Síran olovnatý se přírodě vyskytuje jako minerál anglesit.
| Síran olovnatý | |
|---|---|
_sulfate.jpg.webp) | |
 | |
| Obecné | |
| Systematický název | Síran olovnatý |
| Triviální název | olověná běloba |
| Anglický název | Lead(II) sulfate |
| Německý název | Blei(II)-sulfat |
| Sumární vzorec | PbSO4 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 7446-14-2 |
| EC-no (EINECS/ELINCS/NLP) | 258-142-6 |
| Indexové číslo | 082-001-00-6 |
| SMILES | [O-]S(=O)(=O)[O-].[PbH4+2] |
| InChI | 1S/H2O4S.Pb.4H/c1-5(2,3)4;;;;;/h(H2,1,2,3,4);;;;;/q;+2;;;;/p-2 |
| Vlastnosti | |
| Molární hmotnost | 303,26 g/mol |
| Teplota tání | 1 170 °C (rozklad) |
| Teplota změny krystalové modifikace | 866 °C (α → β) |
| Hustota | 6,35 g/cm³ |
| Index lomu | nDa= 1,877 1 nDb= 1,877 1 nDc= 1,877 1 |
| Tvrdost | 2,5–3 |
| Rozpustnost ve vodě | 0,004 2 g/100 g (25 °C) 0,005 7 g/100 g (40 °C) |
| Rozpustnost v polárních rozpouštědlech |
konc. kyselina sírová |
| Součin rozpustnosti | 1,51×10−8 |
| Relativní permitivita εr | 14,3 |
| Struktura | |
| Krystalová struktura | kosočtverečná (α) jednoklonná (β) |
| Hrana krystalové mřížky | a= 851,6 pm b= 539,9 pm c= 698,7 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −919,94 kJ/mol |
| Entalpie tání ΔHt | 132 J/g |
| Entalpie varu ΔHv | 198 J/g |
| Standardní molární entropie S° | 148,49 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −813,20 kJ/mol |
| Izobarické měrné teplo cp | 0,340 3 JK−1g−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H360Df
H332 H302 H373 H410 |
| R-věty | R61, R20/22, R33, R50/53, R62 |
| S-věty | S53, S45, S60, S61 |
| NFPA 704 |  0
3
0
|
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Vlastnosti
Tento síran je nerozpustný ve vodě a v alkoholech, na druhou stranu se poměrně dobře rozpouští v chlorovodíkové a v dusičné kyselině, stejně jako v kyselině sírové (lépe v koncentrovanější). Také se rozpouští v hydroxidu sodném a v roztocích amonných solí. Síran olovnatý tvoří jako minerál jednoklonné nebo kosočtverečné krystaly.[2]
Ačkoliv ho autoři v 19. století považovali za neškodný, je to toxická látka, nebezpečná zejména v případě, kdy dojde k vdechnutí nebo polknutí prachu síranu olovnatého. Je to kumulativní jed, hromadí se v těle a způsobuje otravu olovem. Zejména jeho využití v divadelnich šminkách, kde se používal, protože ve směsi s olejem nepodporuje jeho vysychání, bylo velmi nebezpečné. Také malířská barviva založená na této látce jsou tedy nebezpečná.[3] Vzniká při vybíjení v olověných akumulátorech v automobilech.
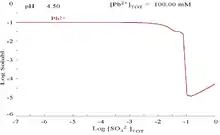
Příprava
Tato látka se dá vyrobit z vodného roztoku obsahujícího rozpuštěnou olovnatou sůl (např. dusičnan), pokud do roztoku přidáme kyselinu sírovou. Síran olovnatý však vzniká i reakcí oxidu, hydroxidu nebo uhličitanu olovnatého právě s kyselinou sírovou.[2]
Reference
- Lead sulfate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- PATNAIK, Pradyot. Handbook of Inorganic Chemical Compounds. [s.l.]: McGraw-Hill, 2003. Dostupné online.
- AMIEN forum - Lead Sulfate [online]. Dostupné online.[nedostupný zdroj]
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.


