Trimethylsilyljodid
Trimethylsilyljodid, také nazývaný jodtrimethylsilan, zkráceně TMSI, je organická sloučenina křemíku, jodderivát silanu.
| Trimethylsilyljodid | |
|---|---|
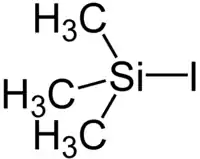
Strukturní vzorec | |
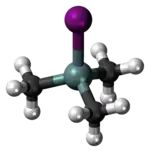
Tyčinkovo-kuličkový model molekuly | |
| Obecné | |
| Systematický název | jodtrimethylsilan |
| Ostatní názvy | trimethylsilyljodid, TMSI, Jungovo činidlo |
| Anglický název | Trimethylsilyl iodide |
| Funkční vzorec | (CH3)3SiI |
| Sumární vzorec | C3H9SiI |
| Vzhled | čirá bezbarvá těkavá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 16029-98-4 |
| PubChem | 85247 |
| SMILES | I[Si](C)(C)C |
| InChI | 1S/C3H9ISi/c1-5(2,3)4/h1-3H3 |
| Vlastnosti | |
| Molární hmotnost | 200,09 g/mol |
| Teplota varu | 106–109 °C (379–382 K) |
| Hustota | 1,406 g/cm3[1] |
| Bezpečnost | |
| [2] Nebezpečí[2] | |
| Teplota vzplanutí | −31 °C (242 K)[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava
Trimethylsilyljodid může být připraven oxdidačním štěpením hexamethyldisilanu jodem[1] nebo štěpením hexamethyldisiloxanu jodidem hlinitým[1]:
- TMS-TMS + I2 → 2 TMSI (TMS = (CH3)3Si)
- 3 TMS-O-TMS + 2 AlI3 → 6 TMSI + Al2O3
Použití
Trimethylsilyljodid se používá k zavedení trimethylsilylové skupiny do alkoholů (obecný vzorec ROH):
- ROH + TMSI → RO(TMS) + HI
Tato reakce může být užitečná pro analýzu plynovou chromatografií; vzniklý silylether je těkavější než původní látka.[3] Díky své nižší ceně se ovšem častěji používá trimethylsilylchlorid.
TMSI reaguje s alkylethery (ROR′) za vzniku silyletherů (ROSiMe3) a jodalkanů (RI), které mohou být hydrolyzovány na alkoholy (ROH).[4]
Trimethylsilyljodid se rovněž používá na odstranění tercbutoxykarbonylové chránicí skupiny,[1][5][6] hlavně tehdy, když jsou ostatní deprotekční metody pro daný substrát nevhodné.[7]
Reference
V tomto článku byl použit překlad textu z článku Trimethylsilyl iodide na anglické Wikipedii.
- OLAH, G; NARANG, S. C. Iodotrimethylsilane—a versatile synthetic reagent. Tetrahedron. 1982, s. 2225. DOI 10.1016/0040-4020(82)87002-6. (anglicky)
- Iodotrimethylsilane. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- GC/MS Analysis for Morphine and Other Opiates in Urine [online]. Dostupné online. (anglicky)
- Michael E. Jung; MARK A. LYSTER. Quantitative dealkylation of alkyl ethers via treatment with trimethylsilyl iodide. A new method for ether hydrolysis. Journal of Organic Chemistry. 1977, s. 3761–3764. DOI 10.1021/jo00443a033. (anglicky)
- Michael E. Jung; MARK A. LYSTER. Conversion of alkyl carbamates into amines via treatment with trimethylsilyl iodide. J. Chem. Soc., Chem. Commun.. 1978, s. 315–316. DOI 10.1039/C39780000315. (anglicky)
- Richard S. Lott; VIRANDER S. CHAUHAN; CHARLES H. STAMMER. Trimethylsilyl iodide as a peptide deblocking agent. J. Chem. Soc., Chem. Commun.. 1979, s. 495–496. DOI 10.1039/C39790000495. (anglicky)
- Zhijian Liu; NOBUYOSHI YASUDA; MICHAEL SIMEONE; ROBERT A. REAMER. N-Boc Deprotection and Isolation Method for Water-Soluble Zwitterionic Compounds. Journal of Organic Chemistry. 2014, s. 11792–11796. DOI 10.1021/jo502319z. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Trimethylsilyljodid na Wikimedia Commons
Obrázky, zvuky či videa k tématu Trimethylsilyljodid na Wikimedia Commons

