Imidoylchloridy
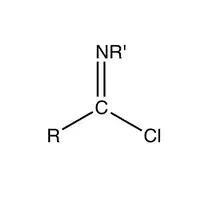
Imidoylchloridy jsou organické sloučeniny, jejichž molekuly obsahují funkční skupiny s obecným vzorcem RC(NR')Cl, přičemž mezi R'N a uhlíkatým centrem je dvojná vazba. Jedná se o analogy acylchloridů. Imidoylchloridy se vyznačují vysokou reaktivitou a obvykle se objevují jako meziprodukty různých syntetických postupů. K reakcím, při kterých se tvoří imidoylchloridy, patří Gattermannova syntéza aldehydů, Houbenova-Hoeschova syntéza ketonů a Beckmannův přesmyk. Svými chemickými vlastnostmi se podobají enaminům.[1] Mnoho chlorovaných N-heterocyklických sloučenin, jako například 2-chlorpyridin a 2, 4, a 6-chlorpyrimidiny, formálně patří mezi imidoylchloridy.
Příprava a vlastnosti
Imidoylhalogenidy se připravují reakcemi amidů s halogenačními činidly. Na výsledek reakce má velký vliv struktura amidu. Imidoylchlorid je možné získat z monosubstituovaného amidu a fosgenu[1]:
- RC(O)NHR’ + COCl2 → RC(NR’)Cl + HCl + CO2
Lze také použít thionylchlorid.[2]
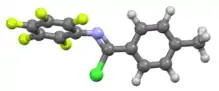
Imidoylchloridy jsou obvykle bezbarvé kapaliny s nízkými teplotami tání citlivé na teplo a vlhkost. V jejich infračervených spektrech se nacházejí νC=N pásy mezi 1650 a 1689 cm−1. I když mohou mít syn- i anti-izomery, tak většinou zaujímají anti konfiguraci.[1]
Reaktivita
Imidoylchloridy reagují s vodou, sulfanem, aminy a halogenovodíky. S vodou vytvářejí příslušné amidy:
- RC(NR’)Cl + H2O → RCONHR’ + HCl
Alifatické imidoylchloridy jsou k hydrolýze náchylnější než arylové. Rychlost reakce snižují substituenty odtahující elektrony.
Reakcemi imidoylchloridů se sulfanem vznikají thioamidy:[1]
- RC(NR’)Cl + H2S → RC(S)NHR’ + HCl
Reakcemi s aminy se tvoří amidiny.[1]
- RC(NR’)Cl + 2R”NH2 → RC(NR’)NHR” + R”NH3Cl
Pokud jsou skupiny R' a R" odlišné, mohou vznikat dva různé izomery.
Zahříváním imidoylchloridů dochází k jejich dehydrohalogenaci na nitrily:[1]
- RC(NR’)Cl → RC≡N + R’Cl
Působením halogenovodíků, například HCl, na imidoylchloridy se vytváří iminiumhalogenidové kationty:[1]
- RC(NR’)Cl + HCl → [RC(NHR’)Cl]+Cl−
Využití
Imidoylchloridy slouží jako meziprodukty při syntéze některých organických sloučenin, jako jsou karboximidáty, thioimidáty, amidiny a imidoylkyanidy. Při těchto syntézách dochází k nahrazení chloridu jinými funkčními skupinami, například alkoholovými, thiolovými, aminovými či kyanátovými.[1] Imidoylchloridy mohou také vstupovat do Friedelových–Craftsových reakcí, kde slouží k navázání iminových skupin na aromatické substráty. Pokud jsou na dusíkový atom imidoylchloridu navázány dva substituenty, tak je vzniklý chloriminiový ion náchylný k reakcím s aromatickými kruhy i za nepřítomnosti Lewisovy kyseliny; tato reakce se nazývá Vilsmeierova–Haackova reakce, chloriminiové ionty bývají označovány jako Vilsmeierova činidla.[4][5][6]
Po navázání iminiového iontu může být vzniklá funkční skupina hydrolyzována na karbonylovou za účelem dalších reakcí. Vilsmeierova-Haackova reakce je tak užitečným nástrojem k přidávání funkčních skupin na aromatické kruhy obsahující skupiny odtahující elektrony, jež ztěžují provedení Friedelovy-Craftsovy reakce.
Imidoylchloridy lze snadno halogenovat na α uhlíku.[1] Reakce imidoylchloridů s halogenovodíky mívají za následky nahrazení všech α vodíků halogenidy. Tento postup je vhodný k halogenaci mnoha různých sloučenin. Imidoylchloridy lze též použít k vytváření peptidových vazeb tvorbou amidinů a jejich hydrolýzou na amidy. Takto je možné získat syntetické proteiny.[1]
Imidoylchloridy se obtížně skladují. Snadno reagují s vodou, v důsledku čehož je jejich izolace, stejně jako dlouhodobé skladování, náročná. Navíc u nich při vyšších teplotách dochází, pokud molekuly obsahují skupiny CH, k autokondenzačním reakcím. Při ještě vyšších teplotách může nastat odštěpení chloru, vedoucí ke vzniku nitrilu. Z těchto důvodů se imidoylchloridy obvykle připravují těsně před použitím. Jako stabilnější, a tedy lépe využitelné, meziprodukty byly navrženy například imidoylbenzotriazoly.[7]
Reference
V tomto článku byl použit překlad textu z článku Imidoyl chloride na anglické Wikipedii.
- Ulrich, H. The Chemistry of Imidoyl Halides; Plenum Press: New York, 1968; pp. 55–112.
- Arthur C. Hontz; E. C. Wagner. N,N'-Diphenylbenzamidine. Organic Syntheses. 1951, s. 48. DOI 10.15227/orgsyn.031.0048.
- T. D. Petrova, I. V. Kolesnikova, V. I. Mamatyuk, V. P. Vetchinov, V. E. Platonov, I. Yu. Bagryanskaya, Yu. V. Gatilov. Izv. Akad. Nauk SSSR, Ser. Khim.. 1993, s. 1605.
- Anton Vilsmeier; Albrecht Haack. Über die Einwirkung von Halogenphosphor auf Alkyl-formanilide. Eine neue Methode zur Darstellung sekundärer und tertiärer p-Alkylamino-benzaldehyde. Berichte der Deutschen Chemischen Gesellschaft zu Berlin. 1927, s. 119–122. DOI 10.1002/cber.19270600118.
- O. Meth-Cohn; S. P. Stanforth. The Vilsmeier–Haack Reaction (Review). Comprehensive Organic Synthesis. 1991, s. 777–794. DOI 10.1016/B978-0-08-052349-1.00049-4.
- CAMPAIGNE, E.; ARCHER, W. L. Formylation of dimethylaniline. Org. Synth.. S. 27. Dostupné online. DOI 10.15227/orgsyn.033.0027. (anglicky); Coll. Vol.. S. 331. (anglicky)
- Katritzky, A. R.; Stevens, C. V.; Zhang, G.-F.; Jiang, J.; Kimpe, N. D. Heterocycles 1995, 40, 231.