Hydrosilylace
Hydrosilylace je chemická reakce, při níž se za přítomnosti katalyzátoru připojuje vazba Si-H na násobnou vazbu;[1] substráty jsou obvykle nenasycené organické sloučeniny. Z alkenů vznikají alkyl- a z alkynů vinylsilany. U aldehydů a ketonů jsou produkty silylethery. Hydrosilylace bývá považována za „nejvýznamnější způsob využití platiny k homogenní katalýze“.[2]
Mechanismus
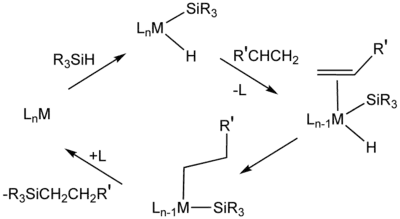
Hydrosilylace alkenů je významným způsobem přípravy organokřemičitých sloučenin. Reakční mechanismus je podobný jako u hydrogenace alkenů a často se i používají podobné katalyzátory.
Hydrosilylační reakce probíhají převážně Chalkovým-Harrodovým mechanismem, kdy se utváří kovový komplex obsahující hydridovou skupinu, silylový ligand (R3Si) a alken, který je substrátem. Poté probíhá oxidační adice, jejímž meziproduktem je komplex silanu a přechodného kovu, v němž jsou ještě přítomny některé vazby Si-H.
Hydrosilylace alkenů většinou probíhá proti Markovnikovovu pravidlu, takže se křemík při hydrosilylaci koncového alkenu nejčastěji navazuje na koncový uhlík; byly však také popsány hydrosilylace, které probíhaly v souladu s Markovnikovovým pravidlem. V některých případech se tvoří vinyl- nebo allylsilany beta-hydridovou eliminací.[3]
Hydrosilylaci (probíhající podobným mechanismem) lze provést i u alkynových substrátů, příkladem může být adice triethylsilanu na difenylacetylen:[4]
- (C2H5)3SiH + (C6H5)C≡C(C6H5) → (C2H5)3Si(C6H5)C=CH(C6H5)
Asymetrická hydrosilylace
Z chirálních fosfinových ligandů lze připravit katalyzátory pro asymetrickou hydrosilylaci; příkladem je reakce trichlorsilanu se styrenem za vzniku 1-fenyl-1-(trichlorsilyl)ethanu:
- Cl3SiH + C6H5CH=CH2 → (C6H5)(CH3)CHSiCl3
Pomocí katalyzátorů založených na palladiu a binaftylovaných monofosfinových ligandech lze dosáhnout téměř dokonale enantioselektivní hydrosilylace.[5]
Povrchová silylace
Křemíkové wafery mohou být pomocí kyseliny fluorovodíkové zbaveny zbytků oxidu křemičitého, čímž se také vytvoří křemíkové řetězce zakončené vodíkem. Na takto upravených površích mohou být provedeny hydrosilylační reakce s nenasycenými sloučeninami (jako jsou koncové alkeny a alkyny) za tvorby stabilních monovrstev.
- Si-H + H2C=CH(CH2)7CH3 → Si-CH2CHH-(CH2)7CH3
Hydrosilylace zde může být iniciována ultrafialovým zářením při pokojové teplotě a nebo zahřátím (obvykle na teploty 120 až 200 °C); přitom je potřeba suché prostředí bez přítomnosti kyslíku.
Tímto způsobem vytvořené vrstvy chrání křemík před oxidací a používají se v mnoha různých zařízeních.[6]
Katalyzátory
Před objevem platinových katalyzátorů se hydrosilylační reakce běžně neprováděly. V roce 1947 byla popsána hydrosilylace katalyzovaná peroxidy,[7] ovšem Speierův objev kyseliny chloroplatiničité znamenal velký průlom.
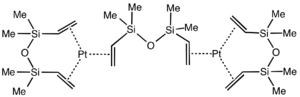
Později se začal používat Kartstedtův katalyzátor, což je lipofilní komplex rozpustný v průmyslově významných organických rozpouštědlech..[8] Při hydrosilylacích jsou často účinné i některé katalyzátory hydrogenace, jako je Wilkinsonův katalyzátor.
Reference
V tomto článku byl použit překlad textu z článku Hydrosilylation na anglické Wikipedii.
- "Hydrosilylation A Comprehensive Review on Recent Advances" B. Marciniec (ed.), Advances in Silicon Science, Springer Science, 2009. DOI:10.1007/978-1-4020-8172-9
- Ullmann's Encyclopedia of Industrial Chemistry. [s.l.]: Wiley, 2002. DOI 10.1002/14356007.a21_075. Kapitola Platinum group metals and compounds.
- D. Troegel; J. Stohrer. Recent Advances and Actual Challenges in Late Transition Metal Catalyzed Hydrosilylation of Olefins from an Industrial Point of View. Coord. Chem. Rev.. 2011, s. 1440–1459. DOI 10.1016/j.ccr.2010.12.025.
- James L. Fry, Ronald J. Rahaim Jr., Robert E. Maleczka, Jr. "Triethylsilane", Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, 2007. DOI:10.1002/047084289X.rt226.pub2
- T. Hayashi; K. Yamasaki. Comprehensive Organometallic Chemistry III. Příprava vydání Robert H. Crabtree, D. Michael P. Mingos. Amsterdam: Elsevier, 2007. ISBN 978-0-08-045047-6. DOI 10.1016/B0-08-045047-4/00140-0. Kapitola C–E Bond Formation through Asymmetric Hydrosilylation of Alkenes.
- Direct electrical detection of DNA Hybridization at DNA-modified silicon surfaces, W. Cai, J. Peck, D. van der Weide, and R. J. Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)
- L. Sommer; E. Pietrusza; F. Whitmore. Peroxide-catalyzed addition of trichlorosilane to 1-octene. Journal of the American Chemical Society. S. 188. DOI 10.1021/ja01193a508.
- C. Elschenbroich, Organometallics (2006) Wiley and Sons-VCH: Weinheim. ISBN 978-3-527-29390-2