Beta-hydridová eliminace
Beta-hydridová eliminace nebo β-hydridová eliminace je chemická reakce, ve které je alkylová skupina navázaná na kov přeměněna na odpovídající přes kov vázaný hydrid a alken.[1] U methylové skupiny tato reakce na rozdíl například od butylové skupiny neprobíhá. Aby reakce proběhla, musí mít kovový komplex volnou cis pozici vzhledem k alkylové skupině.
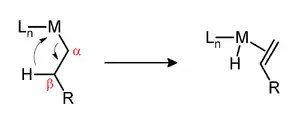
Beta-hydridová eliminace může být i neproduktivní vedlejší reakcí i produktivní reakcí.
V některých případech je β-hydridová eliminace prvním z řady kroků, například při syntéze RuHCl(CO)(PPh3)3 z chloridu ruthenitého, trifenylfosfinu a 2-methoxyethanolu alkoxidový komplexní meziprodukt reaguje β-hydridovou eliminací za vzniku hydridového ligandu a π-vázaného aldehydu, jenž se následně přeměňuje na karbonylový (CO) ligand.
Znemožnění β-hydridové eliminace
Existuje několik způsobů, jak znemožnit β-hydridovou eliminaci. Nejčastěji se používají alkylové ligandy, které nemají β-vodíková centra na první pozici, například methyl a neopentyl. β-hydridovou eliminaci je rovněž inhibována, pokud by vznikal rozvětvený alken.[2]
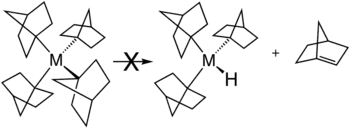
Velké alkylové ligandy jako jsou terc-butyl nebo trimethylsilyl, mohou vodíkovému atomu znemožňovat dosažení koplanární konfigurace s kovem, α a β atomy. Pokud kovové centrum nemá volná koordinační místa, například u komplexu s 18elektronovou konfigurací, pak také nemůže dojít k beta-hydridové eliminaci.
V některých případech mohou koligandy vytvářet geometrie, které zabraňují β-hydridové eliminaci. Ve výše uvedeném případě je nežádoucí β-hydridové eliminaci zabráněno použitím difosfanu, kde jsou dva atomy fosforu drženy od sebe. Jedním způsobem, jak tohoto dosáhnout, je použití speciálních ligandů jako je Xantphos. Jelikož tyto kovové komplexy vytvářejí čtvercovou rovinnou geometrii, nemůže vzniknout volná cis pozice a tedy nemůže dojít k beta-hydridové eliminaci.
Reference
V tomto článku byl použit překlad textu z článku beta-Hydride elimination na anglické Wikipedii.
- ELSCHENBROICH, C. Organometallics. Weinheim: Wiley-VCH, 2006. ISBN 978-3-527-29390-2. (anglicky)
- BOWER, Barton K.; TENNENT, Howard G. Transition metal bicyclo[2.2.1]hept-1-yls. J. Am. Chem. Soc.. 1972, s. 2512–2514. DOI 10.1021/ja00762a056. (anglicky)