Hexafluorpropan-2-ol
Hexafluorpropan-2-ol je organická sloučenina se vzorcem (CF3)2CHOH se silným zápachem. Používá se jako rozpouštědlo a meziprodukt při přípravě dalších látek. Patří mezi polární rozpouštědla a vytváří silné vodíkové vazby, díky čemuž rozpouští látky, které jsou akceptory těchto vazeb, například amidy a ethery. Je průsvitný pro ultrafialové záření.
| Hexafluorpropan-2-ol | |
|---|---|
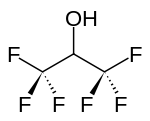
Strukturní vzorec | |
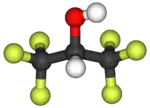
Model molekuly | |
| Obecné | |
| Systematický název | 1,1,1,3,3,3-hexafluorpropan-2-ol |
| Funkční vzorec | (CF3)2CHOH |
| Sumární vzorec | C3H2F6O |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 920-66-1 |
| PubChem | 13529 |
| SMILES | C(C(F)(F)F)(C(F)(F)F)O |
| InChI | 1/C3H2F6O/c4-2(5,6)1(10)3(7,8)9/h1,10H |
| Vlastnosti | |
| Molární hmotnost | 168,04 g/mol |
| Teplota tání | −3,3 °C (269,8 K) |
| Teplota varu | 58,2 °C (331,4 K) |
| Hustota | 1,596 g/cm3 |
| Rozpustnost ve vodě | mísitelný |
| Tlak páry | 16 kPa (20 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R20/22 R34 R41 |
| S-věty | S26 S36/37/39 S45 |
| Teplota vzplanutí | >100 °C (>373 K) |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava a použití
Hexafluorpropan-2-ol se připravuje přeměnou hexafluorpropenu na hexafluoraceton, který se následně hydrogenuje:
- (CF3)2CO + H2 → (CF3)2CHOH
Používá se jako rozpouštědlo některých polárních polymerů a jako surovina v organické syntéze.[2][3]
Velmi dobře rozpouští i polymery nerozpustné většině ostatních organických rozpouštědel, mimo jiné polyamidy, polyakrylonitrily, polyacetaly, polyestery (například polyglykolidy) a polyketony. Využití nachází rovněž v biochemii, kde zvyšuje rozpustnost peptidů a k monomerizaci shluků beta-skládaných listů. Díky své kyselosti (pKa = 9,3) může být použit na přípravu pufrů pro analýzu nukleových kyselin pomocí iontovopárové vysokoúčinné kapalinová chromatografie s hmotnostní spektrometrií.[4]
Význam v lékařství
Hexafluorpropan-2-ol může být prekurzorem i metabolitem inhalačního anestetika sevofluranu.
Bezpečnost
Hexafluorpropan-2-ol je těkavá žíravá kapalina, která může způsobit těžké popáleniny a dýchací potíže.[5]
Reference
V tomto článku byl použit překlad textu z článku Hexafluoro-2-propanol na anglické Wikipedii.
- 1,1,1,3,3,3-Hexafluoro-2-propanol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- J.-P. Bégué; D. Bonnet-Delpon; B. Crousse. Fluorinated Alcohols: A New Medium for Selective and Clean Reaction. Synlett. 2004, s. 18–29.
- Ivan A. Shuklov; Natalia V. Dubrovina; Armin Börner. Fluorinated Alcohols as Solvents, Cosolvents and Additives in Homogeneous Catalysis. Synthesis. 2007, s. 2925–2943.
- A. Apffel; J. A. Chakel; S. Fischer; K. Lichtenwalter; W. S. Hancock. Analysis of oligonucleotides by HPLC-electrospray ionization mass spectrometry. Analytical Chemistry. 1997, s. 1320–1325.
- HFIP MSDS [online]. Fisher Scientific [cit. 2018-08-18]. Dostupné v archivu pořízeném dne 2014-08-19. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Hexafluor-propan-2-ol na Wikimedia Commons
Obrázky, zvuky či videa k tématu Hexafluor-propan-2-ol na Wikimedia Commons

