Ethylmerkaptan
Ethylmerkaptan (C2H5SH) (také ethylhydrogensulfid nebo thioethanol, systematický název ethanthiol) je organická sirná sloučenina, patřící mezi thioly. Je sirnou obdobou ethanolu. Má silný, značně nepříjemný zápach, který člověk dokáže zachytit již při přítomnosti 1 molekuly ethylmerkaptanu na 2 800 000 000 molekul vzduchu (0,357 ppb). Podle Guinnessovy knihy rekordů z roku 2000 se jedná o nejintenzivněji zapáchající známou látku.[zdroj?]
| Ethylmerkaptan | |
|---|---|
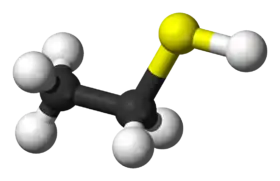
Model molekuly | |
| Obecné | |
| Systematický název | ethanthiol |
| Ostatní názvy | ethylhydrogensulfid, thioethanol |
| Anglický název | Ethanethiol |
| Německý název | Ethanthiol |
| Funkční vzorec | C2H5SH |
| Sumární vzorec | C2H6S |
| Identifikace | |
| Registrační číslo CAS | 75-08-1 |
| PubChem | 6343 |
| SMILES | CCS |
| InChI | 1S/C2H6S/c1-2-3/h3H,2H2,1H3 |
| Číslo RTECS | KI9625000 |
| Vlastnosti | |
| Molární hmotnost | 62,134 04 g/mol |
| Teplota tání | −148 °C, 125 K, −234 °F |
| Teplota varu | 35 °C, 308 K, 95 °F |
| Hustota | 0,861 7 g/cm3 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R11 R20 R50 |
| S-věty | S16 S25 S60 S61 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Průmyslová výroba
Ethylmerkaptan lze vyrobit reakcí sulfanu H2S s plynným ethanolem v kyselém prostředí, nicméně kyselý katalyzátor nesmí reagovat se sulfanem. Tato reakce probíhá pří 400 °C, jako katalyzátor se zde používá ThO2 nebo Al2O3.[2]
C2H5OH + H2S → C2H5SH + H2O
Častěji se však vyrábí reakcí jodethanu s hydrogensulfidem sodným.
C2H5I + NaSH → C2H5SH + NaI
Reakce
Ethylmerkaptan je cenné činidlo v organické syntéze. V přítomnosti hydroxidu sodného vzniká silný nukleofil ethanthiolát sodný. Ten také vzniká při reakci s hydridem sodným.[3]
Také může hořet podle rovnice:
Reference
V tomto článku byl použit překlad textu z článku Ethanethiol na anglické Wikipedii.
- Ethanethiol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- BAHL, Arun; BAHL, B.S. Advanced Organic Chemistry. [s.l.]: S Chand & Co Ltd, 2010. 1524 s. Dostupné online. ISBN 978-8121935159. S. 549. (anglicky)
- MIRRINGTON, R. N.; FEUTRILL, G. I. Orcinol Monomethyl Ether. Org. Synth.. 1988. Dostupné online. (anglicky); Coll. Vol.. S. 859. (anglicky)


