Methylamin
Methylamin (mimo chemii dle PČP metylamin) (CH3NH2) je nejjednodušší amin. Vzniká společně s dimethylaminem při hnití ryb.
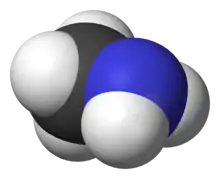
Model molekuly
| Methylamin | |
|---|---|
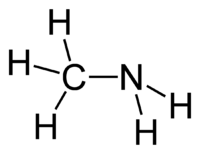
Strukturní vzorec | |
| Obecné | |
| Systematický název | methanamin |
| Anglický název | Methylamine |
| Německý název | Methylamin |
| Funkční vzorec | CH3NH2 |
| Sumární vzorec | CH5N |
| Vzhled | Bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 74-89-5 |
| PubChem | 6329 |
| SMILES | NC |
| InChI | 1S/CH5N/c1-2/h2H2,1H3 |
| Číslo RTECS | PF6300000 |
| Vlastnosti | |
| Molární hmotnost | 31,06 g/mol |
| Teplota tání | −94 °C (179 K) |
| Teplota varu | −6 °C (267 °K) |
| Hustota | 0,699 g/cm3 (−10,8 °C) / 0,902 g/cm3 (40% roztok ve vodě) |
| Viskozita | 0,23 cP (0 °C) |
| Disociační konstanta pKa | 10,62 |
| Rozpustnost ve vodě | 108 g/100 ml (20 °C) |
| Struktura | |
| Dipólový moment | 1,31 D (plyn) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R11 R36/37 (40% vodný roztok) |
| NFPA 704 |  4
3
0
|
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Vlastnosti
Jeho bod vzplanutí je 8 °C, pKa je 10,62[2] (je to tedy slabá zásada). Také je to nukleofilní činidlo.
Bezpečnost
LD50 je (pro myši) 2 400 mg/kg. Methylamin je také prekurzorem metamfetaminu.
Výroba
Vyrábí se reakcí amoniaku s methanolem za přítomnosti katalyzátoru:
CH3OH + NH3 → CH3NH2 + H2O. Touto reakcí se ročně vyrobí více než 400 000 t methylaminu.
Příprava
V laboratoři se připravuje hydrochlorid methylaminu reakcí formaldehydu a chloridu amonného:
- NH4Cl + HCHO → CH2=NH·HCl + H2O
- CH2=NH·HCl + HCHO + H2O → CH3NH2·HCl + HCOOH
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Methylamin na Wikimedia Commons
Obrázky, zvuky či videa k tématu Methylamin na Wikimedia Commons
Reference
- Methylamine. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- PUBCHEM. METHYLAMINE | CH3NH2 - PubChem. pubchem.ncbi.nlm.nih.gov [online]. [cit. 2016-07-11]. Dostupné online.
V tomto článku byl použit překlad textu z článku Methylamine na anglické Wikipedii.
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.



