Trimethylamin
Trimethylamin (zkráceně TMA) je organická sloučenina a nejjednodušší terciární amin. Při pokojové teplotě je v plynném skupenství, ale obvykle se prodává zkapalněný v tlakových lahvích nebo jako 40% vodný roztok. Je zásaditý a lze jej snadno protonovat za vzniku trimethylamoniového kationtu. Trimethylamin je dobrý nukleofil, tato vlastnost je základem většiny jeho využití.
| Trimethylamin | |
|---|---|

strukturní vzorec | |
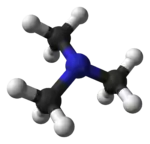
kuličkový model molekuly | |
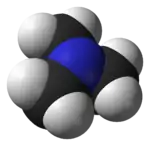
kalotový model molekuly | |
| Obecné | |
| Systematický název | N,N-dimethylmethanamin |
| Anglický název | trimethylamine |
| Německý název | Trimethylamin |
| Funkční vzorec | (CH3)3N |
| Sumární vzorec | C3H9N |
| Vzhled | bezbarvý zapáchající plyn |
| Identifikace | |
| Registrační číslo CAS | 75-50-3 |
| PubChem | 1146 |
| ChEBI | 18139 |
| SMILES | CN(C)C |
| InChI | 1S/C3H9N/c1-4(2)3/h1-3H3 |
| Vlastnosti | |
| Molární hmotnost | 59,11 g/mol |
| Teplota tání | −117,2 °C (156,0 K) |
| Teplota varu | 3–7 °C (276–280 K) |
| Hustota | 0,67 g/cm3 (0 °C) |
| Disociační konstanta pKb | 4,19 |
| Rozpustnost ve vodě | mísitelný |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H220 H315 H318 H332 H335 |
| P-věty | P210 P261 P280 P305 P338 P351 |
| R-věty | R12 R20 R37/38 R41 |
| S-věty | S2 S16 S26 S29 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Trimethylamin je produktem rozkladu organické hmoty a v lidském těle je vytvářen střevní mikroflórou ze složek potravy jako jsou cholin a karnitin. Také je to hlavní látka způsobující zápach z úst a zápach spojovaný s hnitím masa a některými infekcemi.
Výroba
TMA se vyrábí katalyzovanou reakcí methanolu s amoniakem[2]:
3 CH3OH + NH3 → (CH3)3N + 3 H2O
Při této reakci vznikají také dimethylamin a methylamin.
Trimethylamin se také vyrábí reakcí chloridu amonného a paraformaldehydu:
9 (CH2O)n + 2n NH4Cl → 2n (CH3)3N·HCl + 3n H2O + 3n CO2
Použití
Trimethylamin se používá při výrobě cholinu, inhibitorů růstu rostlin, herbicidů, zásaditých anexů a mnoha barviv.[3]
Reference
V tomto článku byl použit překlad textu z článku Trimethylamine na anglické Wikipedii.
- Trimethylamine. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- A. B. van Gysel, W. Musin "Methylamines" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim. DOI:10.1002/14356007.a16_535
- Ashford's Dictionary of Industrial Chemicals. 3rd. vyd. [s.l.]: [s.n.], 2011. ISBN 978-0-9522674-3-0. S. 9362. (anglicky)



