Fluorid sulfurylu
Fluorid sulfurylu je anorganická sloučenina se vzorcem SO2F2. Je to snadno kondenzovatelný plyn, s vlastnostmi podobnými fluoridu sírovému, je odolný vůči hydrolýze až do teploty 150 °C. Má neurotoxické účinky a jde o silný skleníkový plyn, je široce využíván jako insekticid určený k regulaci termitů.
| Fluorid sulfurylu | |
|---|---|
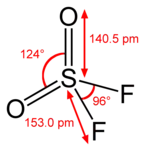
Struktura fluoridu sulfurylu | |
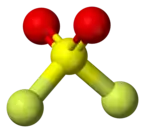
Model molekuly fluoridu sulfurylu | |
| Obecné | |
| Systematický název | Fluorid sulfurylu |
| Anglický název | Sulfuryl fluoride |
| Německý název | Sulfuryl fluoride |
| Sumární vzorec | SO2F2 |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 2699-79-8 |
| PubChem | 17607 |
| SMILES | FS(F)(=O)=O |
| InChI | 1S/F2O2S/c1-5(2,3)4 |
| Vlastnosti | |
| Molární hmotnost | 102,06 g/mol |
| Teplota tání | −124,7 °C |
| Teplota varu | −55,4 °C |
| Hustota | 4,172 kg·m−3 |
| Rozpustnost ve vodě | 0,2 % (0 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| NFPA 704 |  0
3
1
|
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Struktura a příprava
Molekula je tetraedrická, se symetrií C2v. Délka vazby S-O je 140,5 pm, S-F pak 153,0 pm. V souhlasu s teorií VSEPR je úhel O-S-O větší (124°) než F-S-F (96°).[2][3]
Lze jej připravit reakcí oxidu siřičitého s fluoridem draselným:[4]
- SO2 + KF → KSO2F
a následnou reakcí vzniklé soli s chlorem:
- KSO2F + Cl2 → SO2ClF + KCl
Následné zahřívání na 180 °C s fluorosíranem draselným poskytne konečný produkt:
- SO2ClF + KSO2F → SO2F2 + KCl + SO2
Zahřívání fluorosíranu kovu poskytne také požadovaný produkt:[2]
- Ba(OSO2F)2 → BaSO4 + SO2F2
Lze jej připravit i přímou reakcí oxidu siřičitého s fluorem:
- SO2 + F2 → SO2F2
nebo reakcí oxidu sírového s fluoridem sírovým:[3]
- 2 SO3 + SF6 → 3 SO2F2
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Sulfuryl fluoride na anglické Wikipedii.
- Sulfuryl fluoride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- WIBERG, EGON. Inorganic chemistry. 1st English ed.. vyd. San Diego: Academic Press xxxix, 1884 pages s. Dostupné online. ISBN 0-12-352651-5, ISBN 978-0-12-352651-9. OCLC 48056955
- GREENWOOD, NORMAN NEILL. Chemie prvků. Sv. 2.. 1. vyd. vyd. Praha: Informatorium 793 s., 1 příl s. Dostupné online. ISBN 80-85427-38-9. OCLC 320245802 S. 851–853.
- SEEL, F.; CZEREPINSKI, Ralph G.; CADY, George H. Potassium Fluorosulfite: (Potassium Fluorosulfinate). Příprava vydání S. Y. Tyree. Hoboken, NJ, USA: John Wiley & Sons, Inc. Dostupné online. ISBN 978-0-470-13240-1, ISBN 978-0-470-13168-8. DOI 10.1002/9780470132401.ch29. S. 113–115. DOI: 10.1002/9780470132401.ch29.
Externí odkazy
 Obrázky, zvuky či videa k tématu Fluorid sulfurylu na Wikimedia Commons
Obrázky, zvuky či videa k tématu Fluorid sulfurylu na Wikimedia Commons


