3-deoxy-D-arabino-2-heptulózonová kyselina 7-fosfát
3-deoxy-D-arabino-2-heptulózonová kyselina 7-fosfát (DAHP) je sedmiuhlíkatá karboxylová kyselina. Je součástí šikimátové metabolické dráhy a meziproduktem při biosyntéze aromatických aminokyselin.
| 3-deoxy-D-arabino-2-heptulózonová kyselina 7-fosfát | |
|---|---|
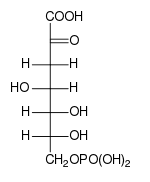
Fischerova projekce DAHP | |
| Obecné | |
| Systematický název | (4R,5S,6R)-4,5,6-trihydroxy-2-oxo-7-fosfonooxyheptanová kyselina |
| Ostatní názvy | DAHP |
| Anglický název | 3-Deoxy-D-arabino-heptulosonic acid 7-phosphate |
| Sumární vzorec | C7H13O10P |
| Identifikace | |
| Registrační číslo CAS | 2627-73-8 |
| PubChem | 160647 |
| SMILES | C([C@H]([C@@H]([C@@H](COP(=O)(O)O)O)O)O)C(=O)C(=O)O |
| InChI | 1S/C7H13O10P/c8-3(1-4(9)7(12)13)6(11)5(10)2-17-18(14,15)16/h3,5-6,8,10-11H,1-2H2,(H,12,13)(H2,14,15,16)/t3-,5-,6+/m1/s1 |
| Vlastnosti | |
| Molární hmotnost | 288,14 g/mol |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Fosfoenolpyruvát a erythróza-4-fosfát vzájemně reagují za vzniku 3-deoxy-D-arabino-2-heptulózonát-7-fosfátu, reakce je katalyzovaná enzymem DAHP syntázou:
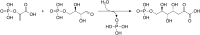 Biosyntéza DAHP z fosfoenolpyruvátu a erythróza-4-fosfátu
Biosyntéza DAHP z fosfoenolpyruvátu a erythróza-4-fosfátu
DAHP je následně přeměněn na 3-dehydrochinát v reakci katalyzované 3-dehydrochinát syntázou. I když tato reakce vyžaduje nikotinamidadenindinukleotid (NAD) jako kofaktor, enzymatický mechanismus jej obnovuje a celkově tak žádný NAD není spotřebován:
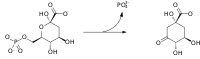 Reakce katalyzovaná 3-dehydrochinát syntázou
Reakce katalyzovaná 3-dehydrochinát syntázou
Mechanismus uzavření kruhu je složitý, ovšem zahrnuje aldolovou kondenzaci na druhém a sedmém uhlíku.
Metabolickým inženýrstvím byla zlepšena produkce DAHP bakterií Escherichia coli.[1] První reakce, kondenzace DAHP z PEP/E4P, využívá tři isoenzymy AroF, AroG a AroH.[2] Ty jsou regulovány tyrosinem, fenylalaninem, resp. tryptofanem. Když je koncentrace některé z uvedených aminokyselin v buňce příliš vysoká, dojde k alosterickému „vypnutí“ DAHP syntázy.
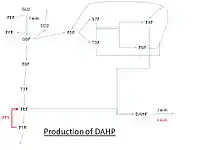 Syntéza DAHP za použití glukózy. Zkratky: GLU: glukóza; G6P: glukóza-6-fosfát; PEP: fosfoenolpyruvát; PYR: pyruvát; F6P: fruktóza-6-fosfát; P5P: pentóza-5-fosfát (ribóza- nebo xylulóza-5-fosfát); T3P: glyceraldehyd-3-fosfát; S7P: sedoheptulóza-7-fosfát; E4P: Erythróza-4-fosfát; PPS: PEP syntáza
Syntéza DAHP za použití glukózy. Zkratky: GLU: glukóza; G6P: glukóza-6-fosfát; PEP: fosfoenolpyruvát; PYR: pyruvát; F6P: fruktóza-6-fosfát; P5P: pentóza-5-fosfát (ribóza- nebo xylulóza-5-fosfát); T3P: glyceraldehyd-3-fosfát; S7P: sedoheptulóza-7-fosfát; E4P: Erythróza-4-fosfát; PPS: PEP syntáza
Reference
V tomto článku byl použit překlad textu z článku 3-Deoxy-D-arabino-heptulosonic acid 7-phosphate na anglické Wikipedii.
- Patnaik, R.; Liao, J. Engineering of Escherichia coli central metabolism for aromatic metabolite production with near theoretical yield. Appl. Environ. Microbiol.. 1994, roč. 60, čís. 11, s. 3903–3908. PMID 7993080. (anglicky)
- PATNAIK, Ranjan; SPITZER, Richard G.; LIAO, James C. Pathway engineering for production of aromatics inEscherichia coli: Confirmation of stoichiometric analysis by independent modulation of AroG, TktA, and Pps activities. Biotechnology and Bioengineering. 1995, roč. 46, čís. 4, s. 361–70. DOI 10.1002/bit.260460409. PMID 18623323. (anglicky)