Kyselina hipurová
Kyselina hipurová alebo kyselina hippurová (obidva tvary sú správne[1]) je karboxylová kyselina. Tvorí rombické kryštály, ktoré sú dobre rozpustné vo vode. Prirodzene sa nachádza v moči, jej hladiny sa zvyšujú pri konzumácii jedál alebo nápojov, ktoré v sebe obsahujú fenolové deriváty, ako napríklad ovocné džúsy, čaje alebo vína.[2] Veľmi vysoké hladiny môžu naznačovať aj otravu toluénom (pozri mechanizmus vzniku nižšie), ale presnosť určenia otravy pomocou takýchto hodnôt je prinajmenšom otázna, pretože hladiny tejto kyseliny môžu ovplyvniť aj mnohé iné faktory.[3] Názov pochádza zo spojenia gréckych slov ἵππος (hippos = kôň) a οὖρον (ouron = moč).
| Kyselina hipurová | |||||||||||||||||||||||||
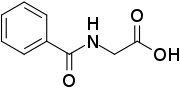 Kyselina hipurová | |||||||||||||||||||||||||
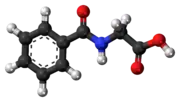 Kyselina hipurová | |||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||
| Sumárny vzorec | C9H9NO3 | ||||||||||||||||||||||||
| Synonymá | Kyselina hippurová | ||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||
| Molárna hmotnosť | 179,175 g·mol−1 | ||||||||||||||||||||||||
| Teplota topenia | 188 °C | ||||||||||||||||||||||||
| Teplota varu | nemá, rozkladá sa pred dosiahnutím varu | ||||||||||||||||||||||||
| Teplota rozkladu | 240 °C | ||||||||||||||||||||||||
| Hustota | 1,371 g/cm3 | ||||||||||||||||||||||||
| Rozpustnosť | dobre rozpustná vo vode | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||
| Číslo CAS | 495-69-2 | ||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||
Výroba
Priemyselne sa vyrába acyláciou glycínu s benzoylchloridom.[4]
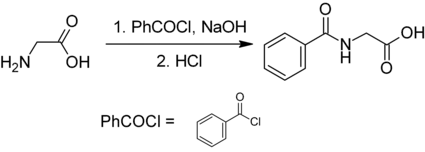
Biosyntéza v tele
V tele vzniká ako jeden z produktov metabolizmu kyseliny benzoovej pomocou priamej acyláciu glycínu s kyselinou benzoovou. Kyselina benzoová v tele vzniká metabolizmom už predtým spomínaných fenolových derivátov (napríklad v jedle), alebo aj niektorých iných zlúčenín, ako napríklad toluén, benzylalkohol, benzoan sodný, ktorý sa pridáva do minerálnych vôd ako konzervačná látka a taktiež hydrolýzou benzylbenzoátu.[5]
Reakcie
Kyselina hipurová sa hydrolyzuje pomocou horúceho roztoku zásad na glycín a kyselinu benzoovú. Jej etylester reaguje s hydrazínom za vzniku hipurylhydrazínu, ktorý použil nemecký chemik Theodor Curtius na prípravu kyseliny azidovodíkovej.
Referencie
- kyselina hipurová, jazykovaporadna.sk
- Human Metabolome Database: Showing metabocard for Hippuric acid (HMDB0000714) [online]. www.hmdb.ca, [cit. 2019-02-28]. Dostupné online.
- PERO, Ronald W.. Health Consequences of Catabolic Synthesis of Hippuric Acid in Humans [online]. Current Clinical Pharmacology, 2010-01-31, [cit. 2019-02-28]. Dostupné online. (po anglicky)
- http://orgsyn.org/demo.aspx?prep=CV2P0328 [online]. orgsyn.org, [cit. 2019-02-28]. Dostupné online. (po anglicky)
- JR, Wayland J. Hayes. Classes of Pesticides. [s.l.] : Elsevier, 2013-10-22. Google-Books-ID: WiIlBQAAQBAJ. Dostupné online. ISBN 9781483288635. (po anglicky)

