Kyselina glutamová
Kyselina L-glutamová (symbol Glu nebo E) je kódovaná glukogenní neesenciální aminokyselina. V potravinářství se označuje kódem E 620. Její soli se nazývají glutamany (glutamáty), např. glutaman sodný nebo glutaman draselný.
| Kyselina glutamová | |
|---|---|

Strukturní vzorec L-glutamové kyseliny | |
| Obecné | |
| Systematický název | kyselina (2S)-2-aminopentandiová ; kyselina L-2-aminopentandiová |
| Ostatní názvy | Racionální název
|
| Sumární vzorec | C5H9NO4 |
| Identifikace | |
| Registrační číslo CAS | (L-forma) ; 6893-26-1 (D-forma) ; 617-65-2 (racemická směs, DL)&Units=SI 56-86-0 (L-forma) ; 6893-26-1 (D-forma) ; 617-65-2 (racemická směs, DL) |
| Vlastnosti | |
| Molární hmotnost | 147,130 g/mol |
| Teplota tání | 247–249 °C (rozklad) |
| Teplota varu | — |
| Hustota | 1,538 g/cm3 |
| Disociační konstanta pKa | 2,13 (COOH, 25 °C) ; 4,31 (COOH, 25 °C) ; 9,67 (NH3+) |
| Rozpustnost ve vodě | 0,340 g/100 ml (0 °C) ; 0,857 g/100 ml (25 °C) ; 1,40 g/100 ml (100 °C) |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava a výroba
Vyrábí se průmyslově ve velkém množství hydrolýzou bílkovin a následným dělením směsi aminokyselin, zejména z hydrolyzátu kvasinek pěstovaných na substrátech obsahujících škrob (zejména brambory, mouka, cukrová řepa, melasa apod.).
Chemické vlastnosti
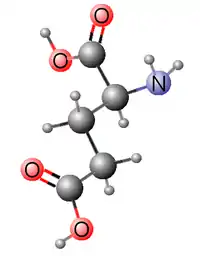
Vzhledem k přítomnosti dvou karboxylových skupin v molekule vykazuje kyselina L-glutamová slabě kyselou reakci; proto se řadí ke kyselým aminokyselinám, spolu s kyselinou L-asparagovou.
Protože má v molekule jedno chirální centrum, uhlíkový atom, k němuž je připojena karboxylová a aminová skupina, existuje kyselina glutamová ve dvou stereoizomerech, jako kyselina L-glutamová a kyselina D-glutamová, které mají stejné fyzikální vlastnosti s výjimkou optické aktivity. Živé organismy však většinou vytváří pouze proteiny obsahující L-formu. Výjimkou jsou neribozomální peptidy nebo proteiny dodatečně modifikované pomocí izomeráz, jedná se typicky o toxiny.[1] D-glutamová kyselina je také významnou složkou peptidoglykanu z bakteriální buněčné stěny.[2]
Její barnatá a zinečnatá sůl jsou špatně rozpustné ve vodě, čehož se využívá k jejímu dělení od směsi jiných aminokyselin. Její kodóny jsou GAA, GAG.
Fyziologický význam
Neurotransmise
Glutamát jako konjugovaná báze kyseliny je hlavní excitační transmiter v CNS a rychlá excitační glutamátergní transmise je podkladem přenosu a zpracování informací v celém mozku (ostatní transmiterové systémy mají pouze buď inhibiční nebo modulační funkce). V intermediárním metabolismu produkován transaminací alfa-ketoglutarátu a resyntéza přes glutamin.
Zpětné vychytávání a recyklace
K vychytávní dochází pomocí EAAT (excitatory amino acid transporter), který má 5 podtypů, přičemž EAAT1-2 je primárně astrogliální (rodent GLAST, resp. GLT-1), EAAT3-4 je výlučně neuronální a EAAT5 se vyskytuje pouze v sítnici. Vychytávací mechanismy velmi efektivní a rychlé, což je nutná podmínka rychlého a přesného přenosu informací, proto extracelulární koncentrace glutamátu za fyziologických okolností enormně nízká a při patologických stavech zvýšení koncentrace glutamátu vede k excitotoxicitě. K jeho distribuci se užívá vesikulární transportér VGLUT 1-3 a k recyklaci glutamát-glutaminový cyklus.
Receptory glutamátu
Mezi ionotropní glutamátu patří AMPA receptory, NMDA receptory a kainátové a mezi metabotropní pak mGluR1-5.
Klinické aspekty
U ischémie dochází k selhání znovu vychytávacích mechanismů (ztráta hnacího iontového gradientu) a riziko Glu excitotoxicity v důsledku přehnané aktivace synaptických receptorů a nefyziologické aktivace extrasynaptických receptorů. Schizofrenii provází funkční (narušená NMDA signalizace) i strukturální změny glutamátergního systému, části dány abnormálním vývojem, tj. defektní migrace a pruning a abnormální konektivita mezi některými oblastmi a systémy (konektopatie).
Syntéza
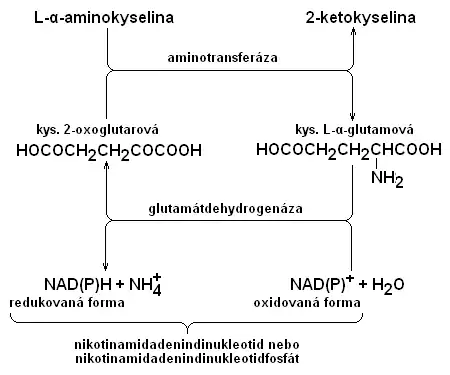
Kyselina L-glutamová se uplatňuje v řadě reakcí, zejména při přenosu aminových skupin NH2 (viz transaminace) mezi jinými aminokyselinami. Tato reakce je v organismu řízena enzymem aminotransferázou (transaminázou), přičemž kyselina L-glutamová je v rovnováze s kyselinou.2-oxoglutarovou. S touto reakcí úzce souvisí i oxidační deaminace kyseliny glutamové působením enzymu glutamátdehydrogenáza, takže vzniká významný dvojitý cyklus, zjednodušeně popsaný následujícím schématem:
Syntéza glukozy a transport tuků
Produkt deaminace - kyselina 2-oxoglutarová - je důležitým meziproduktem při přeměně kyseliny glutamové na glukosu.
Kyselina glutamová se podílí též na metabolizmu tuků. Hraje důležitou roli v detoxikaci amoniaku v organizmech. Podílí se na přenosu iontů draslíku mezi krevním řečištěm a mozkovou tkání. Kromě toho je kyselina glutamová prekurzorem biosyntézy neesenciálních aminokyselin glutaminu a prolinu. Glutamová kyselina je nejdůležitějším excitačním (budivým) neurotransmiterem v centrální nervové soustavě[3] (zajišťuje až 75 % excitace) a v sítnici; váže se na různé glutamátové receptory. Dekarboxylací glutamátu v buňkách vzniká naopak tlumivý neurotransmiter GABA (kyselina γ-aminomáselná) podle této rovnice:
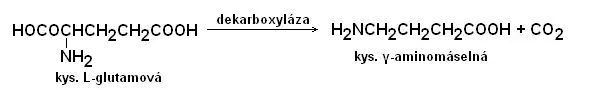
Vzhledem k tomu, že se ve značném množství nachází i v prostatě, zdá se, že zde má významnou, byť dosud plně neobjasněnou funkci.
Použití
V lékařství se uvažuje o jejím využití zejména při léčbě neurologických poruch jako např. epilepsie, Parkinsonovy nemoci, mentální retardace, poruch osobnosti, poruch v chování (zejména u dětí), dále pak k potlačování svalové dystrofie, hypoglykemického kómatu, při léčbě žaludečních vředů aj.[zdroj?]
V potravinářství se kyselina L-glutamová používá jako stabilizátor barviv nebo jako antioxidant; české a evropské právní normy vyžadují uvedení jejího použití v potravinářských výrobcích na jejich obalech. Značné množství kyseliny se průmyslově přeměňuje neutralizací hydroxidem sodným
- HOOC-CH(NH2)-CH2-CH2-COOH + NaOH → HOOC-CH(NH2)-CH2-CH2-COONa + H2O
na její monosodnou sůl (glutaman sodný), která slouží k ochucování potravin.
Zdravotní rizika
Předávkování kyselinou glutamovou může způsobovat přechodné zdravotní problémy, zejména bolesti hlavy (migréna), případně i různé neurologické potíže. Podle některých zdrojů může vyvolávat rovněž záchvaty u určitých forem epilepsie.[4][5]
V červenci 2017 Evropský úřad pro bezpečnost potravin (EFSA) zveřejnil hodnocení bezpečnosti glutamátů a stanovil přijatelný denní příjem 30 miligramů na kilogram tělesné hmotnosti. Zároveň doporučil přezkoumat maximální limity pro glutamáty přidávané do potravin, např. pro jemné pečivo, polévky a bujóny, omáčky, maso a masné výrobky, koření a doplňky stravy.[6]
Odkazy
Reference
- KREIL, G. D-amino acids in animal peptides.. Annu Rev Biochem. 1997, roč. 66, s. 337–45. Dostupné online. DOI 10.1146/annurev.biochem.66.1.337. PMID 9242910.
- DOUBLET, P.; VAN HEIJENOORT, J.; MENGIN-LECREULX, D. Identification of the Escherichia coli murI gene, which is required for the biosynthesis of D-glutamic acid, a specific component of bacterial peptidoglycan.. J Bacteriol. Sep 1992, roč. 174, čís. 18, s. 5772–9. Dostupné online. PMID 1355768.
- SCOTT, Derek B.; EHLERS, Michael D. Glutamate Receptors, Ionotropic. In: Lennarz,W.J., Lane, M.D. Encyclopedia of Biological Chemistry , Four-Volume Set, 1-4. [s.l.]: [s.n.]
- DEVINSKY, SCHACHTER, PACIA. Complementary and Alternative Therapies for Epilepsy. www.ilae.org [online]. 2005 [cit. 2019-11-17]. Dostupné v archivu pořízeném z originálu.
- Glutamátová dieta - proti migréně, epilepsii a dalším zdravotním neduhům. glutamat-dieta.blogspot.com [online]. 2017 [cit. 2019-11-17]. Dostupné online.
- Miroslav Šuta: Syndrom čínské restaurace a kontroverzní „éčka“. Hlídejte si glutamáty v jídle, Zdraví "v cajku", 2. srpna 2017
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina glutamová na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina glutamová na Wikimedia Commons