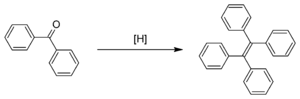
Deoxygenace
Deoxygenace je chemická reakce, při které dochází k odstranění atomu kyslíku z molekuly nebo molekulárního kyslíku (O2) z plynů a rozpouštědel. U organických sloučenin se využívá například na výrobu paliv a v organické syntéze mimo jiné při výrobě léčiv.
Deoxygenace vazeb C-O
Nahrazení H2
Kyslíkový atom může být odstraněn pomocí dvou vodíkových atomů (A=O → A) hydrogenolýzou. Tato reakce se často provádí pomocí kovových katalyzátorů a plynného vodíku (H2). Reakční podmínky jsou obvykle tvrdší než u hydrogenace.
Stechiometrickou deoxygenační reakcí je například Wolffova–Kishnerova redukce arylketonů. Nahrazení hydroxylové skupiny vodíkem (A-OH → A-H) je součástí Bartonovy–McCombieovy a Markóovy–Lamovy deoxygenace.
Přeměna biomasy
Deoxygenace jsou důležitými kroky při výrobě paliv a chemikálií z biomasy. Účinnost částečných deoxygenací se zvyšuje dehydratacemi a dekarboxylacemi.[1]
Ostatní způsoby
Kyslíkaté skupiny mohou být odstraněny také redukčním párováním ketonů, například v McMurryovově reakci.
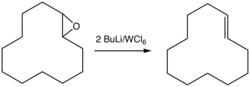
Epoxidy lze deoxygenovat oxofilními činidly připravenými smícháním chloridu wolframového a n-butyllithia na alkeny; reakce může proběhnout se zachováním i obrácením konfigurace.[2][3]
Deoxygenace vazeb S-O a P-O
Vazby P=O
Fosfor se v přírodě vyskytuje ve formě oxidů, takže k přípravě elementární formy je potřeba provést deoxygenaci. Nejběžnějším postupem je karbotermická redukce, kdy je deoxygenačním činidle uhlík.
- 4 Ca5(PO4)3F + 18 SiO2 + 30 C → 3 P4 + 30 CO + 18 CaSiO3 + 2 CaF2
U některých deoxygenačních reakcí prováděných v laboratořích lze použít oxofilní sloučeniny prvků hlavní skupiny. Silně oxofilní hexachlordisilan (Si2Cl6) stereospecificky deoxygenuje fosfinoxidy.[4]
Vazby S=O
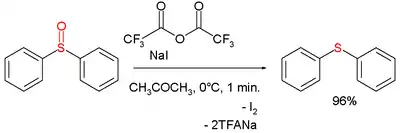
K deoxygenaci sirných a dusíkatých oxosloučenin se často používá směs anhydridu kyseliny trifluoroctové a jodidu sodného.[6] Na následujícím obrázku je znázorněna deoxygenace difenylsulfoxidu na difenylsulfid:
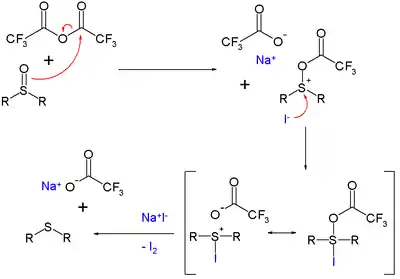
Reakční mechanismus spočívá v aktivaci sulfoxidu trifluoracetylovou skupinou a oxidaci jodu. Jod se vytváří kvantitativně a tak se uvedené činidlo používá k důkazu přítomnosti mnohých oxosloučenin.
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Deoxygenation na anglické Wikipedii.
- Roger A. Sheldon. Green and sustainable manufacture of chemicals from biomass: state of the art. Green Chemistry. 2014, s. 950–963. DOI 10.1039/C3GC41935E.
- K. Barry Sharpless; Martha A. Umbreit. Deoxygenation of Epoxides with Lower Valent Tungsten Halides: trans-Cyclododecene. Organic Syntheses. 1981, s. 29. DOI 10.15227/orgsyn.060.0029.
- Takuya Nakagiri; Masahito Murai; Kazuhiko Takai. Stereospecific Deoxygenation of Aliphatic Epoxides to Alkenes under Rhenium Catalysis. Organic Letters. 2015, s. 3346–3349. DOI 10.1021/acs.orglett.5b01583.
- David P. Sebesta "Hexachlorodisilane" in Encyclopedia of Reagents for Organic Synthesis John Wiley, London, 2001. DOI:10.1002/047084289X.rh007 Article Online Posting Date: April 15, 2001.
- Evgeniya Podyacheva; Ekaterina Kuchuk; Denis Chusov. Reduction of phosphine oxides to phosphines. Tetrahedron Letters. 2019, s. 575–582. DOI 10.1016/j.tetlet.2018.12.070.
- Trifluoroacetic anhydride-sodium iodide reagent. Nature and applications Arkivoc 2007 (JE-2136MR) Zbigniew H. Kudzin, Marcin H. Kudzin, Józef Drabowicz, and Andrzej Kotyński Link