Chloraceton
Chloraceton je chemická sloučenina patřící mezi organické sloučeniny, její vzorec je CH3COCH2Cl.
| Chloraceton | |
|---|---|
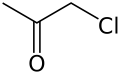
Zjednodušený strukturní vzorec | |
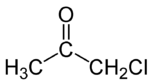
Strukturní vzorec | |
| Obecné | |
| Systematický název | Chlorpropanon |
| Anglický název | Chloroacetone |
| Německý název | Chloraceton |
| Funkční vzorec | CH3COCH2Cl |
| Sumární vzorec | C3H5ClO |
| Vzhled | bezbarvá kapalina, oxidací mění barvu na zlatohnědou |
| Identifikace | |
| Registrační číslo CAS | 78-95-5 |
| PubChem | 6571 |
| SMILES | ClCC(=O)C |
| InChI | 1/C3H5ClO/c1-3(5)2-4/h2H2,1H3 |
| Vlastnosti | |
| Molární hmotnost | 92,524 g/mol |
| Teplota tání | −44,5 °C |
| Teplota varu | 119 °C |
| Hustota | 1,15 g/cm3 (20 °C/kapalný) |
| Rozpustnost ve vodě | 10 g/100 ml |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Teplota vznícení | 610 °C |
| Meze výbušnosti | 3,4 % |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava
Vzniká přímou chlorací acetonu (zaváděním plynného chloru do acetonu) za kyselé katalýzy.
- CH3-CO-CH3 + Cl2 → Cl-CH2-CO-CH3 + HCl.
Tímto způsobem lze připravit i další halogenderiváty ketonů (např. jodaceton, bromaceton…) Halogenace ketonů probíhá zpravidla velmi snadno, dokonce již ve vodném prostředí.
Může vznikat též reakcí kyseliny chlorné nebo chlornanu (nejlépe vápenatého Ca(ClO)2) a acetonu v kyselém prostředí:
- CH3-CO-CH3 + HClO → Cl-CH2-CO-CH3 + H2O
Vlastnosti
Je silně dráždivý. Jeho páry způsobují slzení, proto se používá jako bojová slzotvorná látka. Jeho toxicita je za prahem snesitelnosti, tudíž otrava jím je nepravděpodobná.
Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu chloraceton na Wikimedia Commons
Obrázky, zvuky či videa k tématu chloraceton na Wikimedia Commons
Reference
- Chloroacetone. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.



