CD47
CD47 (Cluster of Differentiation 47) také známý pod názvem „integrin associated protein“ (IAP, s integriny asociovaný protein) je pětkrát transmembránový protein kódovaný u lidí genem CD47. CD47 patří do nadrodiny[1] a tvoří funkční celek s membránovými integriny, dále váže trombospondin-1 (TSP-1) a signalizační-regulační protein alfa (SIRPα).[2] Díky schopnosti tvořit vazbu CD47-SIRPα slouží CD47 jako tzv. „don't eat me“ signál.[3] CD47 je funkčně důležitý pro mnoho buněčných procesů jakými jsou např. apoptóza, proliferace, adheze a migrace. Především je však klíčový pro imunitní odpověď a angiogenezi. CD47 je exprimován na všech zdravých buňkách lidského těla a zároveň byla jeho zvýšená exprese zjištěna u buněk nádorových.[2][4] Kromě toho byla zjištěna jeho exprese i u koňských nádorů kůže.[5]
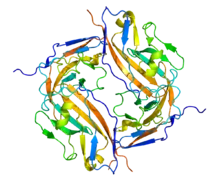
Struktura
CD47 je 50kDa membránový receptor, který má extracelulární N-koncovou imunoglobulinovou doménu, 5 transmembránových úseků a intracelulárně orientovaný C-konec, který se může vyskytovat v několika alternativních sestřihových variantách. Tyto jednotlivé isoformy se od sebe vzájemně liší pouze délkou C-koncové oblasti.[6] Izoforma č. 2 je v lidském těle nejrozšířenější a vyskytuje se v cirkulujících imunitních buňkách. Druhá nejčastější je izoforma č. 4 exprimovaná především v mozku a periferním nervovém systému, s výjimkou keratinocytů, které exprimují izoformu č. 1. Funkční význam alternativního sestřihu nebyl v případě CD47 zatím popsán, ačkoliv jednotlivé izoformy jsou vysoce konzervované jak u člověka, tak u myši.[2][6]
Interakce s vazebnými partnery
Trombospondin (TSP)
CD47 je vysoko-afinní receptor pro trombospondin-1 (TSP-1), sekretovaný glykoprotein hrající roli ve vývoji vaskulary a angiogenezi, během níž TSP1-CD47 vazba inhibuje signalizaci NO.[7] Vazba TSP-1 s CD47 ovlivňuje základní děje v buňce, jako jsou například adheze, migrace, apoptóza a buněčná proliferace a podílí se na řízení angiogeneze a zánětu.[2]
Signal-regulatory protein (SIRP)
CD47 tvoří vazbu se SIRPA (signal-regulatory protein alpha, SIRPα) proteinem, což je inhibiční receptor na povrchu myeloidních buněk. CD47-SIRPα vazba vede k obousměrné signalizaci, která vede uvnitř myeloidní buňky skrze ITIM motivy SIRPα proteinu k zablokování fagocytického pohlcení buňky nesoucí CD47. Zároveň tato interakce aktivuje T-buněk.[8][9][10]
Funkce
Nádorové buňky
Navzdory všeobecné expresi CD47 se signalizace skrze tento protein liší v závislosti na buněčném typu. Výsledek signalizace skrze CD47 je tedy ovlivněn jeho intracelulárními a transmembránovými partnery.
Buněčná proliferace
Role CD47 ve stimulaci proliferace je taktéž závislá na buněčném typu, neboť jak aktivace, tak ztráta CD47 mohou vést k zahájení proliferace buňky. Vazba CD47 s TSP-1 zvyšuje proliferaci lidských buněk astrocytomové linie U87 a U37, ačkoliv u zdravých astrocytů tento efekt nenastává. U stejných buněk bylo dokázáno, že blokující protilátky inhibují proliferaci nádorových, nikoliv zdravých astrocytů. Ačkoliv přesný mechanismus je neznámý, CD47 zřejmě aktivuje proliferaci skrze PI3K/Akt dráhu u nádorově transformovaných buněk.[11] K přetrvávající proliferaci také vede ztráta CD47 u primárních endoteliálních buněk myši, a zároveň dovoluje přeprogramovat tyto buňky na multipotentní tělíska embryonálního charakteru. Exprese kmenových znaků, jako je například c-Myc, je zvýšena u endoteliálních buněk s deletovaných CD47 a u lidských T-buněčných linií postrádajících expresi CD47. Aktivace CD47 vazbou TSP-1 inhibuje proliferaci a snižuje expresi transkripčních faktorů zodpovědných za kmenový charakter.[12]
Buněčná smrt
Signalizace skrze CD47 vede k iniciaci buněčné smrti (apoptózy, či autofágie) v mnoha zdravých i nádorových buněčných liniích. K rychlé aktivaci apoptózy tak dochází u lidských T-buněčných linií, linie Jurkat a periferní mononukleární buňky (PBMC) inkubované s monoklonální protilátkou klonu Ad22 přejdou do apoptotického stavu během 3 hodin. Jiné klony protilátek však tento efekt neprokázaly. Indukce apoptózy je tedy závislá na blokování pouze určitých epitopů extracelulární domény CD47.[13] Indukce apoptózy byla prokázány i u B-buněčné chronické lymfocytární leukémie (CLL). Inkubace s dimerem protilátek spojeným disulfidickou vazbou opouští apoptózu CD47+ primárních buněk B-CLL a buněk linie MOLT-4 a JOK-1. Navíc vnesení protilátky do SCID myši po implantaci JOK-1 buněk prodlouží její věk dožití. Spuštění apoptózy je v tomto modelu ovlivněno HIF-1α dráhou.[14]
Migrace
Buněčná migrace je ligací CD47 všeobecně stimulována. Význam CD47 pro migraci byl zprvu studován na neutrofilech, u kterých inkubace s monoklonální protilátkou inhibovala transmigraci endotelem. Tento jev je způsoben integriny avb3, které jsou aktivovány proteinem CD47 na plazmatické membráně.[10][2] Blokování CD47 protilátkou zabraňuje migraci a tvorbě metastáz u mnoha nádorů. Lze tak zabránit chemotaxi vyvolané kolagenem IV u melanomů, karcinomu prostaty a ovária.[15] V myším modelu násobného melanomu dochází ke snížení metastatického potenciálu do kostní dřeně u myší s knock-outovaným CD47.[16] Stejně tak delece CD47 pomocí shRNA u myší s xenotransplantovaným non-Hodgkinovým lymfomem snižuje výskyt.[17]
Angiogeneze
Ztráta CD47 zvyšuje proliferaci a asymetrické dělení primárních myších endoteliálních buněk.[12] Aktivace CD47 pomocí TSP-1 u primárních myších cerebrálních endoteliálních buněk indukuje cytotoxicitu, která je významně nižší u cerebrálních endoteliálních buněk s deletovaným CD47.[18] In vitro bylo aktivací TSP-1, která inhibovala migraci endoteliálních buněk, dokázáno, že CD47 tlumí angiogenezi.[18] Mechanismus anti-angiogenní aktivity CD47 není zatím známý, ale monoklonální protilátky v kombinaci s TSP-1 inhibují NO-stimulované reakce u endoteliálních buněk a buněk hladkého svalstva cév.[7] CD47 signalizace ovlivňuje SDF-1 chemokinovou dránu, která je zásadní pro angiogenezi.[19]
Zánětlivá odpověď
Interakce mezi CD47 na endoteliální buňce a SIRPγ na leukocytu regulují T-buněčnou transendoteliální migraci (TEM) v místech zánětu. CD47 knockout myši mají nižší schopnost rekrutovat T-buňky, neutrofily a monocyty do míst zánětu.[20] CD47 také slouží jako tzv. self-marker u myších erytrocytů, kde zabraňuje jejich fagocytóze. Erytrocyty postrádající CD47 jsou ihned odstraněny makrofágy.[21] Myší hematopoietické kmenové buňky (HSCs) přechodně zvyšují expresi CD47 během migratorní fáze, což zabraňuje pohlcení makrofágem in vivo.[22] Podobně se i nádorové buňky vyhýbají odstranění fagocytickými buňkami z těla zvýšenou expresí CD47.[4] CD47 je například exprimován ve zvýšené míře na kmenových buňkách nádoru močového měchýře (CSCs). Zablokování CD47 monoklonální protilátkou vede k pohlcení nádorových buněk makrofágem.[23] Exprese CD47 je také zvýšena u myeloidní leukémie a u dalších pevných i krevních nádorových onemocnění, kde napomáhá ochraně nádoru před imunitním systémem.[22]
Klinický význam
CD47 byl nejprve objeven jako nádorový antigen u karcinomu ovária 80. letech 20. století. Od té doby bylo zjištěno, že je exprimován u mnohých dalších nádorů včetně akutní myeloidní leukémie, chronické myeloidní leukémie, non-Hodgkinovského lymfomu, násobného myelomu, nádoru močového měchýře, a u dalších pevných nádorů.[4] CD47 je také hojně exprimován u nádorů mozku dětí i dospělých.[24] Vysoká exprese CD47 umožňuje nádoru vyhnout se fagocytóze navzdor vysoké expresi kalretikulinu, který je jedním z pro-fagocytických signálů.[25] za to je zodpovědná signalizace skrze vazbu CD47-SIRPA a aktivace inhibičních ITIM motivů ve fagocytující buňce.
Terapeutický cíl
Odblokování fagocytózy nádorových buněk anti-CD47 monoklonální protilátkou aktivuje zároveň i silnou T-buněčnou protinádorovou odpověď. Terapie zablokováním CD47 má tedy dvojí účinek, kdy kromě aktivace fagocytózy, mechanismu vrozeného imunitního systému, aktivuje nádorově-specifické lymfocyty tak, že rozpoznají a budou aktivovány nádorovými antigeny.[26][27] Humanizovaná anti-CD47 protilátka dnes prochází klinickým testováním jako terapeutikum pro řadu krevních i pevných nádorů.[24]
Reference
- "Entrez Gene: CD47 CD47 molecule".
- Sick E, Jeanne A, Schneider C, Dedieu S, Takeda K, Martiny L (December 2012). "CD47 update: a multifaceted actor in the tumour microenvironment of potential therapeutic interest". Br. J. Pharmacol. 167 (7): 1415–30. doi:10.1111/j.1476-5381.2012.02099.x. PMC 3514757 Freely accessible. PMID 22774848
- https://medicalxpress.com/news/2017-04-fibrosis-reversed-dont-blocked-stanford.html
- Chao MP, Weissman IL, Majeti R (April 2012). "The CD47-SIRPα pathway in cancer immune evasion and potential therapeutic implications". Curr. Opin. Immunol. 24 (2): 225–32. doi:10.1016/j.coi.2012.01.010. PMC 3319521 Freely accessible. PMID 22310103
- Caston, Stephanie; Cooper, Elizabeth; Chandramani-Shivalingappa, Prashanth; Sponseller, Brett; Hostetter, Jesse; Sun, Yaxuan (July 2016). "CD47 expression in cryopreserved equine cutaneous masses and normal skin". Journal of Veterinary Diagnostic Investigation. 28 (4): 408–413. doi:10.1177/1040638716643352. PMID 27154320
- Reinhold MI, Lindberg FP, Plas D, Reynolds S, Peters MG, Brown EJ (November 1995). "In vivo expression of alternatively spliced forms of integrin-associated protein (CD47)". J. Cell Sci. 108 (Pt 11): 3419–25. PMID 8586654. Frazier WA, Isenberg JS, Kaur S, Roberts DD (February 2010). "CD47". UCSD Nature Molecule Pages. doi:10.1038/mp.a002870.01
- Isenberg JS, Ridnour LA, Dimitry J, Frazier WA, Wink DA, Roberts DD (September 2006). "CD47 is necessary for inhibition of nitric oxide-stimulated vascular cell responses by thrombospondin-1". J. Biol. Chem. 281 (36): 26069–80. doi:10.1074/jbc.M605040200. PMID 16835222
- Sick E, Jeanne A, Schneider C, Dedieu S, Takeda K, Martiny L (December 2012). "CD47 update: a multifaceted actor in the tumour microenvironment of potential therapeutic interest". Br. J. Pharmacol. 167 (7): 1415–30. doi:10.1111/j.1476-5381.2012.02099.x. PMC 3514757 Freely accessible. PMID 22774848
- Barclay AN (February 2009). "Signal regulatory protein alpha (SIRPα)/CD47 interaction and function". Curr. Opin. Immunol. 21 (1): 47–52. doi:10.1016/j.coi.2009.01.008. PMC 3128989 Freely accessible. PMID 19223164
- Brown EJ, Frazier WA (March 2001). "Integrin-associated protein (CD47) and its ligands". Trends Cell Biol. 11 (3): 130–5. doi:10.1016/S0962-8924(00)01906-1. PMID 11306274
- Sick E, Boukhari A, Deramaudt T, Rondé P, Bucher B, André P, Gies JP, Takeda K (February 2011). "Activation of CD47 receptors causes proliferation of human astrocytoma but not normal astrocytes via an Akt-dependent pathway". Glia. 59 (2): 308–19. doi:10.1002/glia.21102. PMID 21125662
- Kaur S, Soto-Pantoja DR, Stein EV, Liu C, Elkahloun AG, Pendrak ML, Nicolae A, Singh SP, Nie Z, Levens D, Isenberg JS, Roberts DD (April 2013). "Thrombospondin-1 Signaling through CD47 Inhibits Self-renewal by Regulating c-Myc and Other Stem Cell Transcription Factors". Sci Rep. 3: 1673. doi:10.1038/srep01673. PMC 3628113 Freely accessible. PMID 23591719
- Pettersen RD, Hestdal K, Olafsen MK, Lie SO, Lindberg FP (June 1999). "CD47 signals T cell death". J. Immunol. 162 (12): 7031–40. PMID 10358145
- Sagawa M, Shimizu T, Fukushima N, Kinoshita Y, Ohizumi I, Uno S, Kikuchi Y, Ikeda Y, Yamada-Okabe H, Kizaki M (June 2011). "A new disulfide-linked dimer of a single-chain antibody fragment against human CD47 induces apoptosis in lymphoid malignant cells via the hypoxia inducible factor-1α pathway". Cancer Sci. 102 (6): 1208–15. doi:10.1111/j.1349-7006.2011.01925.x. PMID 21401803
- Shahan TA, Fawzi A, Bellon G, Monboisse JC, Kefalides NA (February 2000). "Regulation of tumor cell chemotaxis by type IV collagen is mediated by a Ca(2+)-dependent mechanism requiring CD47 and the integrin alpha(V)beta(3)". J. Biol. Chem. 275 (7): 4796–802. doi:10.1074/jbc.275.7.4796. PMID 10671513
- Uluçkan O, Becker SN, Deng H, Zou W, Prior JL, Piwnica-Worms D, Frazier WA, Weilbaecher KN (April 2009). "CD47 regulates bone mass and tumor metastasis to bone". Cancer Res. 69 (7): 3196–204. doi:10.1158/0008-5472.CAN-08-3358. PMC 2763641 Freely accessible. PMID 19276363
- Chao MP, Tang C, Pachynski RK, Chin R, Majeti R, Weissman IL (November 2011). "Extranodal dissemination of non-Hodgkin lymphoma requires CD47 and is inhibited by anti-CD47 antibody therapy". Blood. 118 (18): 4890–901. doi:10.1182/blood-2011-02-338020. PMC 3208297 Freely accessible. PMID 21828138
- Xing C, Lee S, Kim WJ, Wang H, Yang YG, Ning M, Wang X, Lo EH (August 2009). "Neurovascular effects of CD47 signaling: promotion of cell death, inflammation, and suppression of angiogenesis in brain endothelial cells in vitro". J. Neurosci. Res. 87 (11): 2571–7. doi:10.1002/jnr.22076. PMC 3712846 Freely accessible. PMID 19360900
- Smadja DM, d'Audigier C, Bièche I, Evrard S, Mauge L, Dias JV, Labreuche J, Laurendeau I, Marsac B, Dizier B, Wagner-Ballon O, Boisson-Vidal C, Morandi V, Duong-Van-Huyen JP, Bruneval P, Dignat-George F, Emmerich J, Gaussem P (March 2011). "Thrombospondin-1 is a plasmatic marker of peripheral arterial disease that modulates endothelial progenitor cell angiogenic properties". Arterioscler. Thromb. Vasc. Biol. 31 (3): 551–9. doi:10.1161/ATVBAHA.110.220624. PMID 21148423
- Azcutia V, Stefanidakis M, Tsuboi N, Mayadas T, Croce KJ, Fukuda D, Aikawa M, Newton G, Luscinskas FW (September 2012). "Endothelial CD47 promotes vascular endothelial-cadherin tyrosine phosphorylation and participates in T cell recruitment at sites of inflammation in vivo". J. Immunol. 189 (5): 2553–62. doi:10.4049/jimmunol.1103606. PMC 3424398 Freely accessible. PMID 22815286
- Oldenborg PA, Zheleznyak A, Fang YF, Lagenaur CF, Gresham HD, Lindberg FP (June 2000). "Role of CD47 as a marker of self on red blood cells". Science. 288 (5473): 2051–4. doi:10.1126/science.288.5473.2051. PMID 10856220
- Jaiswal S, Jamieson CH, Pang WW, Park CY, Chao MP, Majeti R, Traver D, van Rooijen N, Weissman IL (July 2009). "CD47 is upregulated on circulating hematopoietic stem cells and leukemia cells to avoid phagocytosis". Cell. 138 (2): 271–85. doi:10.1016/j.cell.2009.05.046. PMC 2775564 Freely accessible. PMID 19632178
- Chan KS, Espinosa I, Chao M, Wong D, Ailles L, Diehn M, Gill H, Presti J, Chang HY, van de Rijn M, Shortliffe L, Weissman IL (August 2009). "Identification, molecular characterization, clinical prognosis, and therapeutic targeting of human bladder tumor-initiating cells". Proc. Natl. Acad. Sci. U.S.A. 106 (33): 14016–21. doi:10.1073/pnas.0906549106. PMC 2720852 Freely accessible. PMID 19666525
- Gholamin S, Mitra SS, Feroze AH, Liu J, Kahn SA, Zhang M, et al. (March 2017). "Disrupting the CD47-SIRPα anti-phagocytic axis by a humanized anti-CD47 antibody is an efficacious treatment for malignant pediatric brain tumors". Science Translational Medicine. 9 (381): eaaf2968. doi:10.1126/scitranslmed.aaf2968. PMID 28298418
- Chao MP, Jaiswal S, Weissman-Tsukamoto R, Alizadeh AA, Gentles AJ, Volkmer J, Weiskopf K, Willingham SB, Raveh T, Park CY, Majeti R, Weissman IL (December 2010). "Calreticulin is the dominant pro-phagocytic signal on multiple human cancers and is counterbalanced by CD47". Sci Transl Med. 2 (63): 63ra94. doi:10.1126/scitranslmed.3001375. PMC 4126904 Freely accessible. PMID 21178137
- Tseng D, Volkmer JP, Willingham SB, Contreras-Trujillo H, Fathman JW, Fernhoff NB, Seita J, Inlay MA, Weiskopf K, Miyanishi M, Weissman IL (July 2013). "Anti-CD47 antibody-mediated phagocytosis of cancer by macrophages primes an effective antitumor T-cell response". Proc. Natl. Acad. Sci. U.S.A. 110 (27): 11103–8. doi:10.1073/pnas.1305569110. PMC 3703977 Freely accessible. PMID 23690610
- Unanue ER (July 2013). "Perspectives on anti-CD47 antibody treatment for experimental cancer". Proc. Natl. Acad. Sci. U.S.A. 110 (27): 10886–7. doi:10.1073/pnas.1308463110. PMC 3704033 Freely accessible. PMID 23784781