Butyl-acetát
Butylacetát, přesněji n-butylacetát, je organická sloučenina patřící mezi estery, za pokojové teploty bezbarvá, hořlavá, kapalina. Vyskytuje se v řadě druhů ovoce, kde společně s dalšími látkami vytváří vůně a chuti, je například zodpovědný za chuti banánů a jablek. Přidává se jako ochucovadlo do potravin, jako jsou cukrovinky, zmrzliny, sýry a pečivo. Butylacetát také může sloužit jako vysokovroucí středně polární rozpouštědlo. Společně s ethylacetátem se používá jako rozpouštědlo v lacích na nehty.
| Butyl-acetát | |
|---|---|
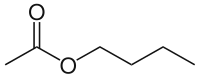
Strukturní vzorec | |
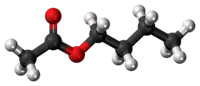
Model molekuly | |
| Obecné | |
| Systematický název | butylethanoát |
| Ostatní názvy | n-butylacetát |
| Funkční vzorec | CH3(CH2)3OCOCH3 |
| Sumární vzorec | C6H12O2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 123-86-4 |
| EC-no (EINECS/ELINCS/NLP) | 204-658-1 |
| PubChem | 31272 |
| ChEBI | 31228 |
| SMILES | CCCCOC(=O)C |
| InChI | 1S/C6H12O2/c1-3-4-5-8-6(2)7/h3-5H2,1-2H3 |
| Vlastnosti | |
| Molární hmotnost | 116,16 g/mol |
| Teplota tání | −78 °C (195 K)[1] |
| Teplota varu | 126 °C (399 K)[1] |
| Hustota | 0,875 g/cm3[1] |
| Rozpustnost ve vodě | 0,5 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v ethanolu a propan-1,2-diolu[1] |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v diethyletheru[1] |
| Tlak páry | 1,2 kPa (20 °C)[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H226 H336[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P261 P271 P280 P303+361+353 P304+340 P312 P370+378 P403+233 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Kromě nejčastěji se vyskytujícího nerozvětveného izomeru také existují rozvětvené izomery isobutylacetát, terc-butylacetát a sek-butylacetát.
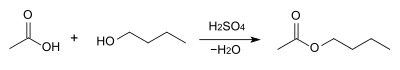
Výroba
Butylacetát se vyrábí Fischerovou–Speierovou esterifikací butan-1-olu (pro nerozvětvený izomer) nebo jeho izomeru (při výrobě rozvětveného izomeru) s kyselinou octovou za přítomnosti kyseliny sírové jako katalyzátoru:[2]
Výskyt
Část aromatu jablek vytváří butylacetát, ten je také obsažen ve feromonech včel.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Butyl acetate na anglické Wikipedii.
- https://pubchem.ncbi.nlm.nih.gov/compound/31272
- Acetic acid. (2003). In Ullman's encyclopedia of industrial chemistry (6th ed., Vol. 1, pp. 170-171). Weinheim, Germany: Wiley-VCH.