Peroxid vodíka
Peroxid vodíka (H2O2, HO-OH) je binárna zlúčenina kyslíka a vodíka. V molekule peroxidu vodíka sú atómy kyslíka viazané navzájom a na každom z nich je atóm vodíka, pričom väzby O-H sa nenachádzajú v jednej rovine.
| Peroxid vodíka | |||||||
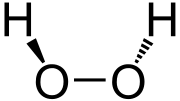 Peroxid vodíka | |||||||
| Všeobecné vlastnosti | |||||||
| Sumárny vzorec | H2O2 | ||||||
| Vzhľad | bezfarebná kvapalina | ||||||
| Fyzikálne vlastnosti | |||||||
| Teplota topenia | -0,43 °C | ||||||
| Teplota varu | 150,2 °C | ||||||
| Hustota | 1,11 g/cm³ (20 °C) | ||||||
| |||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||
Peroxid vodíka je bezfarebná kvapalina, s vodou neobmedzene miešateľná. Je silné oxidačné činidlo.
- H2O2 + 2H+ + 2e ↔ 2H2O
- HO2− + H2 + 2e ↔ 3OH−
Pri kontakte s horľavým materiálom môže spôsobiť požiar. Spôsobuje silné popáleniny a poleptanie.
Použitie
Bielenie celulózy, dezinfekcia v medicíne ako 3-percentný vodný roztok, leptanie v elektrotechnickom priemysle, pokovovanie, bielenie zubov, melírovanie, úprava pitnej a odpadovej vody, ako okysličovadlo v hypergolických palivových zmesiach.
Počas 2. Svetovej vojny sa Peroxid vodíka používal v nemeckých ponorkách typu "U 571" ako okysličovadlo pre spaľovacie motory pod hladinou. Čo umožňovalo vyvinutie rýchlosti až 20 uzlov oproti akumulátorom ktoré mohli vyvinuť rýchlosť iba 6 až 8 uzlov
Vplyvom katalyzátorov ako platina, burel alebo krv sa peroxid vodíka rozkladá na kyslík a vodu.
