Staphylococcus aureus
Staphylococcus aureus (také zlatý stafylokok) je grampozitivní bakterie patřící do rodu stafylokoků. Objevil ji v roce 1880 skotský chirurg Alexander Ogston v hnisu z otevřených poranění a o čtyři roky později ji německý bakteriolog F. Rosenbach dal latinský název. Způsobuje velmi často různé infekce v rozsahu od mírných zánětů kůže a měkkých tkání až po život ohrožující sepse („otravy krve“, směřující až do septického šoku spojeného se selháváním orgánů), syndrom toxického šoku a nekrotizující pneumonie. Patogenita této bakterie je výsledkem produkce toxinů (exfoliativní toxiny, enterotoxiny atd.), které způsobují ničení tkáně nemocného. Tvoří žlutý pigment (od toho odvozeno druhové jméno aureus – zlatý), zkvašuje mannitol a přibližně u třetiny lidské populace je přirozeně přítomen na kůži a sliznicích. Přenos genů antibiotikové rezistence (např. na plazmidech) mezi kmeny S. aureus se uskutečňuje nejčastěji transdukcí prostřednictvím temperovaných bakteriofágů z čeledi Siphoviridae.
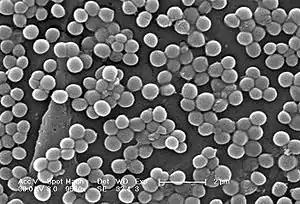 Zlatý stafylokok | |
| Vědecká klasifikace | |
| Doména | bakterie (Bacteria) |
| Kmen | Firmicutes |
| Třída | Bacilli |
| Řád | Bacillales |
| Čeleď | Staphylococcaceae |
| Rod | stafylokok (Staphylococcus) |
| Binomické jméno | |
| Staphylococcus aureus Rosenbach, 1884 | |
| Některá data mohou pocházet z datové položky. | |
Antigenní struktura
Antigenní strukturu tvoří několik částí:
- peptidoglykan – je složka buněčné stěny. Navozuje v těle tvorbu interleukinu-1 a opsonizačních látek. Aktivuje komplement, má endotoxinovou aktivitu a působí jako chemotaktický faktor. Na peptidoglykanu je navázána kyselina teichoová a protein A.
- kyselina teichoová – navozuje tvorbu protilátek.
- protein A – se váže na Fc fragment IgG, čehož se pak užívá v diagnostice u tzv. koaglutinační reakce. Dále inhibuje opsonizaci a fagocytózu – má antifagocytární a antikomplementární účinek.
- adheziny – jsou kolonizační faktory. Způsobují adhezi stafylokoků na mezibuněčné nebo buněčné struktury (např. fibrinogen, fibronektin, kolagen, sialoprotein)
- vázaná koaguláza – je shlukovací faktor a zprostředkovává vazbu na fibrinogen.
Patogenita
Patogenita se vyznačuje tvorbou extracelulárních proteinů (toxiny, enzymy). Toxiny patří mezi superantigeny. Známe tyto patogenní faktory:
- Stafylolyziny – patří sem hemolyzin alfa, beta, gama, delta. Jsou to cytotoxiny, které poškozují nejen erytrocyty, ale i buňky různých tkání. S. aureus a Staphylococcus haemolyticus způsobují beta-hemolýzu.
- Leukocidin – zvyšuje permeabilitu membrány leukocytů.
- Exfoliatin – je epidermolytický toxin typický pro S. aureus. Způsobuje syndrom opařené kůže (SSSS, Ritterův syndrom), což je toxická epidermolýza. Jedná se o těžké poškození kůže, při němž vznikají vodnaté puchýře, které postupně praskají a kůže se pak olupuje. Tekutina v puchýřích je sterilní.
- TSST-1 (toxic shock syndrome toxin) – jedná se o toxin syndromu toxického šoku, jehož hlavním projevem je multisystémový efekt (horečka, difúzní erytrém, průjmy, hypotenze, selhání funkce jater a ledvin). Zvyšuje propustnost endotelu.
- Enterotoxiny – způsobují stafylokokovou enterotoxikózu. Vyskytují se i v infikovaných potravinách, jsou termostabilní a odolné vůči kyselině chlorovodíkové v žaludku.
- Plazmokoaguláza (volná) – sráží fibrinogen. Vytváří ochranný fibrinový obal a napomáhá tím k tvorbě abscesů.
- Hyaluronidáza – je faktor invazivity. Napomáhá tvorbě flegmóny. Štěpí kyselinu hyaluronovou a pomáhá pronikání stafylokoků do mezibuněčných prostor.
- Stafylokináza – je fibrinolyzin, který rozpouští fibrinové sraženiny.
- Lipázy – hydrolyzují lipidy a způsobují tak lepší šíření do podkoží.
- Nukleáza – její úloha je zatím v patogenezi nejasná. Využívá se v laboratorní diagnostice.
- Penicilináza – je beta-laktamáza kódovaná genem bla lokalizovaném často na plazmidech. Štěpí beta-laktamový kruh beta-laktamových antibiotik.
Klinický obraz
Syndrom opařené kůže
- viz exfoliatin
Syndrom toxického šoku
- viz TSST-1
Stafylokoková enterotoxikóza
- jedná se o otravu z potravy kontaminované termostabilním enterotoxinem B (majonézové saláty, sekaná atd.)
Stafylokoková enterokolitida
- u nemocných léčených širokospektrými antibiotiky může dojít k přemnožení stafylokoků s tvorbou enterotoxinu B a vzniku enterokolitidy
Stafylokokové impetigo bullosa
- lokalizovaná forma SSSS, u dětí a dospělých vznikají puchýře s hnisem
Další infekce
- absces (ohraničená dutina naplněná hnisem), hnisavá onemocnění mazových folikulů a mazových žlázek (folikulitida, furunkl, karbunkl), ranné infekce, infekce popálenin, tonsilitidy, otitidy, pneumonie, meningitidy, empyém, endokarditidy, osteomyelitidy, puerperální sepse, septikémie s metastázemi do různých orgánů, pemphigus. Pro vznik onemocnění je důležitá vysoká infekční dávka a snížená funkce imunitního systému (při popáleninách, traumatech kůže, tumorech, alkoholismu, DM atd.).
Epidemiologie
Výskyt přenašečství je asi 20-50 % populace, přičemž u zdravotnického personálu bývá nález stafylokoků vyšší. Léčba přenašečů antibiotiky nebývá úspěšná.
Kultivace
Využívá se krevní a slaný agar, mikroskopie, průkaz pigmentu, test na plasmokoagulázu, katalázový test, latexová aglutinace a štěpení mannitolu.
Katalázový test
- odliší stafylokoky od streptokoků; po smíchání kolonie stafylokoka s peroxidem vodíku dochází k uvolňování bublinek – katalázapozitivní
Průkaz vázané koagulázy
- průkaz clumping faktoru na sklíčku; orientačně odliší S. aureus od Staphylococcus epidermidis
Průkaz volné koagulázy
- jedná se o zkumavkovou metodu k odlišení koagulázapozitivních stafylokoků. Pokud dojde po smíchání kolonie s králičí plazmou ke koagulaci plazmy, jedná se o stafylokoky koagulázapozitivní
Latexová aglutinace
- používá se k odlišení MRSA od koagulázanegativních stafylokoků
Léčba
Lokalizované infekce se mohou řešit chirurgicky. Přibližně 90% stafylokoků je rezistentních na běžný penicilin. Tudíž se musejí používat tzv. peniciliny inhibující beta-laktamázu (oxacilin/meticilin nebo cloxacilin s AMP). Dále se používají makrolidy, cefalosporiny I. a IV. generace, aminoglykosidy, linkosamidy, tetracykliny, glykopeptidy, chloramfenikol, fluorochinolony (+doplněk Stasea = stafylokokový antitoxin). V případě přenašectví se používá lokální antibiotikum mupirocin.
MRSA
Jedná se o meticilin-rezistentní kmeny Staphylococcus aureus. Poprvé byly objeveny v roce 1961 krátce po zavedení meticilinu (jakožto polosyntetického derivátu penicilinu) do klinické praxe. Od té doby se jejich procentuální zastoupení v populacích kmenů S. aureus zvyšuje a v současnosti představují celosvětově závažný problém ve zdravotnictví při léčbě stafylokokových infekcí. Rezistenci k meticilinu (a potažmo ke všem β-laktamovým antibiotikům) zajišťuje gen mecA lokalizovaný na stafylokokové chromozomální kazetě SCCmec. Gen mecA kóduje alternativní transpeptidázu (PBP2a nebo také PBP2', PBP = penicillin binding protein), což je enzym zodpovědný za syntézu buněčné stěny bakterie. Tato alternativní transpeptidáza není inaktivována antibiotiky jako je penicilin nebo meticilin, a buňka je tedy vůči těmto antibiotikům rezistentní. Kromě genu pro rezistenci k meticilinu nesou tyto kmeny obvykle ještě další geny pro rezistenci k jiným antibiotikům (např. k tetracyklinu, streptomycinu, chloramfenikolu), což představuje poměrně závažný problém při léčbě onemocnění způsobených kmeny MRSA. Léčba probíhá podáváním antibiotik, ke kterým je tato bakterie citlivá, což jsou např. glykopeptidy vankomycin a teikoplanin nebo syntetický oxazolidinon linezolid. Kmeny MRSA se kultivují na agaru MRSA select – více NaCl+oxacilin+cefoxitin+fungicidin. U diskové metody se objeví malá inhibiční zóna u oxacilinu, avšak za průkazné se považuje, když je malá zóna také u cefoxitinu.
Prevence
Pacientům může být aplikována ke stimulaci specifické imunity vakcína Polystafana (stafylokokový anatoxin) nebo Staphage lysate (lyzát stafylokokové kultury).
Literatura
- MURRAY, Patrick R.; ROSENTHAL, Ken S.; PFALLER, Michael A. Medical Microbiology, Fifth edition. [s.l.]: Elsevier, 2005.
- HORÁČEK, Jiří. Základy lékařské mikrobiologie. [s.l.]: Karolinum, 2000.