Tetraacetylethan
Tetraacetylethan je organická sloučenina se vzorcem [CH(C(O)CH3)2]2. Používá se na přípravu heterocyklických a komplexních sloučenin. Získává se oxidací acetylacetonátu sodného:[1]
- I2 + 2 NaCH(C(O)CH3)2 → [CH(C(O)CH3)2]2 + 2 NaI
| Tetraacetylethan | |
|---|---|
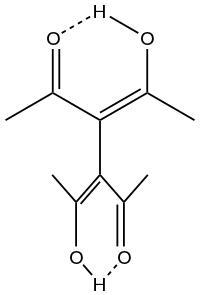
Strukturní vzorec | |
| Obecné | |
| Systematický název | 3,4-diacetyl-hexan-2,5-dion |
| Sumární vzorec | C10H14O4 |
| Vzhled | bílá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 5027-32-7 |
| PubChem | 78730 |
| SMILES | CC(=O)C(C(C(=O)C)C(=O)C)C(=O)C |
| InChI | 1S/C10H14O4/c1-5(11)9(6(2)12)10(7(3)13)8(4)14/h9-10H,1-4H3 |
| Vlastnosti | |
| Molární hmotnost | 198,22 g/mol |
| Teplota tání | 192 až 193 °C (465 až 466 K) |
| Hustota | 1,305 g/cm3 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Podobně jako acetylaceton se tetraacetylethan vyskytuje v enolové formě. Dva C3O2H kruhy jsou vzájemně pootočeny o úhel blízký 90°.[2]
Je známa řada komplexů konjugované zásady tetraacetylethanu, například diruthenitý derivát [Ru(acac)2]2[C(C(O)CH3)2]2, podobný acetylacetonátu ruthenitému.[3]
Reference
V tomto článku byl použit překlad textu z článku Tetraacetylethane na anglické Wikipedii.
- Robert G. Charles. Tetraacetylethane. Organic Syntheses. 1959, s. 61. DOI 10.15227/orgsyn.039.0061.
- Paula M. B. Piccoli, Thomas F. Koetzle, Arthur J. Schultz, Elizabeth A. Zhurova, Jernej Stare, A. Alan Pinkerton, Juergen Eckert, Dusan Hadzi. Variable Temperature Neutron Diffraction and X-Ray Charge Density Studies of Tetraacetylethane. The Journal of Physical Chemistry A. 2008, s. 6667-6677. DOI 10.1021/jp800204r.
- Tomohiro Koiwa, Yuki Masuda, Junpei Shono, Yuji Kawamoto, Yoshimasa Hoshino, Takeshi Hashimoto, Karuppannan Natarajan, Kunio Shimizu. Synthesis, Characterization, and Detailed Electrochemistry of Binuclear Ruthenium(III) Complexes Bridged by Bisacetylacetonate. Crystal and Molecular Structures of [{Ru(acac)2}2(tae)] (Acac = 2,4-Pentanedionate Ion, tae = 1,1,2,2-Tetraacetylethanate Dianion). Inorganic Chemistry. 2004, s. 6215-6223. DOI 10.1021/ic030216c. PMID 15446866.
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.