p-kresol
p-Kresol (tj. para-kresol; systematický název 4-methylfenol), je organická sloučenina, isomer kresolu (CH3C6H4OH). Tato bezbarvá pevná látka se často používá na přípravu dalších sloučenin. Jedná se o methylovaný derivát fenolu a polohový izomer o-kresolu a m-kresolu.
| p-kresol | |
|---|---|
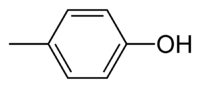
Strukturní vzorec | |
Model molekuly | |
| Obecné | |
| Systematický název | 4-methylfenol |
| Ostatní názvy | p-kresol, 4-methylhydroxybenzen |
| Funkční vzorec | C6H4OH-4-CH3 |
| Sumární vzorec | C7H8O |
| Vzhled | bezbarvá pevná látka[1] |
| Identifikace | |
| Registrační číslo CAS | 106-44-5 |
| EC-no (EINECS/ELINCS/NLP) | 203-398-6 |
| PubChem | 2879 |
| ChEBI | 17847 |
| SMILES | Cc1ccc(O)cc1 |
| InChI | 1/C7H8O/c1-6-2-4-7(8)5-3-6/h2-5,8H,1H3 |
| Číslo RTECS | GO6475000 |
| Vlastnosti | |
| Molární hmotnost | 108,14 g/mol |
| Teplota tání | 35,5 °C (306,6 K)[1] |
| Teplota varu | 201,9 °C (474,0 K)[1] |
| Hustota | 1,034 g/cm3 (20 °C)[1] |
| Viskozita | 4,48 mPa.s (50 °C)[1] |
| Index lomu | 1,5395 (20 °C)[1] |
| Disociační konstanta pKa | 10,26[1] |
| Rozpustnost ve vodě | 2,15 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v ethanolu, acetonu a glycerolu[1] |
| Rozpustnost v nepolárních rozpouštědlech |
rozpustný v diethyletheru, tetrachlormethanu, benzenu a rostlinných olejích[1] |
| Tlak páry | 15 Pa[1] |
| Měrná magnetická susceptibilita | −6,67×105 μm3/g |
| Povrchové napětí | 34,0 mN/m (50 °C)[1] |
| Termodynamické vlastnosti | |
| Standardní molární spalná entalpie ΔH°sp | −3701 kJ/mol[1] |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H301 H311 H314[1] |
| P-věty | P260 P264 P270 P280 P301+310 P301+330+331 P302+352 P303+361+353 P304+340 P305+351+338 P310 P312 P321 P322 P330 P312 P361 P363 P405 P501[1] |
| Teplota vzplanutí | 85 °C (358 K)[1] |
| Teplota vznícení | 555 °C (828 K)[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Výroba
p-Kresol se obvykle, spolu s řadou dalších látek, získává z uhelného dehtu, získávaného při výrobě koksu. Vedlejší produkty této výroby obsahují několik procent fenolu a kresolů. Také se vyrábí průmyslově ve dvou krocích, kdy prvním je sulfonace toluenu,[2]
- CH3C6H5 + H2SO4 → CH3C6H4SO3H + H2O
po které následuje zásaditá hydrolýza vzniklé sulfonátové soli za vzniku sodné soli kresolu:
- CH3C6H4SO3H + 2 NaOH → CH3C6H4OH + Na2SO3 + H2O
Lze také použít chloraci toluenu následovanou hydrolýzou nebo cymenový-kresolový proces, při němž je toluen alkylován propenem za vzniku 'p-cymenu, který je poté oxidačně dealkylován; tento postup je podobný kumenovému procesu.
Použití
p-Kresol se nejčastěji používá na výrobu antioxidantů, jako například butylhydroxytoluenu (BHT). Monoalkylované deriváty mohou sloužit jako suroviny na výrobu difenolových antioxidantů, které se používají velmi často díky nízké toxicitě a také díky tomu, že nevytvářejí barevné skvrny.
Výskyt
Reference
V tomto článku byl použit překlad textu z článku p-Cresol na anglické Wikipedii.
- P-Cresol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- W. W. Hartman. p-Cresol. Organic Syntheses. 1923, s. 37. DOI 10.15227/orgsyn.003.0037.
- H. M. Hamer; V. De Preter; K. Windey; K. Verbeke. Functional analysis of colonic bacterial metabolism: relevant to health?. American Journal of Physiology. Gastrointestinal and Liver Physiology. 2012, s. G1-9. DOI 10.1152/ajpgi.00048.2011. PMID 22016433.
- E. A. Hallem; A. Nicole Fox; L. J. Zwiebel; J. R. Carlson. Olfaction: mosquito receptor for human-sweat odorant. Nature. 2004, s. 212–213. DOI 10.1038/427212a. PMID 14724626. Bibcode 2004Natur.427..212H.
- J. R. Linley. Laboratory tests of the effects of p-cresol and 4-methylcyclohexanol on oviposition by three species of Toxorhynchites mosquitoes. Medical and Veterinary Entomology. 1989, s. 347–352. DOI 10.1111/j.1365-2915.1989.tb00241.x. PMID 2577519.
- R. Talhout; T. Schulz; E. Florek; J. van Benthem; P. Wester; A. Opperhuizen. Hazardous compounds in tobacco smoke. International Journal of Environmental Research and Public Health. 2011, s. 613–628. DOI 10.3390/ijerph8020613. PMID 21556207.
- Brendan Borrell. Why study pig odor? [online]. [cit. 2009-03-05]. Dostupné online.
- L. E. Rasmussen; T. E. Schulz. Physiological correlates of musth: lipid metabolites and chemical composition of exudates. Physiology & Behavior. 1999, s. 539–549. DOI 10.1016/S0031-9384(99)00114-6. PMID 10549891.
- Deepa Ananth. Musth in elephants. Zoos' Print Journal. 2000, s. 259–262. DOI 10.11609/jott.zpj.14.4.259-62.

