Organický peroxid
Organické peroxidy jsou organické sloučeniny obsahující peroxidovou funkční skupinu (ROOR'). Je-li R' vodík, sloučenina se nazývá organický hydroperoxid. Perestery mají obecnou strukturu RC(O)OOR.
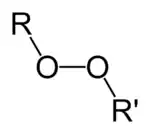
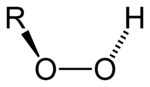
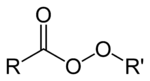
Vazba O-O se snadno rozpadá a tvoří volné radikály v podobě RO·. Proto jsou organické peroxidy užitečné jako iniciátory některých druhů polymerizací, například u epoxidových pryskyřic použitých pro skelné lamináty. K tomuto účelu se obvykle používají MEKP a benzoylperoxid. Uvedené vlastnosti však také znamenají, že organické peroxidy mohou záměrně nebo nechtěně iniciovat explozivní polymerizaci látek s nenasycenými chemickými vazbami - tento proces se využívá ve výbušninách[1].
Většina organických peroxidů jsou vysoce hořlavé a výbušné látky, často reaktivní a těkavé. Již 5 mg diethyletherperoxidu může roztříštit skleněnou chemickou soupravu. Organické peroxidy, podobně jako jejich anorganické obdoby, jsou účinnými bělidly.
Syntéza
Peroxidy lze syntetizovat v laboratoři řadou různých cest:
- peroxykyseliny oxidací karboxylových kyselin peroxidem vodíku
- peroxykyseliny oxidací a hydrolýzou Grignardových čiínidel
- peroxidy fotooxidací dienů
- peroxidy oxymerkurací alkenů s následnou reakcí s hydroperoxidem
- peroxykyseliny reakcí alkylhalogenidů s peroxidem vodíku
Reakce
Některé peroxidové reakce jsou:
- organická redukce na alkoholy hydridem lithnohlinitým nebo estery kyseliny fosforité
- štěpení na ketony a alkoholy v zásadou katalyzovaném Kornblumově–DeLaMareově přesmyku
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu organický peroxid na Wikimedia Commons
Obrázky, zvuky či videa k tématu organický peroxid na Wikimedia Commons - OSH Answers - organic peroxides
- Carolina Biological: The Perils of Peroxides
- Peroxide disposal
Reference
V tomto článku byl použit překlad textu z článku Organic peroxide na anglické Wikipedii.
- See for example the 2006 transatlantic aircraft plot.