Cryptosporidium
Cryptosporidium je rod jednohostitelských kokcidií kmene Apicomplexa vyskytujících se u savců, ptáků a plazů.[1]
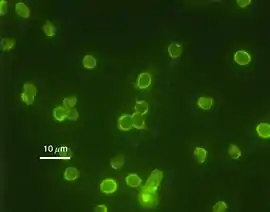 Oocysty Cryptosporidium parvum při imunoflouerescenci | |
| Vědecká klasifikace | |
| Doména | Eukaryota |
| (nekategorizováno) | Chromalveolata |
| Podkmen | výtrusovci (Apicomplexa) |
| Třída | Conoidasida |
| Podtřída | kokcidie (Coccidiasina) |
| Řád | Eucoccidiorida |
| Podřád | Eimeriorina |
| Čeleď | Cryptosporidiae |
| Rod | Cryptosporidium Tyzzer 1907 |
| Některá data mohou pocházet z datové položky. | |
Všechna vývojová stádia se vyvíjí intracelulárně, tj. uvnitř buňky, ale extracytoplazmaticky, tj. uvnitř vlastní parazitoforní vakuoly. Parazitují v buňkách sliznic, nejčastěji trávicího systému, méně často ve výstelce dýchacího systému, v játrech, slinivce břišní, žlučníku, na oční spojivce aj.[1]
Při nepohlavním množení, tzv. merogonii, dochází k tvorbě dvou odlišných typů merontů. Typ I. obsahuje 6–8 jader. Po dozrání z každého jádra vzniká merozoit a ten napadá další slizniční buňku. V následující generaci vznikají opěty meronty I. typu nebo morfologicky odlišné meronty II. typu, které produkují pouze 4 merozoity.[1]
Při následné gametogonii, tj, pohlavním množení, se většina vzniklých zygot vyvíjí v tzv. silnostěnné oocyty, které sporulují v parazitoforní vakuole hostitelské buňky. Tyto oocysty odcházejí ze zažívacího traktu trusem. Část tzv. tenkostěnných oocyst zažívací trakt neopouští, snáze praskají a uvolněné sporozoity opakovaně zahajují endogenní cyklus – merogonii (autoinfekce). Oocysty měří mezi 2–10 µm. Oocysty kryptosporidií obsahují 4 volně uložené sporozoity a poměrně velké reziduální tělísko. Nemají mikropyle a jejich stěna je téměř bezbarvá. Jsou téměř kulaté, silně světlolomné.[1]
Endogenní vývoj probíhá v tenkém střevě. Oocysty jsou pozřeny s potravou, vodou, z vnějšího prostředí nebo inhalovány vhodným hostitelem. Sporozoity pronikají slizničními buňkami zažívacího traktu. Mají však schopnost se uvolňovat z oocysty i spontánně, což částečně vysvětluje, proč kryptosporidie mohou infikovat tkáně mimo zažívací trakt, např. oční spojivku či dýchací systém. Prepatentní perioda je různě dlouhá, zpravidla 2–10 dní a to jak v závislosti na hostitelském druhu, ale i na druhu kryptosporídií.[1]
Diagnostika se provádí ze vzorků trusu, resp. stolice (u lidí), často se využíví koncentrační metody dle Sheathera. Dále je možné detekovat oocysty v nátěrech trusu s následným barvením oocyst barvením dle Ziehl-Nielsena, negativním barvením dle Heineho, barvením dle Baxbyho et al. nebo barvením dle Miláčka a Vítovce. Posmrtně lze oocysty diagnostikovat v histologických řezech a seškrabech sliznice tenkého střeva. Po barvení v hematoxilin-eozinu se kryptosporidie jeví jako drobná, sférická tělíska o velikosti 2–5 um, nacházející se v zóně kartáčového lemu střevních slizničních buněk, kde se barví bazofilně (toto platí u druhů parazitujících u savců). Oocysty lze detekovat také pomocí imunofluorescence s využitím monoklonálních protilátek (MAbs). Dále lze užít techniky PCR nebo RFLP (Restriction Fragment Lenght Polymorpism, fingerprinting) metodu u získaných izolátů C. parvum.[1]
Teplota a vlhkost umožňují oocystám dlouhou dobu životaschopnosti, zůstávají infekční až po dobu 1 roku. Oocysty kryptosporidií spolehlivě ničí peroxid vodíku a chlordioxid, vysoké teploty (65 °C po 20 minut) a zmrazení. Ozonizace vody také napomáhá devitalizaci oocyst kryptosporidií. Jejich vitalitu také ovlivňuje UV záření, přičemž přirozené sluneční záření se tak stává váznamným faktorem, který dezinfikuje vnější prostředí.
K terapii se užívá podpůrná a symptomatická léčba. Užití rehydratačních roztoků je nezbytné k zamezení dehydratace postiženého organismu. U telat často včasné podání kolostra od hyperimunizovaných krav může symptomy onemocnění zmírnit. U plně imunitně vybavených jedinců tura domácího dochází často k samovyzdravení (tzv. fenomén selfcure). K preventivní aplikaci i terapii onemocnění u lidí a zvířat byly ověřovány salinomycin, sulfaquinoxalin, amprolium, dinitolamid a paromomycin. U telat byla zkoušena i perorální vakcinace oocystami. Specifická terapie však dosud není vyřešena.[1]
Druhy Cryptosporidium hominis a C. parvum genotyp 1 jsou významnými parazity člověka. Přenáší se nejčastěji kontaminovanou vodou, zeleninou, přímým kontaktem s infikovaným jedincem, jakož i dalšími cestami. U lidí způsobuje akutní průjmové onemocnění a bolesti břicha, které u imunokompetentních lidí odezní zpravidla do týdne. U imunokompromitovaných jedinců (např. HIV pozitivní) je průběh závažnější, průjmy jsou chronického charakteru a nemoc může končit i fatálně.[2]
Další běžné druhy jsou Cryptosporidium muris, Cr. bailey, Cr. meleagridis, Cr. saurophilum, Cr. serpentis.[1][3]
Reference
- CHROUST, Karel; LUKEŠOVÁ, Daniela; MODRÝ, David. Veterinární protozoologie. 1. vyd. Brno: Ediční středisko VFU, 1998. 113 s. ISBN 80-85114-27-5. S. 84–87.
- BOUZID, Maha; HUNTER, Paul R.; CHALMERS, Rachel M. Cryptosporidium Pathogenicity and Virulence. Clinical Microbiology Reviews. 2013-01-01, roč. 26, čís. 1, s. 115–134. PMID: 23297262. Dostupné online [cit. 2017-07-19]. ISSN 0893-8512. DOI 10.1128/cmr.00076-12. PMID 23297262. (anglicky)
- BECK, WIELAND. Praktische Parasitologie bei Heimtieren : Kleinsäuger - Vögel - Reptilien - Bienen. Hannover: Schlütersche x, 317 Seiten s. Dostupné online. ISBN 3-89993-017-7, ISBN 978-3-89993-017-7. OCLC 181489246