Chlorid vanadičný
Chlorid vanadičný, VCl5, je černá pevná látka. Vytváří dimerní molekuly, vanad má oktaedrickou koordinaci. Oba oktaedry jsou propojeny hranou.[1]
| Chlorid vanadičný | |
|---|---|
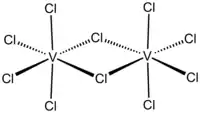
Strukturní vzorec dimeru chloridu vanadičného | |
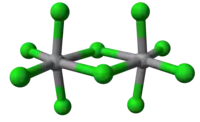
Krystalová struktura V2Cl10 | |
| Obecné | |
| Systematický název | Chlorid vanadičný |
| Anglický název | Vanadium(V) chloride |
| Německý název | Vanadium(V)-chlorid |
| Sumární vzorec | V2Cl10 |
| Vzhled | černá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 1421358-80-6 |
| PubChem | 13643901 |
| SMILES | Cl[V](Cl)(Cl)(Cl)Cl dimer: Cl[V-]1(Cl)(Cl)(Cl)[Cl+][V-]([Cl+]1)(Cl)(Cl)(Cl)Cl |
| InChI | 1S/5ClH.V/h5*1H;/q;;;;;+5/p-5 |
| Vlastnosti | |
| Molární hmotnost | 456,38 g/mol |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava a reakce
VCl5 lze připravit reakcí fluoridu vanadičného s nadbytkem chloridu boritého:
- 2 VF5 + 10 BCl3 → [VCl5]2 + 10 BF2Cl
Je nestabilní, za pokojové teploty se rozkládá na chlorid vanadičitý a chlor:
- [VCl5]2 → 2 VCl4 + Cl2
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Vanadium(V) chloride na anglické Wikipedii.
- TAMADON, Farhad; SEPPELT, Konrad. The Elusive Halides VCl 5 , MoCl 6 , and ReCl 6. Angewandte Chemie International Edition. 2013-01-07, roč. 52, čís. 2, s. 767–769. Dostupné online [cit. 2022-01-22]. DOI 10.1002/anie.201207552. (anglicky)
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.