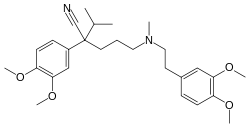
Blokátory vápníkového kanálu
Blokátory vápníkového kanálu (dále jen BVK) nebo také antagonisté vápníkového kanálu (angl. calcium channel blocker) [1] jsou širokou skupinou léčiv, jejichž účinek je podmíněn omezením vstupu vápníkových iontů (Ca2+) skrze buněčný vápníkový kanál, čímž následně dojde k terapeuticky využitelným fyziologickým změnám.[2] BVK jsou využívány především za účelem snížení krevního tlaku (hypertenze), protože zlepšují "pružnost" krevních cév, resp. zvyšují tzv. průsvit cév, a tak dochází ke snížení cévního odporu, který patologicky zúžené cévy kladou toku krve. Tento cévní odpor je nutné "překonávat" pomocí zvýšené srdeční práce (vyšší síla stahu -kontrakce- srdeční svaloviny tj. myokardu), čímž se tlak krve zvýší. BVK jsou tedy schopny vazodilatace.[3] BVK jsou dále využívány za účelem snížení bolesti na hrudi způsobenou anginou pectoris. Speciálnější indikací je zabránění tzv. cerebrálním vazospasmům, což je stav, kdy dojde ke křečovitému stažení (kontrakci) delších komunikačních cév, které procházejí v oblastech pod mozkovou plenou. Toto stažení je fyziologickou odpovědí na krvácení, způsobené prasknutím tepenné výdutě v mozku, tj. ruptury aneurysmatu.
Kromě působení BVK na cévní stěnu, mohou tyto léčiva ovlivňovat tlak krve i jinými fyziologickými mechanismy. Vápníkové kanály jsou totiž obsažené rovněž v tzv. zona glomerulosa, tedy nejvrchnější části kůry nadledvin, která je umístěna těsně pod pouzdrem nadledviny. Blokování vápníkových kanálů v těchto místech může pozitivně působit na snížení sekrece aldosteronu, a tak ovlivnit zvýšený krevní tlak, který je spojen s tzv. hyperaldosteronismem (patologicky zvýšená míra produkce aldosteronu, vedoucí mj. k nižší hladině draslíku v krvi, tj. hypokalémii a vyššímu tlaku krve).[4]
Navzdory vysoké účinnosti BVK, je důležité při jejich podávání zvážit farmakokinetické účinky vybrané látky, a to z důvodu zjištění, že dlouhodobé užívání krátkodobě působících BVK je spojeno se statistickým zvýšením míry úmrtnosti oproti kontrolním skupinám, které krátkodobě působící BVK neužívaly.[5]
Historie

Objev BVK je spojen se jménem německého farmakologa a fyziologa Albrechta Fleckensteina, který poprvé v roce 1964 objevil tlumivý vliv prenylaminu a verapamilu na tzv. elektromechanické spřažení.[6] Přičemž elektromechanickým spřažením ve fyziologii rozumíme převod elektrického impulzu (obvykle akčního potenciálu) na mechanický kontrakční účinek svalového vlákna (angl. excitation–contraction coupling).
Mechanismus účinku
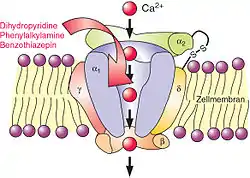
Ve tkáních (nejen) lidského organismu je za běžného fyziologického stavu koncentrace vápníkových iontů na vnější straně buněčné membrány (Ca2+) přibližně 1000násobná oproti koncentraci těchto iontů uvnitř buněk. Za určitých podmínek (většinou při změně napětí na membráně – viz akční potenciál) jsou schopny u některých buněk přestoupit vápníkové ionty z vnějšku buněčné membrány dovnitř buňky. Tento přestup (transport) iontů zajišťují právě vápníkové kanály, které jsou umístěné v buněčné membráně. I velmi malý počet prostupujících iontů vyvolá následné fyziologické změny, které závisí na tom, o jakou buněčnou strukturu se jedná, resp. o kterou tkáň se jedná. BVK zabraňují prostupu vápníkových iontů jejich kanálem, a proto znemožňují efekt, který je výsledkem fyziologických změn navozených ionty vápníku. Nejčastěji dochází ke snížení excitability zasažených tkání.
Vzhledem k tomu, že existuje několik typů vápníkových kanálů (L-typ, T-typ, N-typ, P-typ), je důležité, na který z těchto typů se BVK zaměřují. Klíčovou fyziologickou roli v oblasti kardiovaskulárního systému hraje L-typ (L z angl. long) vápníkového kanálu, protože je zodpovědný za trvání stahu svalových vláken, a to jak uvnitř cév, tak myokardu. To je dáno tím, že omezení vstupu vápníkových iontů zkracuje tzv. plató fázi srdečního akčního potenciálu, což je fáze, kdy srdeční sval zůstává v depolarizované fázi.[7] Síla srdečního stahu je BVK omezena jak fyziologickým mechanismem, kterým vápníkové ionty aktivují tzv. elektromechanické spřažení, tak snížením excitability (budivosti) sinoatrialního uzlu, který je pacemakerem srdečního rytmu. Všeobecně lze říct, že BVK snižují elektrickou vzrušivost celého převodního systému srdce, a tak zpomalují vedení vzruchu tímto systémem (tzv. dromotropní efekt). Důležitý je také výše zmíněný endokrinologický efekt, kdy BVK omezují vyplavování aldosteronu a kortizolu z endokrinních buněk přítomných v kůře nadledvin.[4]
Lze shrnout, že BVK:
- působí na hladkou svalovinu cév, snižují kontrakci tepen a zvětšují průměr a pružnost cév. Tím dochází k vazodilataci a snížení tlaku krve. Důležité je, že tento efekt se neprojevuje na hladké svalovině žil.
- působí na myokard a snižují jeho kontraktibilitu (stažlivost), čímž spoří spotřebu kyslíku, a tak omezují ischemické projevy anginy pectoris. Tento efekt však představuje riziko pro nemocné s kardiomyopatií, protože podáním BVK (zejména ze skupin fenylalkylaminů a benzotiazepinů) dochází ke snížení funkční aktivity již oslabené funkce srdečního svalu.
- snižují budivost převodního systému srdečního (lze využít v léčbě nepravidelného srdečního rytmu, jehož původ je na úrovni srdečních síní -viz arytmie, fibrilace síní).
- redukují vyplavování aldosteronu, čímž posilují svůj hlavní efekt při snižování tlaku krve.
Rozdělení BVK
dihydropyridiny
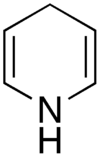
Dihydropidinové BVK jsou odvozeny od molekuly dihydropyridinu a jejich indikací je vysoký krevní tlak spojený se zvýšením krevního odporu cév. Pokud jsou užity v léčbě anginy pectoris, může navozená vazodilatace a snížení krevního tlaku (až hypotenze) vést k fyziologickému zpětnovazebnímu jevu nazvanému reflexní tachykardie, kdy dojde k opětovnému zvýšení tlaku zvýšením tepové frekvence. Tato reakce může způsobit zhoršení příznaků anginy pectoris, protože zvýšená tepová frekvence zvyšuje spotřebu kyslíku srdeční tkání, čímž ještě více zhoršuje původní ischemické projevy tohoto onemocnění. U nemocných s nefropatií dihydropyridiny zvyšují vylučování bílkoviny do moče (proteinurie).
Názvy látek této skupiny končí příponou -dipin.
Patří sem:
- Amlodipin (Norvasc)
- Aranidipin (Sapresta)
- Azelnidipin (Calblock)
- Barnidipin (HypoCa)
- Benidipin (Coniel)
- Cilnidipin (Atelec, Cinalong, Siscard) (Není schválen pro USA)
- Clevidipin (Cleviprex)
- Isradipin (DynaCirc, Prescal)
- Efonidipin (Landel)
- Felodipin (Plendil)
- Lacidipin (Motens, Lacipil)
- Lercanidipin (Zanidip)
- Manidipin (Calslot, Madipine)
- Nicardipin (Cardene, Carden SR)
- Nifedipin (Procardia, Adalat)
- Nilvadipin (Nivadil)
- Nimodipin (Nimotop) prochází hematoencefalickou bariérou, a je proto užíván za účelem předcházení cerebrálních vazospasmů (viz výše v textu)
- Nisoldipin (Baymycard, Sular, Syscor)
- Nitrendipin (Cardif, Nitrepin, Baylotensin)
- Pranidipin (Acalas)
Mezi častější vedlejší účinky dihydropyridinů patří:
- závratě, bolesti hlavy, zčervenání ve tváři
- otok nohou a kotníků
- tachykardie
- zácpa
- hyperplazie dásní
fenylalkylaminy
Terapeutika z této skupiny vykazují tzv. kardioselektivitu, která je výhodná v léčbě anginy pectoris, protože díky nízkému účinku na cévách nedochází k reflexní tachykardii, která zvyšuje spotřebu kyslíku srdeční tkání, a tím zhoršuje ischemické projevy onemocnění. V případě fenylalkylaminů se jedná o tzv. negativní inotropii, což znamená snížení kontraktility (stažlivosti) srdečního svalu, což vede k "úsporám" spotřeby kyslíku a snížení ischemických projevů anginy pectoris. Příčinou negativní inotropie způsobené fenylalkylaminy je ovlivnění depolarizační fáze akčního potenciálu, způsobujícího řízené stahování a uvolňování srdečního svalu skrze převodní systém srdeční. Jde tedy o ovlivnění excitability (budivosti) buněk převodního systému srdce, tím, že je ovlivňován vstup vápníkových iontů do vápníkových kanálů těchto buněk, čímž je zmírněna excitabilita převodního systému srdečního a tím i výsledná síla stahu.[8]
Mezi fenylalkylaminy patří:
- Verapamil (Calan, Isoptin)
- Gallopamil
- Fendiline
Vedlejší účinky jsou obdobné jako u předchozí skupiny.
benzotiazepiny
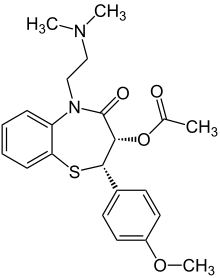
Chemicky jde o tiazepiny s přidruženým benzenem. Svým působením ve smyslu orientace účinku na srdce a cévy stojí uprostřed mezi fenylalkylaminy a dihydropyridiny (zlepšují jak pružnost cév, tak snižují kontraktibilitu (stažlivost) srdeční tkáně) . Z vyrovnaného působení vyplývá menší sklon k navození reflexní tachykardie.
Patří sem:
- Diltiazem (Cardizem – lze ho použít také v profylaxi migrény)
Vedlejší účinky jsou podobné jako u ostatních skupin.
neselektivní BVK
Většina léčiv z předchozí skupiny vykazovala zvýšenou selektivitu vůči kardiovaskulárnímu systému, nicméně existují BVK, které jsou neselektivní a zasahují více orgánů a systémů najednou. Například ty BVK, které jsou schopny prostoupit hematoencefalickou bariéru umožňují působení BVK v oblasti mozku, kde mohou být blokovány různé typy vápníkových kanálu, a to jak na neuronu, tak místních cévách. Např. flunarizin vykazuje účinky antimigrenózní, a také snižuje závratě (má antivertiginózní účinek). Dále účinkuje jako přídatné léčivo u některých druhů epilepsie (neuronální působení). Na druhou stranu neselektivita takového léčiva může rozšířit rejstřík vedlejších účinků. Mezi další neselektivní BVK patří mibefradil, bepridil či fendilin. [9] [10]
jiné
Gabapentinoidy jako např. gabapentin a pregabalin jsou blokátory napěťově řízených vápníkových kanálů, které obsahují α2δ podjednotku (CACNA2D1). Jsou určeny především k léčbě epilepsie a neuropatické bolesti.
Ziconotid je peptidová sloučenina odvozená od omega-conotoxinu, která vykazuje selektivitu vzhledem k N-typu vápníkového kanálu. Jde o mimořádně silné analgetikum s přibližně tisícinásobným účinkem oproti morfiu. Aby byl účinný, musí být vpravován intratekální infuzní pumpou. Tato látka je příkladem terapeutika, které působí na vápníkový kanál (N-typ), pro nějž je charakteristické umístění na neuronu, kde hraje důležitou roli ve vyplavování neurotransmiterů do synaptické štěrbiny.
Toxicita
Mírné předávkování BVK vyžaduje pouze podpůrnou terapii (supportive care). Závažný průběh předávkování mohou navodit ty BVK, která nepatří mezi dihydropyridiny (nebezpečný účinek na srdce). Proto je důležité zajistit včasné odstranění těchto BVK z organismu, zejména těch, které mají dlouhodobý účinek (delší vylučovací poločas). Při závažném předávkování, je důležité zajistit kvalitní monitoring životních funkcí a aplikovat látky, které obnoví normální krevní tlak (vazopresiva = opak vazodilatancií). Důležité je podání tekutin formou infuzí, což má opět kladný vliv na obnovení oběhového systému. Dále se podává kalcium-glukonát spolu s atropinem. Do dvou hodin po požití mohou pomoci živočišné uhlí, výplach žaludku a podání polyetylen-glykolu, aby se maximum požitého BVK odstranilo ze zažívacího ústrojí. Pokud byly podány přípravky s postupným uvolňováním (tzv. retard) je možné pokusit se o odstranění BVK ze zažívacího ústroji i po osmi hodinách. Další možností, jak zajistit opětovnou normální srdeční činnost, je navození hyperinzulinémie. Vyšší hladina inzulinu aktivuje glukózu z periferních tkání, čímž se zlepší přísun energie pro srdeční tkáň. Další možností, jak nouzově zlepšit přísun energie k srdci, je infuzní podání vybraných lipidů ve formě emulze, ačkoliv tento postup není v současnosti standardizován. Velké obezřetnosti je třeba dbát při volbě kombinace verapamilu s beta-blokátorem, protože může dojít k nebezpečnému zpomalení srdeční činnosti (bradykardie). Obecně platí, že při zahájení či změně podávání antihypertenziv, je třeba volit zpočátku nejnižší terapeutické dávky léčiva, a na základě odpovědi organismu obezřetně zvyšovat (titrovat) dávku, než bude dosaženo přijatelného snížení tlaku krve. Výjimkou jsou stavy tzv. hypertenzní krize, a také stavy, kdy je účelné (např. vzhledem k hrozícím zdravotním komplikacím) dosáhnout snížení tlaku, co nejrychleji. V takovém případě se může zvolit na počátku vyšší dávka, ale je nutná dobrá spolupráce s lékařem, tj. kompliance (např. porozumění a přizpůsobení se vedlejším účinkům, jiný časový režim záznamu hodnot krevního tlaku, úprava životosprávy atd.).
Poznámky
Vzhledem k tomu, že vysoký krevní tlak může být důsledkem mnoha fyziologických pochodů, je důležité u každého případu hypertenze zvažovat na základě různých klinických měření (EKG, celodenní monitoring tlaku krve, zátěžové testy, angiografie aj.), které zmíněné pochody jsou v popředí (mají vyšší váhu) a podle toho zvolit vhodnou terapii. BVK jsou vhodné tam, kde vyšší krevní tlak je způsoben přetrvávajícím zúžením krevních cév (sklerotizace), na podkladě patologických cévních změn. BVK se mohou uplatnit tam, kde vysoký krevní tlak víceméně nezávisí na výkyvech sympatického systému, který je příčinou vyššího krevního tlaku na základě odpovědi srdce a cév na zvýšenou hladinu adrenalinu a noradrenalinu (skrze beta receptory). Vyšší tlak krve způsobený zvýšenou aktivitou sympatického systému dobře reaguje na tzv. sympatolytika (mezi ně patří např. beta-blokátory). Je to tedy horší "pružnost" cévního systému a relativní nezávislost na výkyvech sympatiku, kde dlouhodobě působící BVK mohou sehrát pozitivní roli. To ale komplikuje skutečnost, že u některých jedinců může být nerovnováha sympatikus vs. parasympatikus souběžná s cévními změnami. V případě takového souběhu, může být volbou jak kombinace beta-blokátoru s BVK, tak volba takového BVK, který snižuje budivost převodního systému srdce spolu s působením na cévy (viz výše zmíněné vyrovnané působení benzotiazepinů – neplést s benzodiazepiny). Takové rozlišení (omezené jen na dvě skupiny léčiv) však může být pouze orientační, protože naráží na individuální (geneticky podmíněnou) charakteristiku složitých fyziologických pochodů každého jedince, které často vyžadují zásah dalších či úplně jiných léčiv.
Vzhledem k tomu, že ionty hořčíku jsou přirozenými antagonisty vápníkových iontů, může být užívání hořčíku vhodné jako přídatná léčba u těch BVK, kde je očekáván jejich neuronální účinek.[11]
Související články
- hypertenze
- vazodilatancia
- inhibitory ACE
- beta-blokátor
Reference
V tomto článku byly použity překlady textů z článků calcium channel blocker na anglické Wikipedii, flunarizine na anglické Wikipedii a Albrecht Fleckenstein na německé Wikipedii.
- OLSON, Kent. Poisoning & drug overdose. 6th ed.. vyd. New York: McGraw-Hill Medical, 2011. ISBN 0071668330. Kapitola Calcium Channel Antagonists, s. Chapter 40. (anglicky)
- calcium channel blocker v Dorland's Medical Dictionary
- Nelson M. Drug treatment of elevated blood pressure. Australian Prescriber. 2010, s. 108–112. Dostupné v archivu pořízeném dne 10-03-2012. (anglicky) Archivovaná kopie. www.australianprescriber.com [online]. [cit. 2014-11-16]. Dostupné v archivu pořízeném z originálu.
- Felizola SJA, Maekawa T, Nakamura Y, Satoh F, Ono Y, Kikuchi K, Aritomi S, Ikeda K, Yoshimura M, Tojo K, Sasano H. Voltage-gated calcium channels in the human adrenal and primary aldosteronism.. J Steroid Biochem Mol Biol.. 2014, s. 410–416. Dostupné online. DOI 10.1016/j.jsbmb.2014.08.012. PMID 25151951. (anglicky)
- Norman M Kaplan, MD; BURTON D ROSE, MD. Major side effects and safety of calcium channel blockers [online]. Apr 3, 2000 [cit. 2014-11-16]. Dostupné v archivu pořízeném dne 30-12-2011. (anglicky)
- A. Fleckenstein, G. Grün, H. Tritthart, K. Byon, P. Harding: Uterus-Relaxation durch hochaktive Ca++-antagonistische Hemmstoffe der elektro-mechanischen Koppelung wie Iosoptin (Verapamil, Iproveratril), Substanz D 600 und Segontin (Prenylamin). In: Klinische Wochenschrift. 1971, 49, S. 32–41.
- Yousef et al.. The mechanism of action of calcium channel blockers in the treatment of diabetic nephropathy. Int J Diabetes & Metabolism. 2005, s. 76–82. Dostupné v archivu pořízeném dne 2015-10-10. (anglicky) Archivovaná kopie. ijod.uaeu.ac.ae [online]. [cit. 2014-11-17]. Dostupné v archivu pořízeném z originálu.
- Hockerman, G.H.; PETERSON, B.Z.; JOHNSON, B.D.; CATTERALL, W.A. Molecular Determinants of Drug Binding and Action on L-Type Calcium Channels. Annual Review of Pharmacology and Toxicology. 1997, s. 361–396. DOI 10.1146/annurev.pharmtox.37.1.361. PMID 9131258. (anglicky)
- Bezprozvanny I, Tsien RW. Voltage-Dependent Blockade of Diverse Types of Voltage-Gated Ca2+ Channels Expressed in Xenopus Oocytes by the Ca2+ Channel Antagonist Mibefradil (Ro 40-5967). Molecular Pharmacology. 1995, s. 540–549. Dostupné online. PMID 7565636. (anglicky)
- Scultéty S, Tamáskovits E. Effect of Ca2+ Antagonists on Isolated Rabbit Detrusor Muscle. Acta Physiologica Hungarica. 1991, s. 269–278. PMID 1755331. (anglicky)
- Iseri LT, French JH. Magnesium: Nature's Physiologic Calcium Blocker. American Heart Journal. 1984, s. 188–193. DOI 10.1016/0002-8703(84)90572-6. PMID 6375330. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Blokátory vápníkového kanálu na Wikimedia Commons
Obrázky, zvuky či videa k tématu Blokátory vápníkového kanálu na Wikimedia Commons
Přečtěte si prosím pokyny pro využití článků o zdravotnictví.