Aminoglykosidy
Aminoglykosidy jsou molekuly či části molekul nějaké sloučeniny, které mají pozměněnou cukernou (glykosidovou) část pomocí aminu.
Výraz aminoglykosidy se rovněž používá pro označení antibiotik, protože některé aminoglykosidy jsou účinné v léčbě infekcí způsobených zejména aerobními gramnegativními bakteriemi. Mezi tato tzv. aminoglykosidová antibiotika řadíme zejména amikacin, arbekacin, gentamicin, kanamycin, neomycin, netilmicin, paromomycin, rhodostreptomycin,[1] streptomycin, tobramycin a apramycin.[2] Prvním aminoglykosidovým antibiotikem uvedeným na trh byl streptomycin (objeven v r. 1943), který byl také prvním antibiotickým léčivem účinným proti tuberkulóze. Aminoglykosidová antibiotika jsou produkty bakterií Streptomyces nebo Micromonospora (viz dále).
Názvosloví
Aminoglykosidová antibiotika, která jsou produktem bakterií z rodu Streptomyces mají příponu -mycin, zatímco ty, které jsou produkty bakterií Micromonospora[3] mají příponu -micin.[4] Toto názvosloví dobře rozlišuje antibiotika mezi aminoglykosidy, ale nerozlišuje je napříč všemi skupinami antibiotik. Například vankomycin[5] je glykopeptid. Jiným příkladem je makrolidové antibiotikum erythromycin a jeho syntetické odvozeniny jako klarithromycin či azitromycin, jejichž primární účinná molekula byla odvozena od produktu bakterií Saccharopolyspora erythraea, která byla dříve nesprávně řazena mezi Streptomyces (proto zvoleno omylem -mycin).[6][7] Oproti aminoglykosidům mají jak glykopeptidy, tak makrolidy jiný mechanismus účinku.

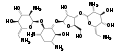
 Framycetin
Framycetin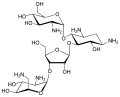 Paromomycin
Paromomycin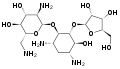 Ribostamycin
Ribostamycin Kanamycin
Kanamycin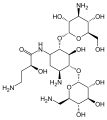 Amikacin
Amikacin Arbekacin
Arbekacin Bekanamycin
Bekanamycin Dibekacin
Dibekacin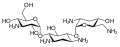 Tobramycin
Tobramycin Spectinomycin
Spectinomycin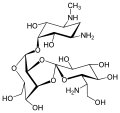 Hygromycin B
Hygromycin B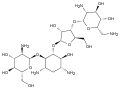 Paromomycin sulfate
Paromomycin sulfate
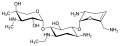 Netilmicin
Netilmicin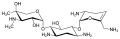 Sisomicin
Sisomicin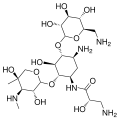 Isepamicin
Isepamicin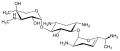 Verdamicin
Verdamicin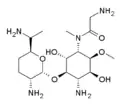 Astromicin
Astromicin
Mechanismus účinku

Aminoglykosidy mají několik antibiotických mechanismů. Mezi jejich základní účinky patří inhibice proteosyntézy citlivé bakterie, čímž se zastaví její růst a rozmnožování. Přesněji jde o tyto účinky:
- křížení (interference) s translačními mechanismy, což způsobuje růst počtu chyb v syntéze. Výsledkem je předčasné ukončení syntézy[8]
- inhibice ribozomální translokace, která zajišťuje přemístění (translokaci) peptidyl-tRNA z místa A (aminoacyl) na místo P (peptidyl)[8]
- narušení struktury stěny (membrány) bakterie[9]
- zastavení růstu a rozmnožování napojením na ribozomální podjednotku 30S[10][11]
Které mechanismy a v jakém období terapie převáží záleží na dávce léčiva. Samotné plazmatické hladiny léčiva, které jsou důležité pro správný efekt antimikrobiální terapie (monitorování plazmatické hladiny), souvisí s tzv. pozdním efektem antibiotické léčby. Totiž, po zaniknutí terapeutické hladiny v plazmě, která je důležitá pro baktericidní účinek aminoglykosidů, zůstává ještě dostatečné množství aminoglykosidů mimo plazma, kde působí proti opětovnému rozmnožení bakterií (chová se jako bakteriostatikum). Příčinou baktericidního účinku je narušení vnější bakteriální stěny, zatímco za bakteriostatický účinek je zodpovědné navázání antibiotika na zmíněnou ribozomální podjednotku 30S. Toto navázání přetrvává podstatně déle než přítomnost léčiva v plazmě. To vysvětluje závislost dávky jak na typu účinku na bakterii (baktericidní vs. bakteriostatický), tak na pozdní antibiotický efekt.
Skutečnost, že u aminoglykosidů se uplatňují ještě jiné mechanismy než inhibice proteosyntézy, souvisí s jejich rychlým působením na vybrané gramnegativní bacily, které nemůže být podmíněno procesy blokování proteosyntézy, ale jejich působením na buněčnou stěnu citlivých bakterií. Empiricky je tento účinek mj. dán rozdílem mezi účinky tetracyklinu, který působí čistě bakteriostaticky a je inhibitorem proteosyntézy a aminoglykosidů, které působí rovněž baktericidně (tetracyklin nikoliv). Bylo zjištěno, že aminoglykosidy pozměňují strukturu biofilmu stěny bakterie, která je založena na kationtech Mg2+ a Ca2+. Tato chemická struktura biofilmu zajišťuje klíčová stavební spojení polysacharidů se sousedícími lipopolysacharidy. Kationaktivní aminoglykosidové molekuly způsobují změnou biofilmu "mikropraskliny", a tím i změnu propustnosti (permeability) v bakteriální stěně. Právě zásahy a změny na bakteriální stěně mohou mnoho citlivých bakterií usmrtit ještě předtím, než aminoglykosid zasáhne ribozomální 30S podjednotku.[12] Zmíněné mikropraskliny způsobují vytékání cytoplazmatického obsahu bakterie a vnikání (uptake) aminoglykosidů dovnitř bakterie (pozn. zmíněný tetracyklin rovněž musí proniknout skrze stěnu bakterie, ale přitom ji nenarušuje, tak jako to činí aminoglykosidy). Samotný uptake aminoglykosidů přes narušenou stěnu vyžaduje energii bakterie. Vzhledem k tomu, že energie anaerobních bakterií pro tyto účely je nižší než u aerobních, jsou aminoglykosidy vůči anaerobním bakteriím méně účinné.
Indikace
Aminoglykosidy jsou určeny především pro léčbu bakteriálních infekcí, které jsou způsobeny aerobními, gramnegativními patogeny jako jsou pseudomonády, acinetobakterie a enterobakterie. Dále jsou aminoglykosidy účinné vůči některým druhům mykobakterií včetně druhu zapřičiňujícího tuberkulózu. Nejčastěji jsou aminoglykosidy nasazovány na léčbu rozsáhlých septických infekcí, komplikovaných infekcí probíhajících v dutině břišní či močovém ústrojí. Uplatňují se rovněž v léčbě nozokomiálních infekcí dýchacích cest. Infekce způsobené grampozitivními bakteriemi mohou být rovněž léčeny aminoglykosidy, ale vhodnější je použít jiné typy antibiotik, které jsou co do účinnosti a vedlejších účinků vhodnější. V minulosti se v léčbě streptokokových infekcí hojně využívala kombinace aminoglykosidů s beta-laktamovými antibiotiky z důvodu jejich synergického účinku. Tato kombinace našla uplatnění mj. v léčbě endokarditidy tj. zánětu vnitřní výstelky srdce (viz endokard). Osvědčená byla zejména kombinace ampicilinu s gentamicinem.
Alternativní indikace
Jak bylo výše poznamenáno aminoglykosidy dokáží interferovat s opravnými mechanismy dekódování DNA, čehož se využívá v léčbě genetických onemocnění způsobených předčasným zastavením proteosyntézy, díky vadným umístěním ukončovacích kódů (biochemické pokyny k ukončení proteosyntézy) v rámci kodónu (viz stop kodon). Nevhodně zařazený stopkodon vede k předčasnému zastavení výroby bílkovinné komponenty resp. vede k výrobě její zkrácené (dysfunkční) varianty. Aminoglykosidy dokážou svým náhodným vkládáním aminokyselin zakrýt chybný ukončovací kód (stopkodon), a tím dovolí dorůst příslušným bílkovinným komponentám.[13] Jedním z onemocnění, které je mj. způsobeno chybnou produkcí výše uvedeného typu je cystická fibróza. Příčinou tohoto onemocnění je porucha (mutace) genu vyrábějícího tzv. CFTR protein (cystic fibrosis transmembrane conductance regulator). V cca 10 % ze všech případů cystické fibrózy jde o poruchu genu ve smyslu výše uvedené předčasně ukončené translace, která vede k výrobě nefunkčního CFTR proteinu. V pokusech in vitro bylo pomocí antibiotika gentamicinu dosaženo úplného vytvoření CFTR proteinu. Vysvětlení spočívá právě ve změně struktury ribozomálního RNA komplexu, která původně vedla k chybné (zkrácené) výrobě CFTR, tak že chybný stop signál je díky gentamicinu "přeskočen" a je pokračováno v normálním procesu výroby CFTR.[14]
Způsoby podání
Protože aminoglykosidy se díky své značné polaritě nevstřebávají ze zažívacího traktu, neužívají se per os (ústy), ale nitrožilně nebo intramuskulárně (do svalu). Pro infekční kožní či oční onemocnění způsobené citlivými bakteriemi lze použít mast, krém, gel či kapky (např. neomycin v českém přípravku Framykoin®). Aminoglykosidy se mohou užít per os v případě, kdy je potřeba "vyčistit" od bakterií zažívací ústrojí. Taková situace může nastat v případě potřeby chirurgického zákroku či v případě jaterní encefalopatie, což je onemocnění, kdy dochází k poruše dusíkového metabolismu (amoniak a další aminy nejsou v játrech zpracovány na močovinu) a dusík s jeho metabolity proniká do mozku, kde způsobuje psychiatrické symptomy). Aminoglykosidy tím, že "vyčistí" játra a střeva od bakterií, zabrání zvýšení koncentrace amoniaku, který bakterie produkují a tím výrazně zpomalí metabolismus dusíku. Pro inhalaci v případě zánětů dolních cest dýchacích lze využít Tobramycin.
Klinické užití vs. toxicita
V oblasti antibiotické léčby gramnegativů mají aminoglykosidy stálé své místo. Jejich používání je odůvodněno i výskytem rezistencí na novější antibiotika spolu s tím, že aminoglykosidy si stále udržují účinnost proti většině gramnegativů v mnoha oblastech světa.[15] Užívání aminoglykosidů je ale spojeno s vážnými vedlejšími účinky spojenými s jejich ototoxicitou a nefrotoxicitou (ohrožují sluchové ústrojí a ledviny). Empirickým řešením tohoto rizika je pečlivé rozvržení a kontrolování dávkování se stanovením takové dávky, která je terapeuticky účinná a přitom nejméně toxická. K hlubšímu porozumění a překonání problému toxicity aminoglykosidů bude potřeba dalších výzkumů. Ideálem by bylo objevit další aminoglykosid, který by si zachoval svojí silnou účinnost proti gramnegativům, ale zároveň by byl zcela oproštěn od všech toxických projevů.[16]
V případě velmi závažné ototoxicity se aminoglykosidy dělí na ty, které spíše zasahují vestibulární ústrojí (gentamicin), což zapříčiňuje závratě, a na ty, co zasahují samotný sluch. Rizika spojená s ototoxicitou se zvyšují dlouhodobým užíváním, nepřiměřeným dávkováním a akumulací léčiva uvnitř organismu z důvodu zpomalení jeho vylučování ledvinami (poruchy ledvin či užívání kličkových diuretik).
Reference
V tomto článku byl použit překlad textu z článku Aminoglycoside na anglické Wikipedii.
- Massachusetts Institute of Technology: Bacterial 'battle for survival' leads to new antibiotic, tisková zpráva, [cit. December 1, 2010], Dostupné on-line.
- RYDEN, R, Moore. BJ. J Antimicrob Chemother. 1977, s. 609–613. DOI 10.1093/jac/3.6.609. PMID 340441. (anglicky)
- Kroppenstedt RM, Mayilraj S, Wink JM. Eight new species of the genus Micromonospora, Micromonospora citrea sp. nov., Micromonospora echinaurantiaca sp. nov., Micromonospora echinofusca sp. nov. Micromonospora fulviviridis sp. nov., Micromonospora inyonensis sp. nov., Micromonospora peucetia sp. nov., Micromonospora sagamiensis sp. nov., and Micromonospora viridifaciens sp. nov. Syst Appl Microbiol.. 2005, s. 328–39. DOI 10.1016/j.syapm.2004.12.011. PMID 15997706. (anglicky)
- Paul M. Dewick. Medicinal Natural Products: A Biosynthetic Approach. 3rd. vyd. [s.l.]: Wiley, 2009. ISBN 0-470-74167-8. (anglicky)
- Walter P. Hammes1 and Francis C. Neuhaus. On the Mechanism of Action of Vancomycin: Inhibition of Peptidoglycan Synthesis in Gaffkya homari. Antimicrobial agents and chemotherapy. 1974, s. 722–728. PMID 4451345. (anglicky)
- Protein synthesis inhibitors: macrolides mechanism of action animation. Classification of agents Pharmacology Corner. Author: Gary Kaiser. The Community College of Baltimore County. Retrieved on July 31, 2009
- The Mechanism of Action of Macrolides, Lincosamides and Streptogramin B Reveals the Nascent Peptide Exit Path in the Ribosome Archivováno 25. 8. 2009 na Wayback Machine Martin Lovmar and Måns Ehrenberg
- Pharmacology Corner → Protein synthesis inhibitors: aminoglycosides mechanism of action animation. Classification of agents Posted by Flavio Guzmán on 12/08/08
- SHAKIL, Shazi; KHAN, Rosina; ZARRILLI, Raffaele; KHAN, Asad U. Aminoglycosides versus bacteria – a description of the action, resistance mechanism, and nosocomial battleground. Journal of Biomedical Science. 2007, s. 5–14. DOI 10.1007/s11373-007-9194-y. PMID 17657587. (anglicky)
- LEVISON, Matthew E. Aminoglycosides: Bacteria and Antibacterial Drugs [online]. 2009. Dostupné online. (anglicky)
- Aminoglycosides [online]. [cit. 2012-10-08]. Dostupné v archivu pořízeném dne 2011-09-09. (anglicky)
- LORIAN, Victor. Antibiotics in Laboratory Medicine. [s.l.]: Williams & Wilkins Press, 1996. ISBN 0-683-05169-5. S. 589–90. (anglicky)
- FEERO, W. Gregory; GUTTMACHER, Alan E.; DIETZ, Harry C. New Therapeutic Approaches to Mendelian Disorders. New England Journal of Medicine. 2010, s. 852–63. DOI 10.1056/NEJMra0907180. PMID 20818846. (anglicky)
- WILSCHANSKI, Michael; YAHAV, Yaacov; YAACOV, Yasmin; BLAU, Hannah; BENTUR, Lea; RIVLIN, Joseph; AVIRAM, Micha. Gentamicin-Induced Correction of CFTR Function in Patients with Cystic Fibrosis andCFTRStop Mutations. New England Journal of Medicine. 2003, s. 1433–41. DOI 10.1056/NEJMoa022170. PMID 14534336. (anglicky)
- FALAGAS, Matthew E; GRAMMATIKOS, Alexandros P; MICHALOPOULOS, Argyris. Potential of old-generation antibiotics to address current need for new antibiotics. Expert Review of Anti-infective Therapy. 2008, s. 593–600. DOI 10.1586/14787210.6.5.593. PMID 18847400. (anglicky)
- DURANTE-MANGONI, Emanuele; GRAMMATIKOS, Alexandros; UTILI, Riccardo; FALAGAS, Matthew E. Do we still need the aminoglycosides?. International Journal of Antimicrobial Agents. 2009, s. 201–5. DOI 10.1016/j.ijantimicag.2008.09.001. PMID 18976888. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu aminoglycoside antibiotic na Wikimedia Commons
Obrázky, zvuky či videa k tématu aminoglycoside antibiotic na Wikimedia Commons - MedlinePlus drug information – Aminoglycosides (Systemic)
- Science Daily Bacterial 'Battle for Survival' – Rhodostreptomycin