Sulfid rtuťnatý
Sulfid rtuťnatý (HgS) je anorganická sloučenina.
| Sulfid rtuťnatý | |
|---|---|
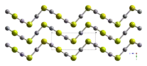
Struktura sulfidu rtuťnatého | |
| Obecné | |
| Systematický název | Sulfid rtuťnatý |
| Ostatní názvy | Rumělka |
| Anglický název | Mercury sulfide (systematický název) Cinnabar Vermilion |
| Německý název | Quecksilbersulfid |
| Sumární vzorec | HgS |
| Vzhled | červená pevná látka (α) černý (β) |
| Identifikace | |
| Registrační číslo CAS | 1344-48-5 |
| PubChem | 62402 |
| Vlastnosti | |
| Molární hmotnost | 232,66 g/mol |
| Teplota tání | 580 °C (rozklad) |
| Hustota | 8,10 g/cm3 |
| Index lomu | 2,905 (w) 3,256 (e) (α modifikace) |
| Rozpustnost ve vodě | nerozpustný |
| Součin rozpustnosti | 4,0×10−53 (20 °C)[1] |
| Struktura | |
| Krystalová struktura | šesterečná (α) |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −58 kJ/mol−1 |
| Standardní molární entropie S° | 78 JK−1mol−1 |
| Bezpečnost | |
| [2] Varování[2] | |
| R-věty | R26/27/28, R33, R50/53 |
| S-věty | S1/2, S13, S28, S45, S60, S61 |
| Teplota vznícení | nehořlavý |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Struktura
HgS existuje ve dvou krystalických modifikacích:
- α modifikace (šesterečná) – je nejběžnější formou rtuti v přírodě, vyskytuje se jako minerál cinabarit (rumělka)
- β modifikace – v přírodě se vyskytuje mnohem méně
Výroba a vlastnosti
Beta modifikace sulfidu rtuťnatého se vyrábí probubláváním sulfanu roztoky rtuťnatých solí a vylučuje se jako černý prášek. Tato modifikace nereaguje s žádnými koncentrovanými kyselinami.
Použití
Alfa modifikace sulfidu rtutňatého se používá jako červený pigment známý jako rumělka, který ovšem tmavne, což je způsobeno přeměnou červené α modifikace na černou β modifikaci.
Související články
- Cinabarit
- Otrava rtutí
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Mercury sulfide na anglické Wikipedii.
- https://old.vscht.cz/fch/prikladnik/prikladnik/tab/rozpust.html
- Mercuric sulfide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu sulfid rtuťnatý na Wikimedia Commons
Obrázky, zvuky či videa k tématu sulfid rtuťnatý na Wikimedia Commons
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
