Spektrofotometrie
Spektrofotometrie je analytická metoda pro měření vlastností vzorku (např. koncentrace určité látky v roztoku) na základě pohlcování světla různých vlnových délek spektra. Pokud se měří jen při jedné vlnové délce, metoda se spíše označuje fotometrie. Obdobně zařízení, která měří při jedné nebo jen několika přesně definovaných vlnových délkách monochromatického světla, se nazývají fotometry. Technicky složitější a dokonalejší přístroje, které umožňují vlnovou délku monochromatického světla libovolně nastavit, nebo měřit část absorpčního spektra v určitém úseku vlnových délek, se nazývají spektrofotometry.

Princip spektrofotometrie
Roztok v kyvetě je ozařován monochromatickým světlem (vybraná oblast elektromagnetického spektra) a světelné záření je molekulami analytu absorbováno. Detektor záření měří intenzitu dopadajícího světla (zářivý tok) neabsorbovaného roztokem. Při analýze je spektrofotometrem porovnávána intenzita zdrojem vysílaného záření s intenzitou záření dopadajícího na detektor - část energie světelného záření je roztokem a rozpuštěnými látkami absorbována. Množství absorbovaného záření je pak úměrné koncentraci látky ve studovaném roztoku.
Druhy spektrofotometrie
Podle rozsahu absorbovaných vlnových délek se rozlišují tyto metody:
- molekulová absorpční spektrofotometrie ve viditelné oblasti elektromagnetického spektra (frekvenční rozsah 400-800 nm)
- Molekulová absorpční spektrometrie v ultrafialové oblasti elektromagnetického spektra (frekvenční rozsah 190-400 nm)
- O absorpční spektrometrii v ultrafialové a viditelné oblasti blíže pojednává samostatný článek Ultrafialovo-viditelná spektroskopie.
- molekulová absorpční spektrofotometrie v infračervené oblasti elektromagnetického spektra (frekvenční rozsah 0,8-1000 μm)
- O absorpční spektrometrii v infračervené oblasti elektromagnetického spektra blíže pojednávají samostatné články infračervená spektroskopie a blízká infračervená spektroskopie.
Pro měření ve viditelné oblasti spektra se používají skleněné, nebo občas i akrylové kyvety, pro měření v ultrafialové oblasti kyvety z křemenného skla. Pro měření v infračervené oblasti se používají kyvety z NaCl nebo TlBr.
Uspořádání a konstrukce fotometru
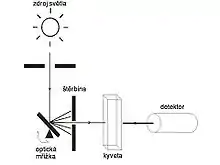
Principiálně se fotometr i spektrofotometr skládá ze čtyř částí:
- zdroj záření - halogenová žárovka, žárovka s wolframovým vláknem, xenonová lampa, vodíková výbojka, deuteriová výbojka, laser
- monochromátor - interferenční filtr, disperzní hranol nebo mřížka
- prostor, ve kterém je umístěn vzorek - kyveta
- detektor - fotonásobič nebo detektor s diodovým polem
- vyhodnocovací/zobrazovací zařízení - počítač, X-Y zapisovač (plotter), display zobrazující hodnotu měřené absorbance
Zdroj záření

Jako zdroj záření slouží vhodná žárovka nebo výbojka. Žárovky a halogenové žárovky poskytují záření o spojitém spektru ve viditelné a infračervené oblasti, nelze je však použít pro měření v ultrafialové oblasti. Jako zdroje ultrafialového záření se používají nejčastěji vodíkové nebo deuteriové výbojky. Zdrojem ultrafialového i viditelného světla může být také například xenonová výbojka, široký rozsah vlnových délek je však vyvážen některými nevýhodami: její záření je složením spojitého a čárového spektra, takže jsou velké rozdíly mezi intenzitami při různých vlnových délkách, výbojka je velmi drahá a intenzita jejího záření není příliš stabilní.
Monochromátor

Polychromatické světlo následně prochází monochromátorem. Nejjednodušší a nejlevnější možností je zařazení vhodného interferenčního filtru do optické dráhy. Komerčně dostupné jsou dnes filtry prakticky pro libovolnou vlnovou délku ultrafialové a viditelné oblasti. Rozlišuje se několik druhů interferenčních filtrů, jejichž vhodnou kombinací se sestaví filtr požadovaných vlastností. Low-pass filtry propouštějí světlo vlnových délek kratších, než je určitá mez (cut-off). High-pass filtry naopak propouštějí jen světlo, které má větší vlnovou délku, než je hraniční vlnová délka filtru. Pásmové filtry propouštějí určitý rozsah vlnových délek. Protože hranice nebývají zcela ostré, uvádí se jako dolní a horní mez zpravidla taková vlnová délka, pro kterou má filtr padesátiprocentní transmitanci ve srovnání s vlnovou délkou, kterou propouští nejlépe. Někdy se také uvádí střední vlnová délka, kterou filtr propouští, a šířka pásma (nebo polopásma).
Jako monochromátor v současnosti obvykle slouží optická mřížka, jejímž nakláněním lze plynule měnit vlnovou délku (například Czerného-Turnerův monochromátor). Rozsah vlnových délek, které z monochromátoru vycházejí, určuje štěrbina, buď pevně nastavená, nebo rovněž nastavitelná. Čím je štěrbina širší, tím větší je intenzita vycházejícího světla, ovšem za cenu menší specifičnosti měření. Naopak užší štěrbina zajistí přesnější dodržení požadované vlnové délky, ovšem za cenu menší intenzity světla a zhoršení odstupu signálu od šumu.
Vzorek
Monochromatické světlo prochází vzorkem. Většinou se pracuje s roztoky, které se plní do standardních kyvet s optickou dráhou 1 cm. Kyvety se v přístroji umisťují do kyvetátoru, který zajišťuje jejich přesnou polohu, může být temperován a někdy obsahuje i magnetickou míchačku, pomocí níž lze po vložení míchadélka do kyvety promíchávat její obsah během měření. Často bývá možné do kyvetátoru založit najednou několik kyvet, které se pak automaticky vsunují do optické dráhy.
Detektor
Světlo vycházející ze vzorku dopadá na detektor, zpravidla fotodiodu nebo jiný fotoelektrický prvek. Intenzita se vyhodnotí pomocí systému převodníků, srovná se s intenzitou světla procházejícího slepým vzorkem, a tím se získá absorbance. Přesnost měření ovlivňuje integrační čas – doba, po kterou se absorbance měří. Čím je delší, tím přesnější bude výsledek měření, pokud ovšem není absorbující látka fotocitlivá (tedy pokud nedojde při delším osvitu k vyblednutí vzorku). Nevýhodou dlouhého integračního času je také prodlužování doby měření, což je podstatné zejména při zpracování velkého množství vzorků, při měření při velkém počtu vlnových délek (měření spekter), nebo při zpracování vzorků, které se v čase mění (kinetická měření).
Kromě jednopaprskových fotometrů, v nichž se nejprve měří slepý vzorek a pak se do stejné optické dráhy vkládá měřený vzorek, se používají i dvoupaprskové fotometry, které jsou vybaveny dvěma detektory a umožňují měřit slepý i měřený vzorek současně ve dvou optických drahách.
V případě dvojpaprskového uspořádání spektrofotometru dopadá orientovaný paprsek monochromatického světelného záření na dělič paprsku.Vznikají dva paprsky nové. Jeden nový paprsek prochází referentní kyvetou s rozpouštědlem a zářivý tok paprsku prošlého kyvetou je zaznamenáván detektorem záření. Druhý nový paprsek prochází kyvetou s roztokem vzorku (stejný druh rozpouštědla) a je zaznamenáván po průchodu kyvetou druhým detektorem. Spektrofotometr pak může porovnat absorbanci čistého rozpouštědla a měřeného roztoku.
Jednopaprskový spektrofotometr využívá pouze jeden detektor, nemá dělič paprsku. Toto konstrukční uspořádání spektrofotometru trpí nestabilitou zdroje záření.
Při stanovení koncentrace analytu se využívá tvorby kalibračních grafů. Měří se série kalibračních roztoků o vzrůstající koncentraci analytu. Ze změřené absorbance analytu ve zkoumaném roztoku se vypočte na kalkulačce jeho koncentrace.
Jiná uspořádání spektrofotometru
Měření spektra na spektrofotometru s optickou mřížkou znamená, že přístroj změří absorbanci při jedné vlnové délce, pak posune mřížku, měří při další vlnové délce a to se neustále opakuje, dokud se neproměří celá požadovaná oblast. To s sebou přináší poměrně dlouhou dobu měření, což může být na závadu z několika důvodů:
- vzorek se může v čase měnit (zejména při kinetických měřeních)
- vzorek může být fotocitlivý, v průběhu měření dochází k jeho vyblednutí
- pokud se zpracovává více vzorků, které nejsou dostatečně stabilní, může být technicky obtížné zajistit stejné podmínky pro první a poslední vzorky
- měření trvá dlouho, výkonnost metody je nízká
Diodové pole

Uvedené nedostatky odstraňuje jiné uspořádání spektrofotometru, měření pomocí diodového pole (diode-array). Při něm prochází vzorkem bílé světlo, které je až poté rozloženo na jednotlivé vlnové délky (zpravidla pomocí pevně postavené optické mřížky) a dopadá na destičku s velkým množstvím detektorů – fotodiod (odtud název diodové pole). Diodové pole je přitom umístěno tak, že na každou fotodiodu dopadá určitý (poměrně úzký – například 2 nm) rozsah vlnových délek. Zařízení neobsahuje žádné pohyblivé prvky, což zvyšuje reproducibilitu měření, a navíc se změří celé spektrum najednou. Doba měření se tak může zkrátit z několika minut na zlomky sekundy. Toto uspořádání navíc umožňuje konstruovat přístroje přibližně o řád přesnější, než klasické fotometry, navíc nevyžadující prakticky žádnou údržbu, kalibraci atd. Zásadní nevýhodou bývá mnohonásobně vyšší pořizovací cena, avšak se zlevňováním miniaturních elektronických prvků se náklady na výrobu diodového pole rychle snižují.
Fotometrie se svislým paprskem
V rutinním použití má klasické uspořádání fotometrie i další nevýhody:
- vyžaduje velké množství vzorku
- má malou výkonnost, zpracování jednotlivých vzorků je pracné
- kyvety jsou drahé a náročné na údržbu
- spektrofotometry jsou nákladné
Tyto nevýhody z velké části odstraňuje měření v mikrotitračních destičkách pomocí fotometru se svislým paprskem (čtečka destiček, plate reader). Vzorky se plní do polystyrénových destiček s 96 jamkami, existují ale i jiné formáty (od 4 do 384 jamek). Pro práci s mikrotitračními deskami jsou k dispozici speciální pomůcky (vícekanálové pipety, opakovací pipety atd.), které výrazně urychlují přípravu vzorků. Na rozdíl od klasických fotometrů, v nichž se absorbance měří vodorovným paprskem a optická dráha je daná tloušťkou kyvety, probíhá v tomto případě měření pomocí svislého paprsku a délka optické dráhy záleží na výšce hladiny v jamce. Pokud ke vzorku přidáme určité množství bezbarvého roztoku, sníží se sice koncentrace absorbující látky, zároveň se ale úměrně zvýší hladina roztoku v jamce (prodlouží se optická dráha) a výsledná absorbance bude stejná.[zdroj?!] Naopak, pokud se ze vzorku odpaří část bezbarvého rozpouštědla, optická dráha se sice zkrátí, zato však stoupne koncentrace absorbující látky a absorbance se opět nezmění.[zdroj?!] Lze říci, že na rozdíl od klasické fotometrie, kde absorbance odpovídá koncentraci absorbující látky v roztoku, závisí absorbance při měření svislým paprskem na látkovém množství absorbující látky ve vzorku.[zdroj?!]
Pro fotometrii svislým paprskem je třeba mnohem menší objem vzorku – jamky se zpravidla plní jen 100 až 300 μl roztoku. Mikrotitrační destičky jsou jednorázové a jsou vzhledem k počtu zároveň měřených vzorků podstatně levnější než plastové kyvety. Změření všech 96 jamek trvá obvykle jen několik sekund. Rovněž destičkové fotometry bývají poměrně levné, jako monochromátor většinou používají sadu interferenčních filtrů. Zvláště často se fotometrie svislým paprskem využívá v imunochemii, zejména v metodice ELISA (odtud rozšířené označení přístroje ELISA-reader).
Pro větší přehlednost se při fotometrii svislým paprskem kromě pojmu absorbance používá ještě termínu optická hustota (OD - z anglického optical density). Platí přitom vztah
- OD = A / l
kde OD je optická hustota, A je absorbance a l je délka optické dráhy.
Optická hustota tedy závisí jen na vlastnostech vzorku, nikoli však na délce optické dráhy, po níž světlo vzorkem prochází.
Reflexní fotometrie
Jinou fotometrickou technikou je reflexní fotometrie - technika rutinně používaná například v klinické biochemii v rámci suché chemie. V suché chemii se biologický materiál nezpracovává obvyklým způsobem ve zkumavkách či jiných nádobkách, ale nanese se na film napuštěný jednotlivými složkami reakční směsi. Výsledkem je změna barvy políčka, kterou lze kvantifikovat pomocí reflexního fotometru – měří se úbytek světla určité vlnové délky odraženého od políčka. Jako zdroj světla se používají buď LED diody emitující vhodnou vlnovou délku, nebo žárovkové zdroje s interferenčními filtry. Pro zvýšení citlivosti se odražené světlo soustřeďuje na detektor vydutým zrcadlem (tzv. Ulbrichtovou koulí). Klasickým příkladem suché chemie a reflexní fotometrie je vyšetření moči pomocí diagnostických proužků, vzhledem k jednoduchosti a rychlosti při přesnosti srovnatelné s klasickými metodami se však množství aplikací rychle rozšiřuje.
Pokročilé spektrofotometrické techniky
Multikomponentní analýza
Často se stává, že v části spektra, kde má absorpční maximum stanovovaná látka, zároveň absorbuje i další složka reakční směsi. V tom případě nelze snadno stanovit koncentraci měřené látky, protože absorbance při zvolené vlnové délce je součtem absorbancí obou látek. Pokud je koncentrace druhé, „překážející“ složky známá, nebo pokud lze experiment uspořádat tak, aby byla konstantní ve všech vzorcích, lze tuto situaci vyřešit pomocí vhodných slepých vzorků. V některých případech je však nutné postupovat metodami multikomponentní analýzy spektra.
Obvykle se neměří při jedné vlnové délce, ale proměřuje se určitá spojitá část spektra, nebo se přinejmenším měří při několika vlnových délkách. Jsou-li známé extinkční koeficienty jednotlivých látek absorbujících v dané oblasti při různých vlnových délkách (nebo ještě lépe, jsou-li známá absorpční spektra jednotlivých složek směsi), lze koncentraci analytu vypočítat řešením soustavy rovnic.

V nejjednodušším případě je třeba stanovit koncentraci jedné látky, přičemž její absorpční spektrum (na obrázku tečkovaně) překrývá spektrum jiné ve vzorku přítomné látky (čárkovaně). Měřením vzorku vznikne spektrum, které je součtem obou absorpčních spekter (plnou čarou). Přestože má stanovovaná látka absorpční maximum při vlnové délce λ1, nelze její koncentraci stanovit přímo, neboť při této vlnové délce nelze zanedbat absorbanci druhé látky. Je-li však znám tvar absorpčního spektra druhé látky, je možné najít vlnovou délku, při které absorbuje stejně, jako při vlnové délce λ1 (označuje se λ2), takže extinkční koeficient je pro λ1 a λ2 stejný. Potom absorbance samotné stanovované látky bude
- A = A(λ1) – A(λ2).
Využití isosbestického bodu
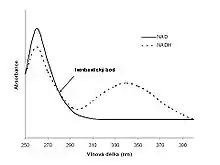
Pokud látka, která má určité spektrum, se v průběhu nějaké reakce mění na jinou látku, která má jiné spektrum, ale obě spektra se částečně překrývají, tak se používá metoda isosbestického bodu; příkladem mohou být spektra NAD+ a NADH (stanovení těchto koenzymů se využívá při měření aktivity řady enzymů pomocí Warburgova optického testu). V tomto případě jsou absorpční maxima dostatečně daleko od sebe, takže stanovení jednotlivých forem koenzymu je jednoduché. Užitečná však může být skutečnost, že všechna spektra pro různé poměry NAD+/NADH (při konstantní celkové koncentraci) se kříží. To je způsobeno tím, že při vlnové délce 281 nm má NAD+ i NADH stejný extinkční koeficient. Průsečík spekter se nazývá isosbestický bod (z řeckého ισος isos = stejný a σβεννυμι sbennými = zháším) a měřením absorbance v tomto bodě se snadno zjistí celková koncentrace NAD+ a NADH, bez nutnosti znát poměr koncentrací obou složek.
Další metody
Řadu dalších dat lze získat vhodným matematickým zpracováním naměřených spekter. Při měření složitějších soustav může pomoci derivační spektrofotometrie, která umožní po vyhodnocení prvních a druhých derivací spekter podle vlnové délky mimo jíiné najít přesné polohy absorpčních maxim. Rovněž pro zpracování kinetických měření je nezbytné matematické zpracování získaných dat.
Děje v molekulách probíhající při spektrofotometrii
Absorpce energie záření probíhá v analyzovaném roztoku tak, aby se veškerá energie molekulou absorbovaného fotonu pohltila. Uplatňují se elektronové, vibrační i rotační přechody v molekule. Změny energie v molekule probíhající při absorpci záření lze popsat vztahem:
ΔE = h·f = E1-E0 = ΔEe + ΔEv+ ΔEr
kde h je Planckova konstanta, f je frekvence absorbovaného záření, E0 je výchozí energetická hladina, E1 je excitovaná hladina molekuly, ΔEe je změna energie v molekule příslušející elektronovým přechodům, ΔEv je změna energie v molekule příslušejícící vibračním přechodům, ΔEr je změna energie v molekule příslušející rotačním přechodům.
Absorpce záření při spektrofotometrii nastává při dějích v molekulových orbitalech (elektronové přechody v organických sloučeninách). Uplatňují se též elektronové přechody v komplexech kovů, které se podílejí na absorpci analytem v roztoku. Spektrofotometrická měření se provádějí ve vodných roztocích (komplex železa, komplex niklu) nebo v organických rozpouštědlech jako jsou chloroform (tenzidy) nebo methanol (léčiva).
Přesnost fotometrických metod
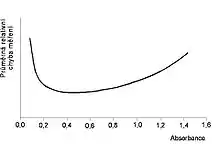
Většina fotometrů může měřit absorbanci v rozmezí 0 až 3 nebo 4. To však neznamená, že by měření v celém tomto rozsahu bylo rozumné. Za předpokladu, že náhodná chyba detektoru bude mít stále stejné vlastnosti, bude mít průměrná relativní chyba měření absorbance v závislosti na skutečné absorbanci vzorku průběh ve tvaru písmene U. Nejlepších výsledků se dosáhne, bude-li se absorbance vzorku pohybovat v rozmezí 0,2 až 0,8, za rozumné lze považovat měření v rozsahu 0,2 až 1,2. Je-li absorbance vyšší, je vhodné vzorek ředit. Konkrétní hodnoty samozřejmě závisejí na vlastnostech použitého fotometru, ovšem průběh průměrné relativní chyby jako funkce absorbance bude stále stejný (liší se jen „roztažení“ křivky).
Přesnost měření je velmi ovlivněna i přípravou vzorku a kyvety. Nejvýznamnější vlivy, které ovlivňují přesnost spektrofotometrických stanovení, jsou:
- Je třeba měřit ve vhodné kyvetě, zvolená vlnová délka musí ležet v pásmu, pro které je kyveta určena
- Měří-li se ve více kyvetách, měly by mít všechny stejný faktor. Plastové kyvety by měly být všechny ze stejné šarže.
- Kyvety pro vzorky i blanky musejí být čisté. To lze ověřit tak, že naplněné destilovanou vodou dají všechny stejnou absorbanci.
- S kyvetami je třeba pracovat tak, aby nedošlo ke znečištění optických ploch (například dotykem prstů). Totéž platí i pro mikrotitrační destičky.
- Kyveta musí být zvenčí suchá, uvnitř nesmějí zůstat bublinky vzduchu, měřený roztok musí být homogenní. Kapka stékající po kyvetě, bublinky nebo plovoucí sraženina v měřeném roztoku se projeví obvykle tím, že se naměřená absorbance neustále mění.
- Kyveta musí být vzorkem dostatečně naplněná.
- Měří-li se více vzorků postupně v jedné kyvetě, je třeba pracovat tak, aby chyba způsobená zbytky předchozího roztoku byla co nejmenší. Obvykle se kyveta mezi vzorky vyplachuje destilovanou vodou a pak se co nejlépe vysuší. Přesnějších výsledků se dosáhne, pokud se kyveta po vymytí ještě propláchne malým množstvím vzorku, který se vylije a pak teprve se kyveta naplní potřebným množstvím vzorku pro měření. Pokud se pracuje s několika podobnými roztoky, může být přesnější kyvety mezi nimi neproplachovat destilovanou vodou, jen je co nejlépe vylít a vysušit.
- Při měření v kyvetách je podstatná koncentrace barevné látky v roztoku, při přípravě vzorku je proto nejdůležitější dodržet poměr jednotlivých složek. Je vhodné uspořádat pokus tak, aby se všechny složky pipetovaly pokud možno stejnou pipetou, nejlépe pevně nastavenou.
- Měří-li se v mikrotitračních destičkách, je naopak rozhodující látkové množství barevné látky ve vzorku. Proto je třeba pokus uspořádat tak, aby byl do jamky co nejpřesněji odměřen analyt. Velkou chybu může také způsobit různý tvar hladiny v jednotlivých jamkách, všechny vzorky by proto měly mít stejnou afinitu ke stěnám destičky, případně je vhodné desku před měřením krátce promíchat, aby se zajistilo smočení stěn i nad hladinou roztoku.