Polární molekula
Polární molekuly jsou molekuly, které mají stálý a nenulový dipólový moment, protože elektrický náboj je v nich rozložen nesymetricky. Tohoto stavu lze dosáhnout, jestliže má molekula polární vazby mezi různými atomy nebo jsou polární vazby ve struktuře molekuly nesymetricky rozložené.
Polární vazby se obvykle vyskytují v molekulách, kde je rozdíl v elektronegativitě mezi atomy zhruba mezi 0,4 a 2,0. U nepolárních vazeb je tento rozdíl menší než 0,4 a u iontových je větší než 2,0.
Elektrický náboj
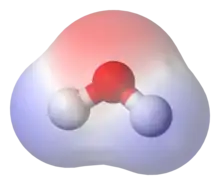
V polární molekule jsou vazebné elektrické náboje v molekule nerovnoměrně rozloženy a vznikají tak kladné nebo záporné póly. Na jedné straně molekuly je pak kladný elektrický náboj a na druhé straně záporný elektrický náboj. Polární molekuly mají tendenci se dobře rozpouštět ve vodě a jiných polárních rozpouštědlech.
Amfifily nebo amfifilní molekuly jsou velké molekuly, které mají polární i nepolární skupiny a jsou s nimi spojeny. To způsobuje, že jsou povrchově aktivní a snižují mezifázové napětí na rozhraní kapalina-kapalina. Využívají se při tvorbě stabilních emulzí nebo směsí vody a tuků.
Dipólový moment
Měřítkem polarizace vazby v molekule je dipólový moment. Je to vektorová veličina popisující nesymetrické rozdělení elektrického náboje v molekule. Polární molekuly mají nenulovou hodnotu elektrického dipólového momentu a tvoří permanentní dipól.
Elektronegativita
Afinita atomů k vazebným elektronům se obvykle vyjadřuje veličinou zvanou elektronegativita prvku. Konvenčně se za polární molekulu považuje molekula, kde je rozdíl elektronegativit atomů, ze kterých je složena, větší než 0,4 a menší než 2,0. Ve složitějších molekulách může být rozložení hustoty vazebných elektronů v jednotlivých kovalentních vazbách výrazně ovlivněno indukčními nebo mezomerními efekty vyvolanými jinými částmi molekuly.
Příklady polárních molekul
- voda
- všechny anorganické kyseliny (kyselina křemičitá je nerozpustná ve vodě)
- nižší alkoholy:
- nižší karboxylové kyseliny:
Polární rozpouštědla
Polární rozpouštědla jsou taková rozpouštědla, která jsou tvořena polárními molekulami. Většinou platí, že libovolná dvě polární rozpouštědla se navzájem mísí a rozpouštějí často tytéž látky. U některých látek to neplatí, v jednom polárním rozpouštědle je látka rozpustná a v jiném není nebo se v něm rozpouští jen velmi málo. Například chlorid sodný se dobře rozpouští ve vodě, méně v methanolu a obtížně v ethanolu.
Související články
Reference
V tomto článku byl použit překlad textu z článku Chemical polarity na anglické Wikipedii.'V tomto článku byl použit překlad textu z článku Chemische Bindung na německé Wikipedii.