L-selektrid
L-selektrid je organoboran používaný jako redukční činidlo v organické chemii při redukci ketonů v Overmanově syntéze strychninu.[1]
| L-selektrid | |
|---|---|
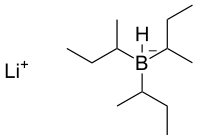
Model struktury | |
| Obecné | |
| Systematický název | tri-sek-butyl(hydrido)borát lithný |
| Sumární vzorec | C12H28BLi |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 38721-52-7 |
| PubChem | 2723989 |
| SMILES | [Li+].[BH-](C(C)CC)(C(C)CC)C(C)CC |
| InChI | 1S/C12H28B.Li/c1-7-10(4)13(11(5)8-2)12(6)9-3;/h10-13H,7-9H2,1-6H3;/q-1;+1 |
| Vlastnosti | |
| Molární hmotnost | 190,10 g/mol |
| Hustota | 0,870 g/cm3 |
| Rozpustnost ve vodě | reaguje |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
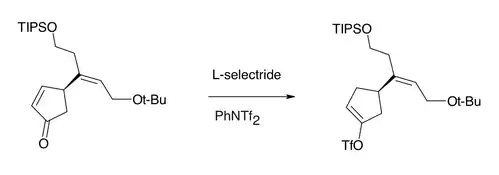
Za určitých podmínek může L-selektrid selektivně redukovat enony konjugovanou nukleofilní adicí hydridu, protože vytváří silnější sterické napětí než hydridový reaktant na karbonylovém uhlíku vzhledem k (rovněž elektrofilní) pozici β.[2] L-selektrid také stereoselektivně redukuje karbonylové skupiny 1,2-mechanismem, což je také způsobeno sterickými vlastnostmi hydridu.[3]
N-selektrid a K-selektrid jsou obdobné sloučeniny, které mají místo lithného kationtu kation sodný či draselný. Používají se někdy místo L-selektridu, například při redukcích sodných amalgámů v anorganické chemii.
L-selektrid se rovněž používá při výrobě léčiva aprepitantu.
Reference
V tomto článku byl použit překlad textu z článku L-selectride na anglické Wikipedii.
- S. D. Knight, L. E. Overman and G. Pairaudeau. Synthesis applications of cationic aza-Cope rearrangements. 26. Enantioselective total synthesis of (−)-strychnine. Journal of the American Chemical Society. 1993, s. 9293–9294. DOI 10.1021/ja00073a057. (anglicky)
- Organic chemistry. Oxford: Oxford University Press 1508 s. Dostupné online. ISBN 0-19-850347-4, ISBN 978-0-19-850347-7. OCLC 43338068 S. 685.
- Scott A. Miller and A. Richard Chamberlin. Highly selective formation of cis-substituted hydroxylactams via auxiliary-controlled reduction of imides. The Journal of Organic Chemistry. 1989, s. 2502–2504. DOI 10.1021/jo00272a004. (anglicky)