Chlorid niobičný
Chlorid niobičný je anorganická sloučenina se vzorcem NbCl5.
Jedná se o žlutou krystalickou pevnou látku. Hydrolyzuje vzdušnou vlhkostí a je často znečištěn malými množstvími NbOCl3, ovšem lze jej přečistit sublimací.[2]
| Chlorid niobičný | |
|---|---|
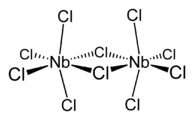
Strukturní vzorec dimeru | |
| Obecné | |
| Systematický název | Chlorid niobičný |
| Anglický název | Niobium(V) chloride Niobium pentachloride |
| Německý název | Niob(V)–chlorid |
| Sumární vzorec | NbCl5 Nb2Cl10 (dimer) |
| Vzhled | žluté monoklinické krystaly |
| Identifikace | |
| Registrační číslo CAS | 10026-12-7 |
| EC-no (EINECS/ELINCS/NLP) | 233-059-8 |
| Číslo RTECS | QU0350000 |
| Vlastnosti | |
| Molární hmotnost | 270,17 g/mol |
| Teplota tání | 204,7 °C |
| Teplota varu | 248,2 °C |
| Hustota | 2,750 g/cm3 |
| Rozpustnost ve vodě | Rozklad |
| Rozpustnost v polárních rozpouštědlech |
rozpustný v ethanolu a kyselině chlorovodíkové |
| Rozpustnost v nepolárních rozpouštědlech |
Rozpustný v chloridu uhličitém a chloroformu |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −797,47 kJ/mol |
| Standardní molární entropie S° | 214,05 JK−1mol−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Teplota vznícení | nehořlavý |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Příprava
Průmyslově se NbCl5 vyrábí chlorací kovového niobu při teplotě 300 až 350 °C[3]:
2 Nb + 5 Cl2 → 2 NbCl5.
V laboratoři se NbCl5 často připravuje chlorací Nb2O5 v přítomnosti uhlíku za teploty 300 °C, ovšem při nedokončení reakce vznikají oxyhalogenidy (Produkt obsahuje malé množství NbOCl3). Konverze může být efektivnější s použitím chloridu thionylu.[4]
Použití
Chlorid niobičný je často používán jako prekurzor ostatních sloučenin niobu.
Je hlavním prekurzorem alkoxidů niobu. Je také prekurzorem mnoha ostatních laboratorních činidel.
Podobné sloučeniny
- Fluorid niobičný
- Bromid niobičný
- Jodid niobičný
Reference
V tomto článku byl použit překlad textu z článku Niobium(V) chloride na anglické Wikipedii.
- Niobium pentachloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- Cotton, F. Albert; Wilkinson, Geoffrey (1980), Advanced Inorganic Chemistry (4th ed.), New York: Wiley, ISBN 0-471-02775-8
- Joachim Eckert, Hermann C. Starck "Niobium and Niobium Compounds" Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. DOI|10.1002/14356007.a17_251
- D. Brown "Niobium(V) Chloride and Hexachloroniobates(V)" Inorganic Syntheses, 1957 Volume 9, pp. 88–92.DOI|10.1002/9780470132401.ch24
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid niobičný na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid niobičný na Wikimedia Commons

